Clear Sky Science · pl
Edytowanie R-pętli przez deaminazę cytozyny w DNA APOBEC3B modyfikuje aktywność enhancerów receptora estrogenowego
Dlaczego to badanie ma znaczenie
Wiele raków piersi zależy od hormonu estrogenowego, by rosnąć. Te same sygnały, które włączają kluczowe geny, mogą też uszkadzać DNA, co wspomaga ewolucję nowotworu i oporność na leczenie. Badanie ujawnia, jak naturalnie występująca enzymatyczna „korekta” DNA — APOBEC3B — współdziała z receptorami estrogenowymi przy regulatorowych przełącznikach DNA zwanych enhancerami. Pokazując dokładnie, gdzie i jak działa ten enzym, praca łączy normalną, napędzaną hormonami kontrolę genów z mutacjami i pęknięciami, które destabilizują genom nowotworu, i sugeruje nowe możliwości celowania w guzy zależne od hormonów.
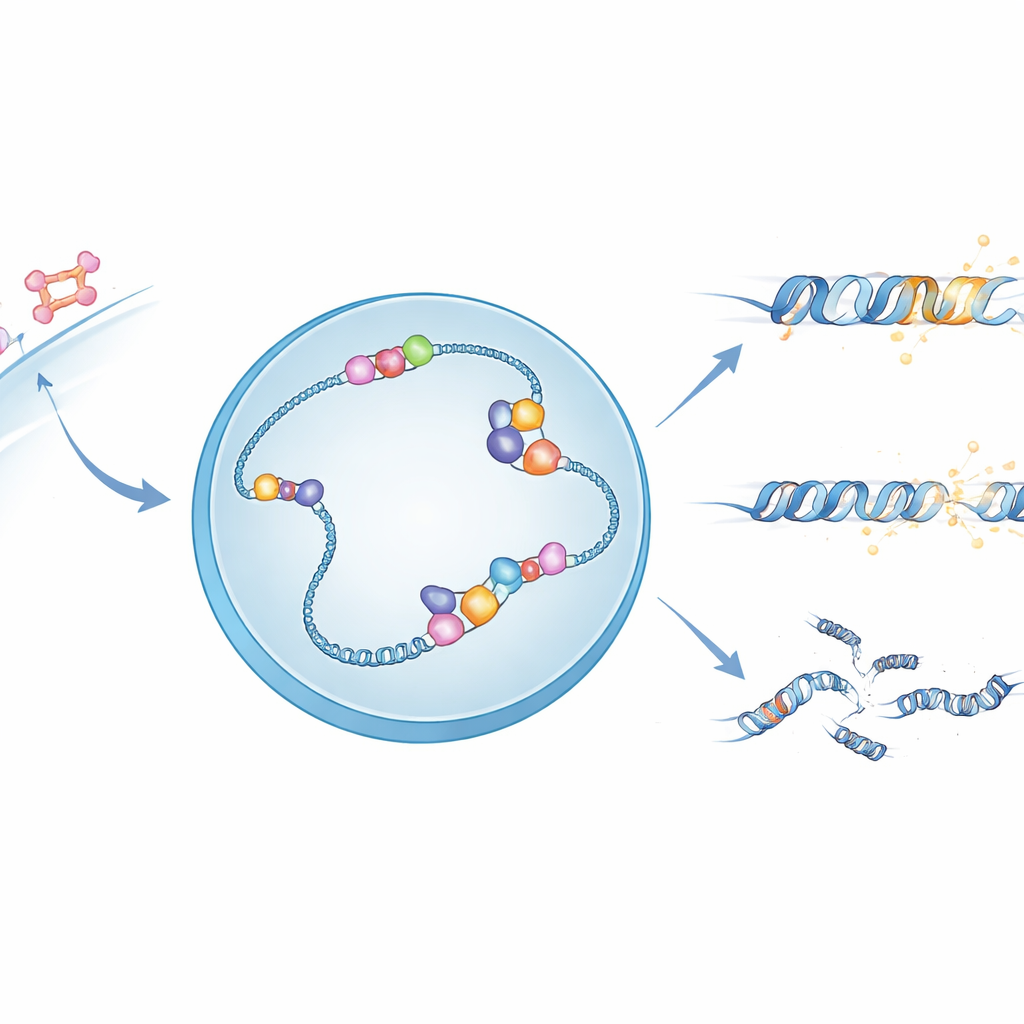
Sygnały hormonalne i kruche struktury DNA
Gdy estrogen wnika do komórki, aktywuje receptor estrogenowy — białko, które trafia do jądra i wiąże się z określonymi miejscami w DNA, kontrolując pobliskie geny. W wielu z tych miejsc odczytywanie DNA na RNA tworzy nietypowe, trójcząsteczkowe struktury zwane R-pętlami, w których nowy RNA przylega do jednej nici DNA, a druga nić pozostaje odsłonięta. R-pętle mogą pomagać w regulacji genów, ale też czynią DNA bardziej kruche i podatne na złamania. Autorzy przypuszczali, że APOBEC3B — enzym już znany z chemicznej modyfikacji pojedynczych nici DNA — może wykorzystywać odsłoniętą nić w R-pętlach jako preferowane miejsce działania.
Mapowanie miejsc, gdzie uderza edytor DNA
Aby zobaczyć ślady APOBEC3B w całym genomie, zespół zmodyfikował komórki raka piersi tak, by kluczowa ścieżka naprawy DNA, naprawa przez wycinanie zasad, była zablokowana. Dzięki temu chemiczne modyfikacje wprowadzone przez APOBEC3B pozostawały dostatecznie długo, by zarejestrować je przez sekwencjonowanie całogenomowe. Odkryli, że charakterystyczne mutacje tego enzymu skupiają się nie w regionach kodujących białka, lecz w DNA regulatorowym w pobliżu miejsc startu genów i enhancerów, zwłaszcza w obszarach, które replikują się wcześnie i są wysoce aktywne. Zmienione miejsca miały tendencję do występowania w sekwencjach sprzyjających tworzeniu R-pętli, co sugeruje ścisły związek APOBEC3B z tymi przejściowymi strukturami DNA:RNA.
Bezpośredni dowód, że APOBEC3B działa na R-pętlach
Następnie badacze zastosowali dwa metody ogniskujące cały genom, aby obserwować APOBEC3B i R-pętle w działaniu. Jedna metoda wyłapywała hybrydy DNA:RNA, a druga izolowała pojedyncze nici DNA związane z oznakowanym APOBEC3B. Wspólnie wykazały, że enzym lokuje się w samych R-pętlach i chemicznie przekształca cytozynę w uracyl na odsłoniętej nici DNA. Gdy nadprodukowano enzym usuwający R-pętle (RNaza H1), wiązanie APOBEC3B gwałtownie spadło, co potwierdza, że R-pętle są niezbędnymi platformami dokującymi. Po krótkiej stymulacji estrogenem zarówno R-pętle, jak i wiązanie APOBEC3B wzrosły w promotorach i szczególnie na aktywnie transkrybowanych enhancerach używanych przez receptor estrogenowy, łącząc sygnalizację hormonalną z falami edycji DNA zależnej od R-pętli.
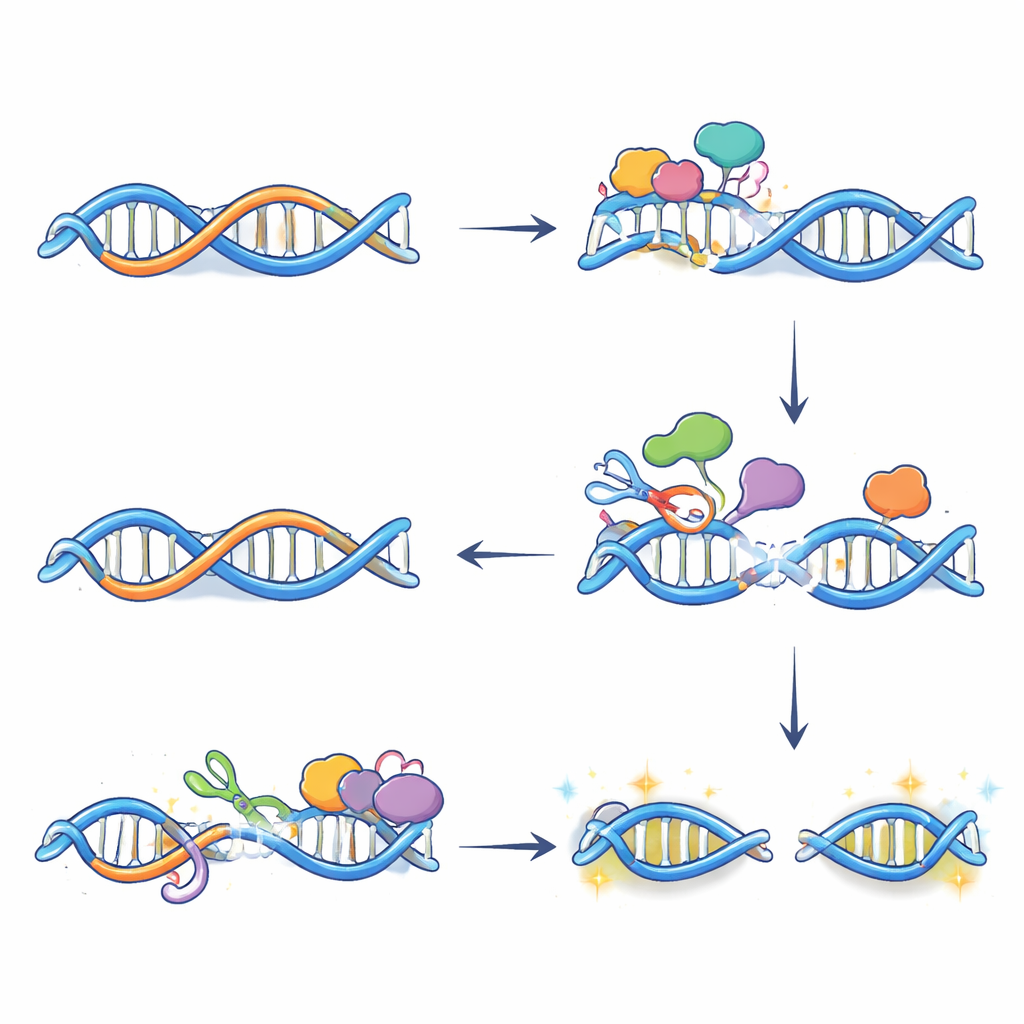
Od chemicznych poprawek do złamań DNA i aktywacji genów
Sama edycja nie powoduje złamań DNA; uszkodzenie powstaje, gdy systemy naprawcze przetwarzają zmienione zasady. Używając techniki znakowania końców złamanych nici DNA, autorzy pokazali, że wiele dwuniciowych złamań pojawiających się po leczeniu estrogenem zależy od APOBEC3B i występuje dokładnie tam, gdzie współistnieją R-pętle i enzym. Dalsze eksperymenty wykazały, że dwie ścieżki naprawcze — naprawa przez wycinanie zasad i transkrypcyjnie sprzężona naprawa przez wycinanie nukleotydów — współdziałają w tych miejscach. Każda wprowadza nacięcie na przeciwległej nici DNA w pobliżu R-pętli; gdy nacięcia się spotkają, powstaje pełne złamanie. Zablokowanie aktywności APOBEC3B lub etapów naprawy zmniejszało te złamania i tłumiło normalny wzrost ekspresji wielu genów reagujących na estrogen, co wskazuje, że kontrolowane uszkodzenia DNA pomagają ustanowić bardziej otwarty, aktywny stan chromatyny na kluczowych enhancerach.
Co to oznacza dla raka i terapii
Ta praca ukazuje APOBEC3B jako miecz obosieczny w hormonozależnym raku piersi. Edytując DNA w R-pętlach w pobliżu enhancerów receptora estrogenowego, przyczynia się do powstawania tymczasowych złamań DNA, które przebudowują chromatynę i zwiększają ekspresję genów sprzyjających wzrostowi. Jednocześnie te zdarzenia pozostawiają blizny — mutacje i zmiany strukturalne — które napędzają niestabilność genomu i ewolucję guza. Zrozumienie tego sprzężenia między sygnalizacją hormonalną, biologią R-pętli i edycją DNA wskazuje APOBEC3B oraz powiązane etapy naprawcze jako potencjalne cele terapeutyczne. Hamowanie tego obwodu mogłoby osłabić szkodliwą aktywację genów i spowolnić genetyczną dywersyfikację leżącą u podstaw oporności na terapie, takie jak tamoksyfen.
Cytowanie: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Słowa kluczowe: receptor estrogenowy, APOBEC3B, R-pętle, rak piersi, uszkodzenia DNA