Clear Sky Science · nl
R-loopbewerking door DNA-cytosinedeaminase APOBEC3B reguleert de activiteit van oestrogeenreceptor-enhancers
Waarom dit onderzoek ertoe doet
Veel borstkankers zijn afhankelijk van het hormoon oestrogeen om te groeien. Dezelfde signalen die vitale genen aanzetten, kunnen ook DNA beschadigen en zo tumoren helpen evolueren en behandelingsresistentie veroorzaken. Deze studie onthult hoe een van nature voorkomende DNA-bewerkende enzym, APOBEC3B, samenwerkt met oestrogeenreceptoren bij regulatorische DNA-schakelaars die enhancers worden genoemd. Door precies aan te tonen waar en hoe dit enzym werkt, brengt het werk normale hormoongestuurde genregulatie in verband met de mutaties en breuken die het kankergenoom destabiliseren en wijst het op nieuwe mogelijkheden om hormoonafhankelijke tumoren te bestrijden.
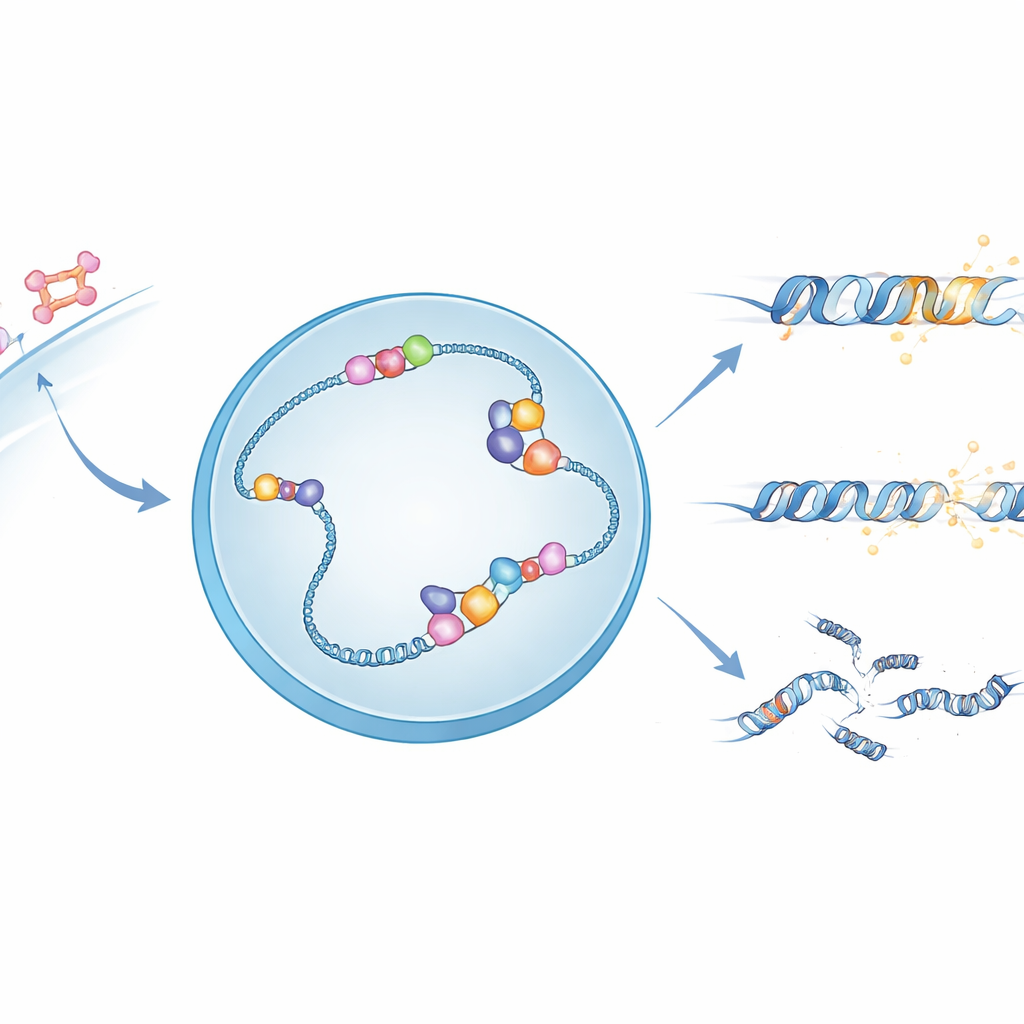
Hormoonsignalen en kwetsbare DNA-structuren
Wanneer oestrogeen een cel binnendringt, activeert het de oestrogeenreceptor, een eiwit dat naar de kern gaat en aan specifieke DNA-locaties bindt om naburige genen te regelen. Op veel van deze plaatsen veroorzaakt het aflezen van DNA naar RNA ongewone driedubbele structuren die R-loops worden genoemd, waarbij het nieuw gevormde RNA aan één DNA-streng hecht en de andere streng blootlegt. Deze R-loops kunnen genen helpen reguleren, maar ze maken het DNA ook kwetsbaarder en gevoeliger voor breukvorming. De auteurs vermoedden dat APOBEC3B, een enzym dat al bekendstaat om chemische aanpassingen aan enkelstrengs DNA, mogelijk de blootgestelde streng in R-loops gebruikt als zijn voorkeursvlak.
In kaart brengen waar de DNA-editor toeslaat
Om het voetafdruk van APOBEC3B over het genoom te zien, maakten de onderzoekers borstkankercellen waarin een belangrijke DNA-reparatieweg, base excision repair, was geblokkeerd. Dat betekende dat chemische aanpassingen door APOBEC3B lang genoeg zichtbaar bleven om met whole-genome sequencing te worden vastgelegd. Ze vonden dat de karakteristieke mutaties van dit enzym zich niet in eiwitcoderende regio’s concentreerden, maar in regulatorisch DNA bij genstarters en enhancers, vooral in zones die vroeg repliceren en zeer actief zijn. Deze bewerkte plekken lagen vaak in sequenties die de bouwstenen bevatten die R-loopvorming bevorderen, wat suggereert dat APOBEC3B nauw verbonden is met deze tijdelijke DNA:RNA-structuren.
Direct bewijs dat APOBEC3B op R-loops werkt
De onderzoekers gebruikten vervolgens twee genoomwijde assays om APOBEC3B en R-loops in actie te volgen. De ene methode trok DNA:RNA-hybriden naar zich toe, terwijl de andere enkelstrengs DNA vastlegde dat gebonden was door getagd APOBEC3B. Gezamenlijk toonden ze aan dat het enzym zich precies binnen R-loops bevindt en cytosinebasen op de blootgestelde DNA-streng chemisch omzet in uracil. Wanneer een enzym dat R-loops verwijdert (RNase H1) overgeproduceerd werd, daalde de binding van APOBEC3B sterk, wat bevestigt dat R-loops essentiële aanlegplaatsen zijn. Bij korte oestrogeentoediening stegen zowel R-loops als APOBEC3B-bindingen op promoters en vooral op actief getranscribeerde enhancers die door de oestrogeenreceptor worden gebruikt, waarmee hormoonsignalen gekoppeld werden aan uitbarstingen van R-loop-afhankelijke DNA-bewerking.
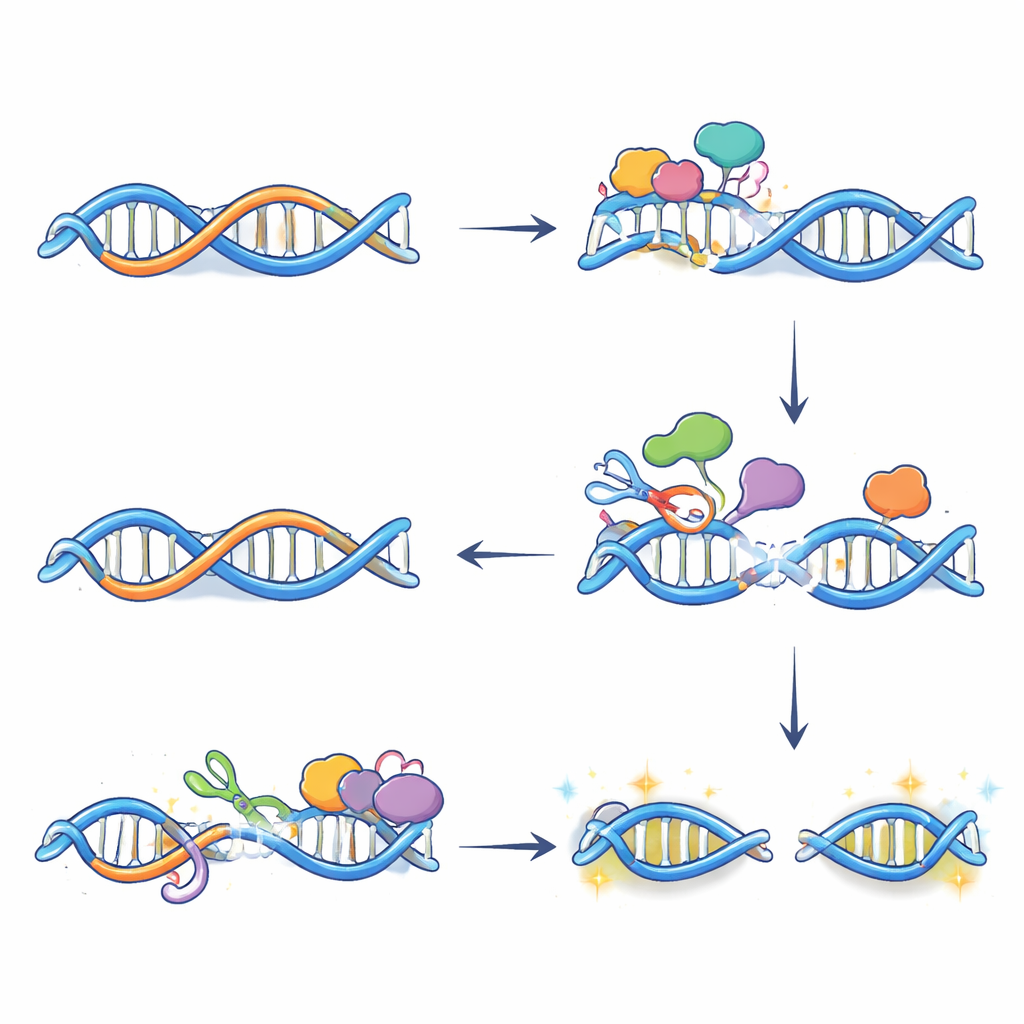
Van chemische aanpassingen naar DNA-breuken en genactivatie
Alleen bewerking breekt het DNA niet; de schade ontstaat wanneer reparatiesystemen deze gewijzigde basen verwerken. Met een techniek die de uiteinden van gebroken DNA labelt, toonden de auteurs aan dat veel dubbelstrengsbreuken die na oestrogeentoediening verschenen afhankelijk waren van APOBEC3B en precies voorkwamen waar R-loops en het enzym samenvielen. Verdere experimenten toonden aan dat twee reparatiepaden — base excision repair en transcription-coupled nucleotide excision repair — samen op deze locaties werken. Elk brengt sneden aan op tegenoverliggende DNA-strengen in de buurt van de R-loop; wanneer die sneden samenvallen, ontstaat een volledige breuk. Het blokkeren van óf de activiteit van APOBEC3B óf de reparatiestappen verminderde deze breuken en dempte de normale toename in expressie van veel oestrogeenresponsieve genen, wat aangeeft dat zorgvuldig gecontroleerde DNA-schade daadwerkelijk helpt een openere, actievere chromatine-toestand bij belangrijke enhancers te vestigen.
Wat dit betekent voor kanker en therapie
Dit werk portretteert APOBEC3B als een tweesnijdend zwaard bij hormoongestuurde borstkanker. Door DNA te bewerken bij R-loops nabij oestrogeenreceptor-enhancers helpt het tijdelijke DNA-breuken te creëren die chromatine herstructureren en de expressie van groeibevorderende genen verhogen. Tegelijkertijd laten deze gebeurtenissen littekens achter — mutaties en structurele veranderingen — die genomische instabiliteit en tumorevolutie aanwakkeren. Inzicht in deze koppeling tussen hormoonsignalering, R-loopbiologie en DNA-bewerking benadrukt APOBEC3B en de bijbehorende reparatiestappen als potentiële medicatiedoelen. Het remmen van dit circuit zou schadelijke genactivering kunnen dempen en de genetische diversificatie die ten grondslag ligt aan resistentie tegen behandelingen zoals tamoxifen kunnen vertragen.
Bronvermelding: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Trefwoorden: oestrogeenreceptor, APOBEC3B, R-loops, borstkanker, DNA-schade