Clear Sky Science · es
Edición de R-loops por la desaminasa de citosina del ADN APOBEC3B modula la actividad de los potenciadores del receptor de estrógeno
Por qué importa esta investigación
Muchos cánceres de mama dependen de la hormona estrógeno para crecer. Las mismas señales que activan genes esenciales también pueden dañar el ADN, ayudando a los tumores a evolucionar y resistir los tratamientos. Este estudio revela cómo una enzima editora de ADN que ocurre de forma natural, APOBEC3B, actúa junto con los receptores de estrógeno en interruptores regulatorios del ADN llamados potenciadores. Al mostrar exactamente dónde y cómo actúa esta enzima, el trabajo vincula el control normal de genes impulsado por hormonas con las mutaciones y roturas que desestabilizan el genoma del cáncer y sugiere nuevas formas de dirigirse a tumores dependientes de hormonas.
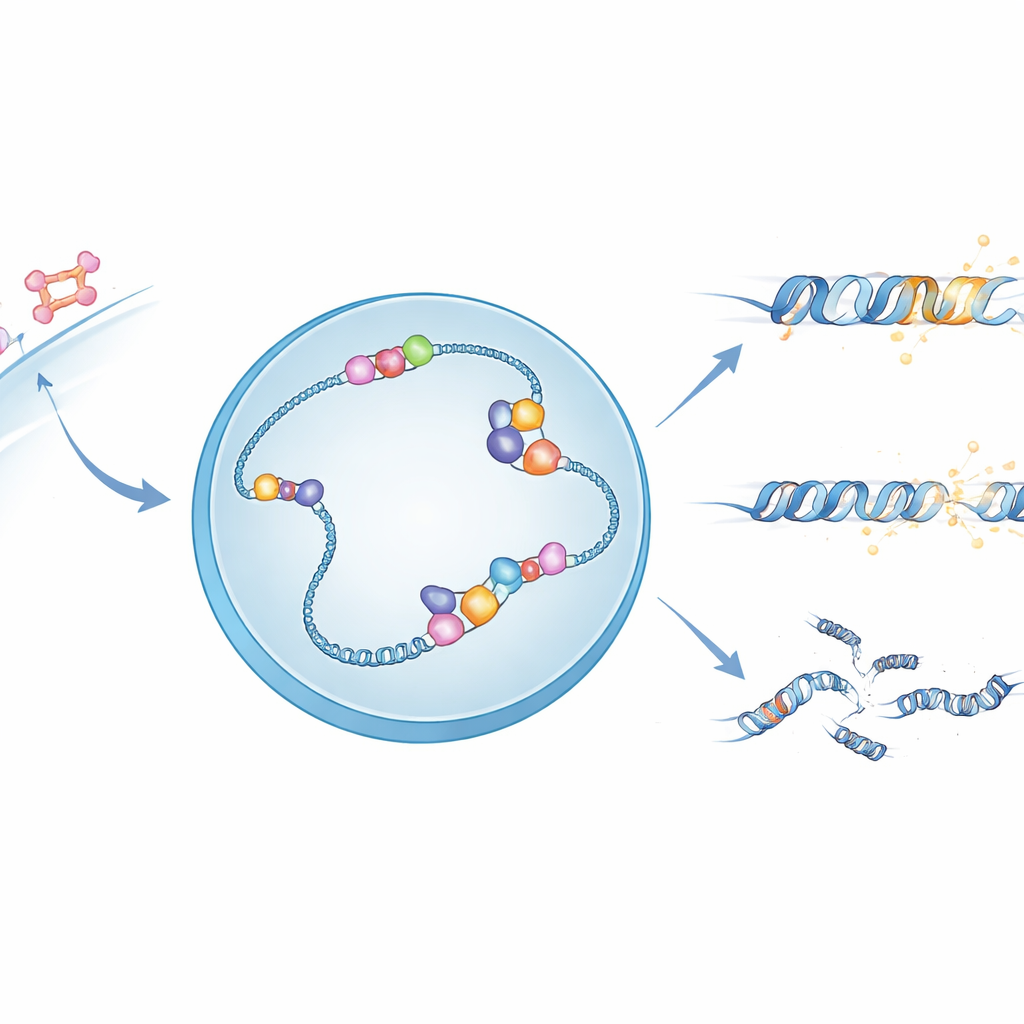
Señales hormonales y estructuras frágiles del ADN
Cuando el estrógeno entra en una célula, activa el receptor de estrógeno, una proteína que viaja al núcleo y se une a sitios específicos del ADN para controlar genes cercanos. En muchos de estos sitios, el acto de leer el ADN en ARN genera estructuras inusuales de tres cadenas llamadas R-loops, donde el ARN recién sintetizado se empareja con una hebra de ADN dejando la otra hebra expuesta. Estos R-loops pueden ayudar a regular genes, pero también hacen que el ADN sea más frágil y propenso a romperse. Los autores sospecharon que APOBEC3B, una enzima ya conocida por modificar químicamente el ADN de hebra simple, podría estar usando la hebra expuesta en los R-loops como su superficie de trabajo preferida.
Mapeando dónde actúa el editor de ADN
Para ver la huella de APOBEC3B en el genoma, el equipo diseñó células de cáncer de mama en las que una vía clave de reparación del ADN, la reparación por escisión de bases, estaba bloqueada. Esto permitió que las modificaciones químicas hechas por APOBEC3B permanecieran visibles el tiempo suficiente para ser capturadas por secuenciación del genoma completo. Encontraron que las mutaciones características producidas por esta enzima se agrupaban no en regiones codificantes de proteínas, sino en ADN regulador cerca de sitios de inicio de genes y potenciadores, especialmente en zonas que se replican temprano y están muy activas. Estos puntos editados tendían a localizarse en secuencias enriquecidas en los nucleótidos que favorecen la formación de R-loops, lo que sugiere que APOBEC3B está íntimamente ligado a estas estructuras transitorias ADN:ARN.
Prueba directa de que APOBEC3B actúa sobre R-loops
Los investigadores usaron entonces dos ensayos a escala del genoma para observar APOBEC3B y los R-loops en acción. Un método aisló híbridos ADN:ARN, mientras que otro capturó hebras simples de ADN unidas a APOBEC3B etiquetada. Juntos mostraron que la enzima se sitúa directamente dentro de los R-loops y convierte químicamente citosinas en uracilos en la hebra de ADN expuesta. Cuando se sobreexpresó una enzima que elimina R-loops (RNasa H1), la unión de APOBEC3B cayó bruscamente, confirmando que los R-loops son plataformas esenciales de anclaje. Tras una estimulación corta con estrógeno, tanto los R-loops como la unión de APOBEC3B aumentaron en promotores y, en particular, en potenciadores activamente transcritos utilizados por el receptor de estrógeno, vinculando la señal hormonal con ráfagas de edición del ADN dependientes de R-loops.
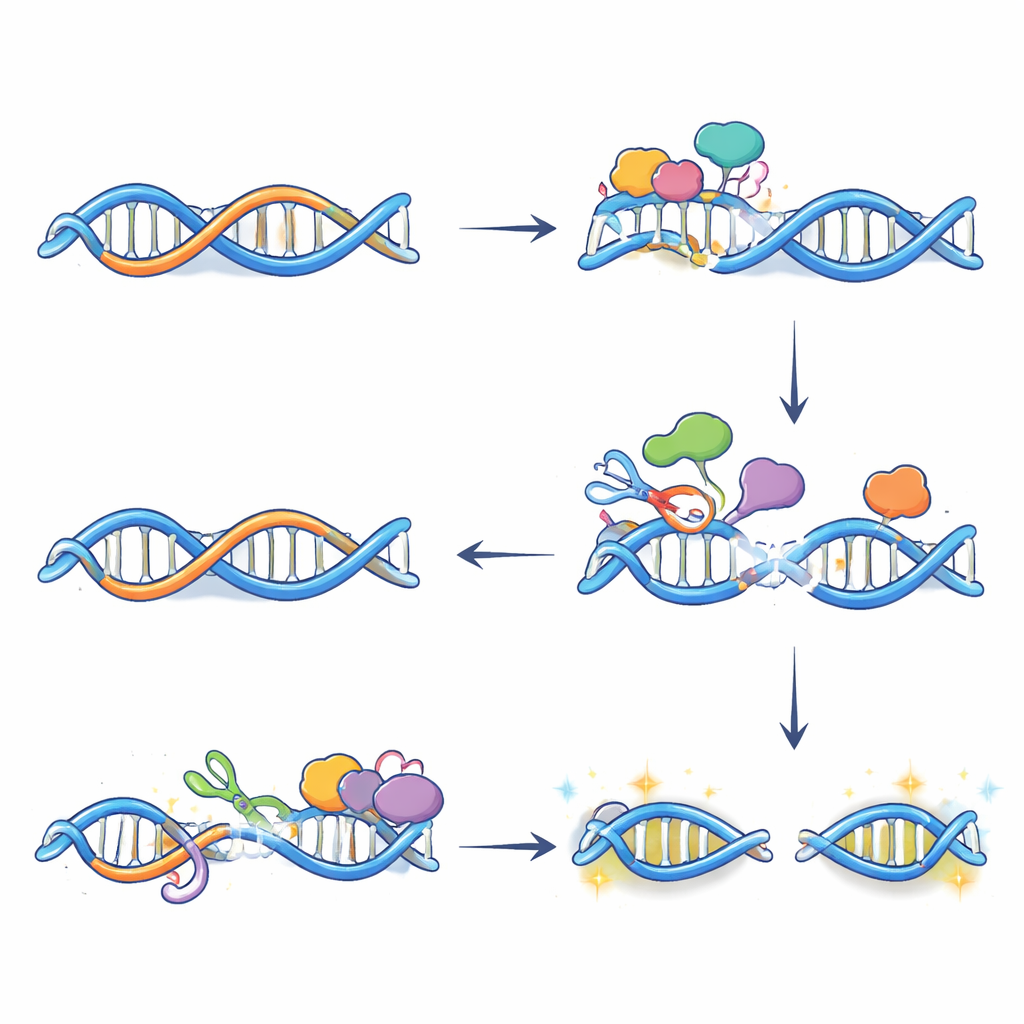
De las modificaciones químicas a las roturas de ADN y la activación génica
La edición por sí sola no rompe el ADN; el daño surge cuando los sistemas de reparación procesan estas bases alteradas. Usando una técnica que marca los extremos de ADN roto, los autores mostraron que muchas roturas de doble hebra que aparecen tras el tratamiento con estrógeno dependen de APOBEC3B y ocurren exactamente donde coinciden R-loops y la enzima. Experimentos adicionales revelaron que dos vías de reparación—reparación por escisión de bases y reparación por escisión de nucleótidos acoplada a la transcripción—trabajan conjuntamente en estos sitios. Cada una introduce cortes en hebras opuestas del ADN cerca del R-loop; cuando los cortes se encuentran, se forma una rotura completa. Bloquear la actividad de APOBEC3B o los pasos de reparación redujo estas roturas y atenuó el aumento habitual en la expresión de muchos genes sensibles al estrógeno, lo que indica que un daño en el ADN cuidadosamente controlado ayuda en realidad a establecer un estado de cromatina más abierto y activo en potenciadores clave.
Qué significa esto para el cáncer y la terapia
Este trabajo presenta a APOBEC3B como una espada de doble filo en el cáncer de mama impulsado por hormonas. Al editar el ADN en R-loops cerca de potenciadores del receptor de estrógeno, contribuye a generar roturas temporales del ADN que remodelan la cromatina y aumentan la expresión de genes que promueven el crecimiento. Al mismo tiempo, estos eventos dejan cicatrices—mutaciones y cambios estructurales—que alimentan la inestabilidad genómica y la evolución tumoral. Comprender esta conexión entre la señalización hormonal, la biología de los R-loops y la edición del ADN destaca a APOBEC3B y a los pasos de reparación asociados como posibles dianas farmacológicas. Inhibir este circuito podría reducir la activación génica dañina y frenar la diversificación genética que subyace a la resistencia a tratamientos como el tamoxifeno.
Cita: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Palabras clave: receptor de estrógeno, APOBEC3B, R-loops, cáncer de mama, daño en el ADN