Clear Sky Science · fr
Édition des R-loops par la cytidine désaminase APOBEC3B module l’activité des enhancers du récepteur des œstrogènes
Pourquoi cette recherche est importante
De nombreux cancers du sein dépendent de l’hormone œstrogène pour croître. Les mêmes signaux qui activent des gènes essentiels peuvent aussi endommager l’ADN, favorisant l’évolution des tumeurs et la résistance aux traitements. Cette étude révèle comment une enzyme d’édition de l’ADN naturellement présente, APOBEC3B, coopère avec les récepteurs des œstrogènes sur des interrupteurs régulateurs de l’ADN appelés enhancers. En montrant où et comment cette enzyme agit, le travail relie le contrôle génique normal piloté par les hormones aux mutations et cassures qui déstabilisent le génome tumoral et suggère de nouvelles voies pour cibler les tumeurs dépendantes des hormones.
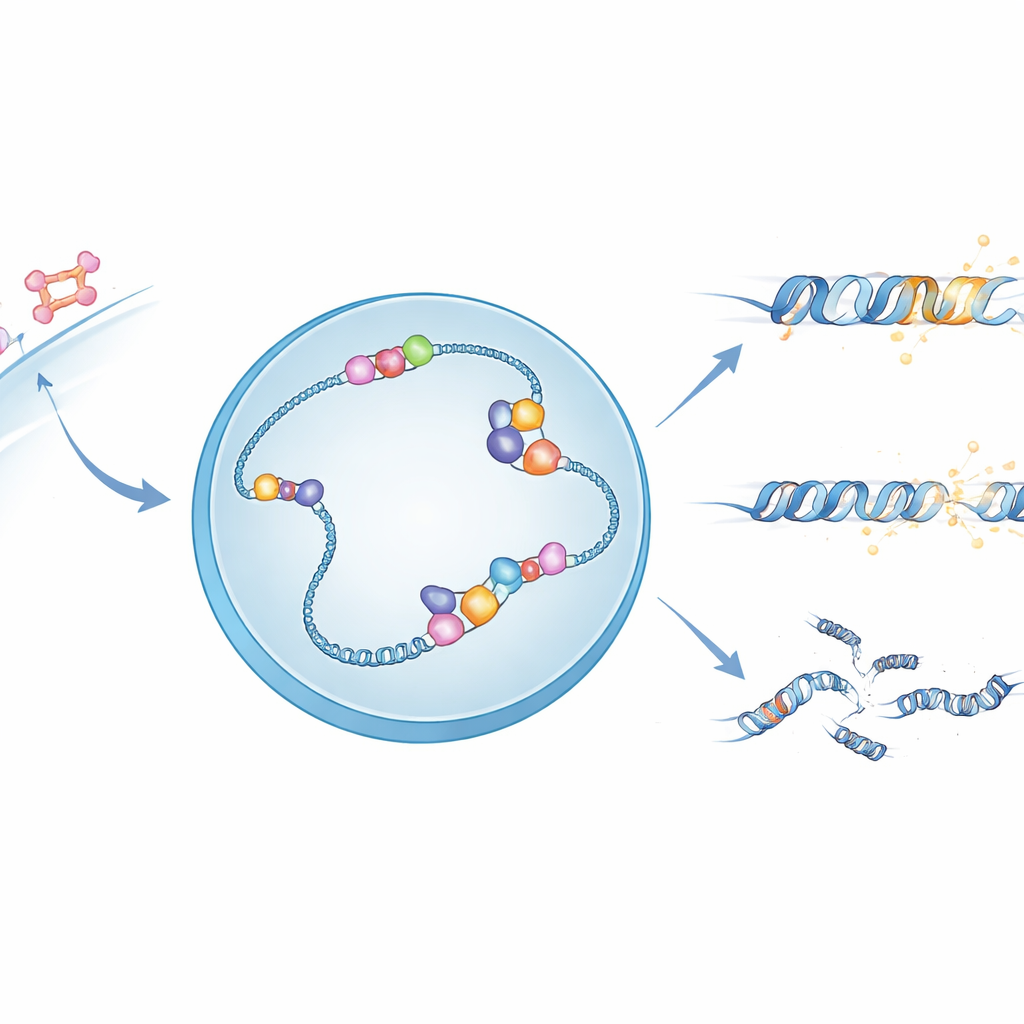
Signaux hormonaux et structures fragiles de l’ADN
Lorsque l’œstrogène pénètre dans une cellule, il active le récepteur des œstrogènes, une protéine qui se rend dans le noyau et se lie à des sites d’ADN spécifiques pour contrôler les gènes voisins. En de nombreux de ces sites, la transcription de l’ADN en ARN génère des structures inhabituelles à trois brins appelées R-loops, où l’ARN nouvellement formé s’apparie à un brin d’ADN et laisse l’autre brin exposé. Ces R-loops peuvent aider à réguler les gènes, mais ils rendent aussi l’ADN plus fragile et susceptible de se rompre. Les auteurs ont émis l’hypothèse qu’APOBEC3B, une enzyme déjà connue pour modifier chimiquement l’ADN simple brin, pourrait utiliser le brin exposé dans les R-loops comme son substrat préféré.
Cartographier l’empreinte de l’éditeur d’ADN
Pour visualiser l’empreinte d’APOBEC3B sur le génome, l’équipe a conçu des cellules de cancer du sein dans lesquelles une voie clé de réparation de l’ADN, la réparation par excision de base, était bloquée. Ainsi, les modifications chimiques effectuées par APOBEC3B demeuraient visibles suffisamment longtemps pour être capturées par séquençage du génome entier. Ils ont constaté que les mutations caractéristiques de cette enzyme se concentraient non pas dans les régions codantes des protéines, mais dans l’ADN régulateur proche des sites d’initiation des gènes et des enhancers, en particulier dans des zones répliquant tôt et très actives. Ces sites édités se trouvaient souvent dans des séquences enrichies en nucléotides favorables à la formation de R-loops, suggérant qu’APOBEC3B est étroitement lié à ces structures transitoires ADN:ARN.
Preuve directe qu’APOBEC3B agit sur les R-loops
Les chercheurs ont ensuite utilisé deux essais génomiques pour observer APOBEC3B et les R-loops en action. Une méthode a enrichi les hybrides ADN:ARN, tandis qu’une autre a capturé les brins d’ADN simples liés à APOBEC3B marqué. Ensemble, elles ont montré que l’enzyme se localise précisément à l’intérieur des R-loops et convertit chimiquement les bases cytosine en uracile sur le brin d’ADN exposé. Lorsque l’enzyme qui élimine les R-loops (RNase H1) était surexprimée, la liaison d’APOBEC3B chuta fortement, confirmant que les R-loops constituent des plates‑formes d’ancrage essentielles. Après une stimulation brève par l’œstrogène, à la fois les R-loops et la liaison d’APOBEC3B augmentèrent de façon marquée aux promoteurs et, en particulier, aux enhancers activement transcrits utilisés par le récepteur des œstrogènes, reliant la signalisation hormonale à des vagues d’édition de l’ADN dépendantes des R-loops.
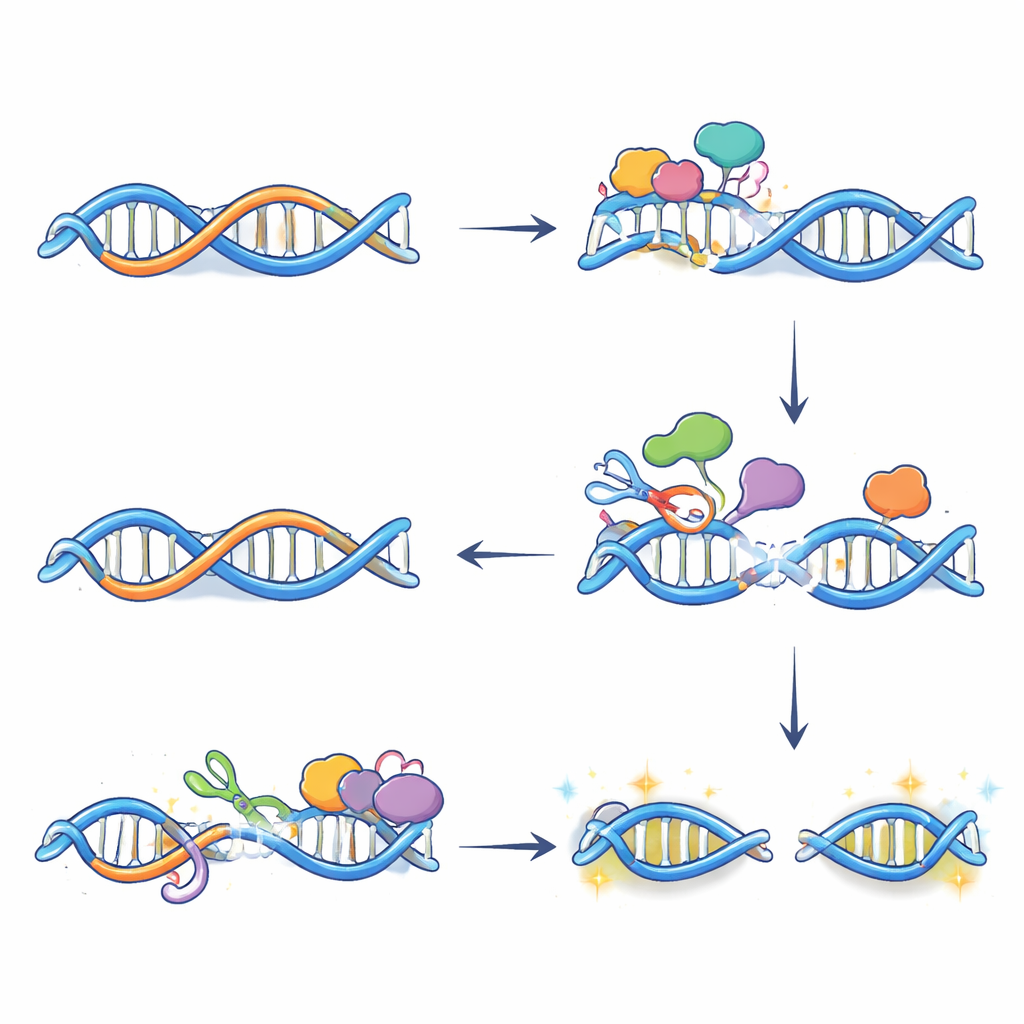
Des modifications chimiques aux cassures d’ADN et à l’activation génique
L’édition à elle seule ne rompt pas l’ADN ; les dommages surviennent lorsque les systèmes de réparation traitent ces bases altérées. À l’aide d’une technique qui marque les extrémités d’ADN cassé, les auteurs ont montré que de nombreuses cassures double brin apparaissant après traitement à l’œstrogène dépendent d’APOBEC3B et surviennent précisément là où R-loops et enzyme coïncident. Des expériences supplémentaires révélèrent que deux voies de réparation — la réparation par excision de base et la réparation par excision de nucléotides couplée à la transcription — agissent de concert en ces sites. Chacune introduit des coupures sur des brins opposés de l’ADN près du R-loop ; lorsque ces coupures se rencontrent, une cassure complète se forme. Bloquer soit l’activité d’APOBEC3B soit les étapes de réparation réduisit ces cassures et atténua la montée d’expression de nombreux gènes répondant à l’œstrogène, indiquant que des dommages à l’ADN finement régulés contribuent en réalité à établir un état de chromatine plus ouvert et actif sur des enhancers clés.
Quelles implications pour le cancer et la thérapie
Ce travail présente APOBEC3B comme une arme à double tranchant dans le cancer du sein dépendant des hormones. En éditant l’ADN au niveau des R-loops proches des enhancers du récepteur des œstrogènes, elle favorise la création de cassures d’ADN temporaires qui remodelent la chromatine et renforcent l’expression de gènes promoteurs de croissance. En même temps, ces événements laissent des cicatrices — mutations et altérations structurelles — qui alimentent l’instabilité génomique et l’évolution tumorale. Comprendre ce couplage entre la signalisation hormonale, la biologie des R-loops et l’édition de l’ADN met en lumière APOBEC3B et les étapes de réparation associées comme des cibles médicamenteuses potentielles. Inhiber ce circuit pourrait atténuer l’activation génique néfaste et ralentir la diversification génétique qui sous-tend la résistance aux traitements comme le tamoxifène.
Citation: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Mots-clés: récepteur des œstrogènes, APOBEC3B, R-loops, cancer du sein, dommages à l’ADN