Clear Sky Science · pt
Edição de R-loop pela DNA citosina desaminase APOBEC3B modula a atividade de enhancers do receptor de estrogênio
Por que esta pesquisa importa
Muitos cânceres de mama dependem do hormônio estrogênio para crescer. Os mesmos sinais que ativam genes vitais também podem danificar o DNA, ajudando tumores a evoluir e a resistir a tratamentos. Este estudo revela como uma enzima de edição de DNA presente naturalmente, a APOBEC3B, atua em conjunto com receptores de estrogênio em interruptores regulatórios do DNA chamados enhancers. Ao mostrar exatamente onde e como essa enzima age, o trabalho liga o controle gênico normal dirigido por hormônios às mutações e quebras que desestabilizam o genoma do câncer e sugere novas formas de atacar tumores dependentes de hormônio.
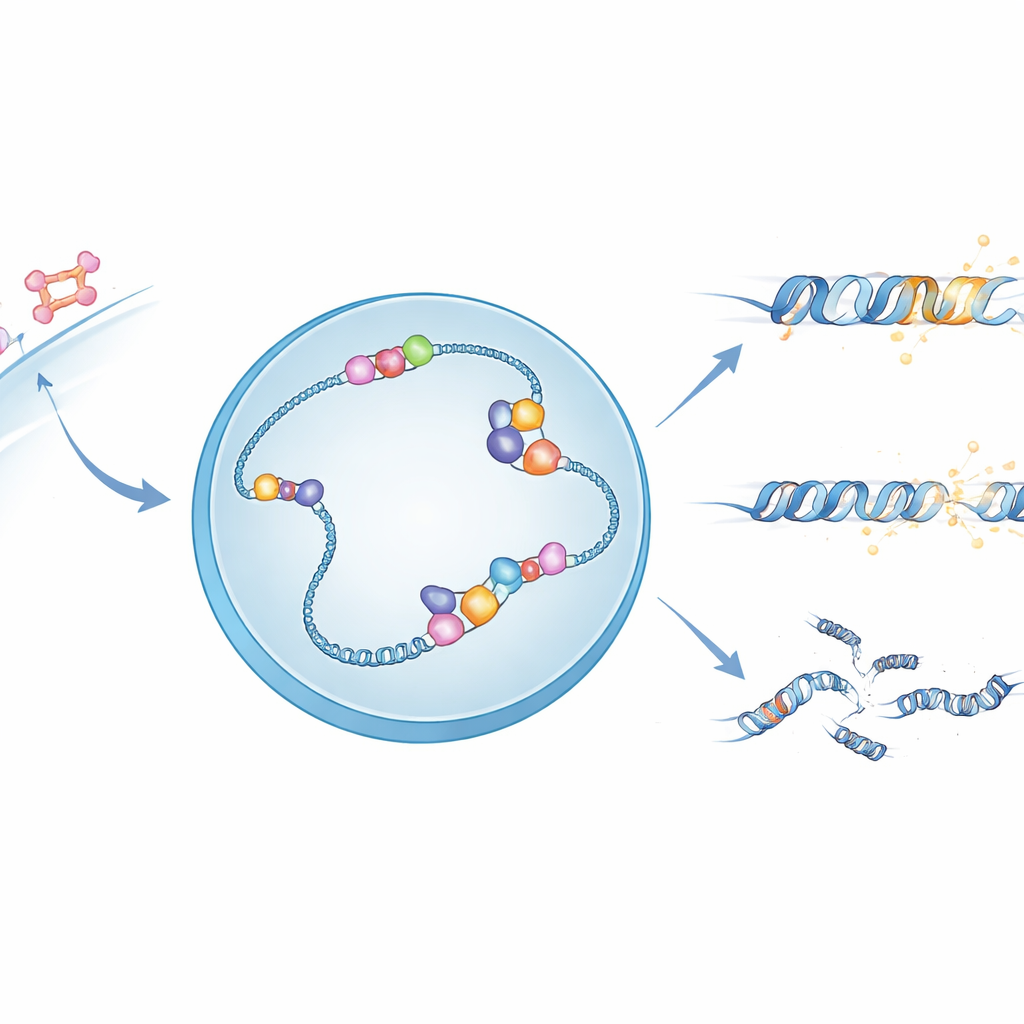
Sinais hormonais e estruturas de DNA frágeis
Quando o estrogênio entra numa célula, ele ativa o receptor de estrogênio, uma proteína que vai ao núcleo e se liga a locais específicos do DNA para controlar genes próximos. Em muitos desses locais, o ato de transcrever DNA em RNA cria estruturas incomuns de três fitas chamadas R-loops, nas quais o RNA recém-sintetizado se liga a uma das fitas de DNA e deixa a outra fita exposta. Esses R-loops podem ajudar a regular genes, mas também tornam o DNA mais frágil e sujeito a quebras. Os autores suspeitaram que a APOBEC3B, uma enzima já conhecida por modificar quimicamente DNA de fita simples, poderia estar usando a fita exposta nos R-loops como seu substrato preferencial.
Mapeando onde o editor de DNA age
Para ver a marca deixada pela APOBEC3B ao longo do genoma, a equipe modificou células de câncer de mama de modo que uma via chave de reparo de DNA, o reparo por excisão de base, ficasse bloqueada. Isso fez com que as modificações químicas realizadas pela APOBEC3B permanecessem visíveis por tempo suficiente para serem capturadas por sequenciamento de genoma completo. Eles descobriram que as mutações características dessa enzima se agrupavam não nas regiões codificadoras de proteínas, mas no DNA regulatório perto de sítios de início de genes e enhancers, especialmente em áreas que replicam cedo e são altamente ativas. Esses pontos editados tendiam a localizar-se em sequências com composição favorável à formação de R-loops, sugerindo que a APOBEC3B está intimamente ligada a essas estruturas transitórias DNA:RNA.
Prova direta de que a APOBEC3B age sobre R-loops
Os pesquisadores então usaram dois ensaios genômicos para observar a APOBEC3B e os R-loops em ação. Um método precipitou híbridos DNA:RNA, enquanto outro capturou fitas simples de DNA ligadas à APOBEC3B marcada. Em conjunto, eles mostraram que a enzima se posiciona dentro dos R-loops e converte quimicamente bases de citosina em uracil na fita de DNA exposta. Quando uma enzima que remove R-loops (RNase H1) foi superexpressa, a ligação da APOBEC3B caiu acentuadamente, confirmando que os R-loops são plataformas de ancoragem essenciais. Após estimulação curta com estrogênio, tanto os R-loops quanto a ligação da APOBEC3B aumentaram em promotores e, em particular, em enhancers transcricionalmente ativos usados pelo receptor de estrogênio, ligando a sinalização hormonal a surtos de edição de DNA dependente de R-loop.
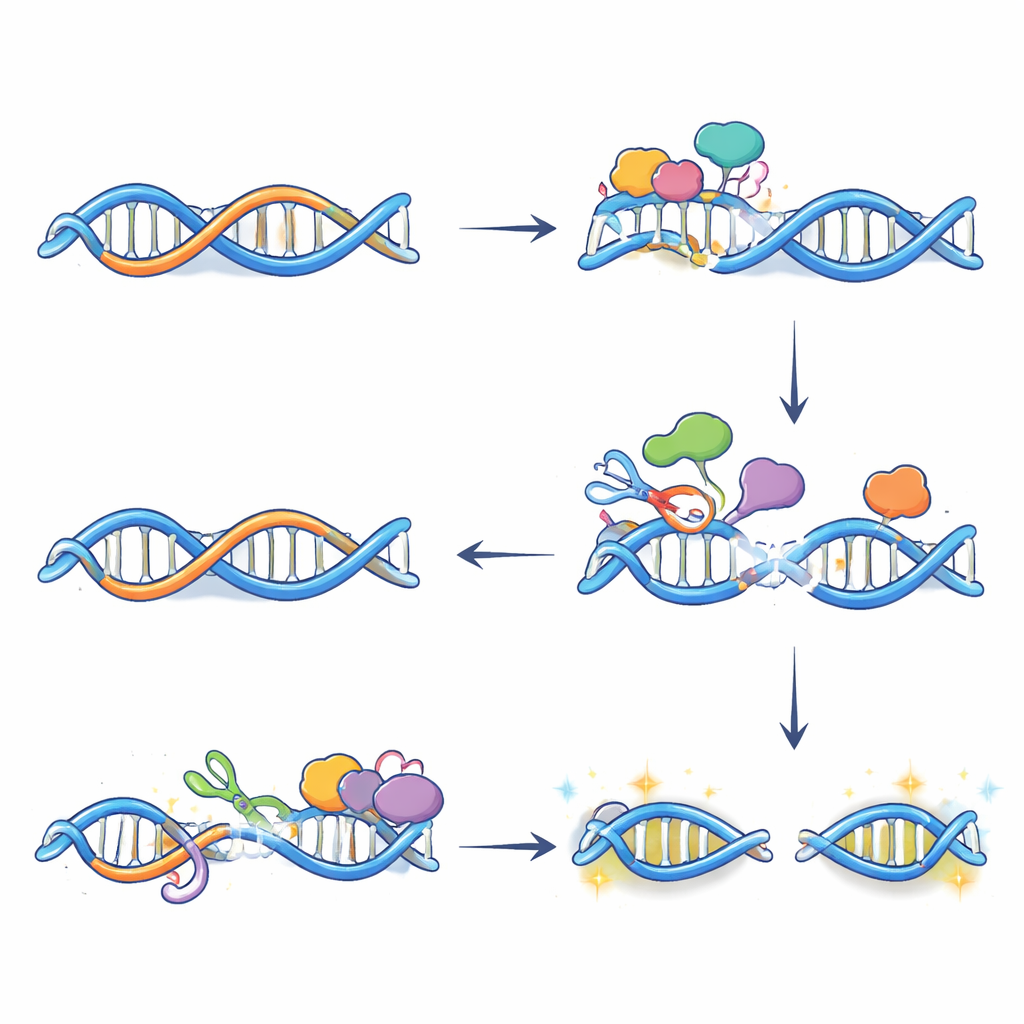
Das edições químicas às quebras de DNA e ativação gênica
A edição por si só não quebra o DNA; o dano surge quando os sistemas de reparo processam essas bases alteradas. Usando uma técnica que marca as extremidades do DNA quebrado, os autores mostraram que muitas quebras de dupla fita que aparecem após o tratamento com estrogênio dependem da APOBEC3B e ocorrem exatamente onde R-loops e a enzima coincidem. Experimentos adicionais revelaram que duas vias de reparo — reparo por excisão de base e reparo por excisão de nucleotídeo acoplado à transcrição — atuam conjuntamente nesses locais. Cada uma introduz incisões em fitas opostas do DNA próximas ao R-loop; quando as incisões se encontram, forma-se uma quebra completa. Bloquear a atividade da APOBEC3B ou os passos de reparo reduziu essas quebras e atenuou o aumento normal na expressão de muitos genes responsivos ao estrogênio, indicando que danos ao DNA controlados ajudam a estabelecer um estado de cromatina mais aberto e ativo em enhancers chave.
O que isso significa para câncer e terapia
Este trabalho descreve a APOBEC3B como uma espada de dois gumes no câncer de mama dirigido por hormônio. Ao editar o DNA em R-loops próximos a enhancers do receptor de estrogênio, ela contribui para quebras temporárias de DNA que remodelam a cromatina e aumentam a expressão de genes promotores do crescimento. Ao mesmo tempo, esses eventos deixam cicatrizes — mutações e alterações estruturais — que alimentam a instabilidade genômica e a evolução tumoral. Compreender essa conexão entre sinalização hormonal, biologia dos R-loops e edição de DNA destaca a APOBEC3B e suas etapas de reparo associadas como potenciais alvos terapêuticos. Inibir esse circuito poderia reduzir a ativação gênica prejudicial e desacelerar a diversificação genética que sustenta a resistência a tratamentos como o tamoxifeno.
Citação: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Palavras-chave: receptor de estrogênio, APOBEC3B, R-loops, câncer de mama, danos ao DNA