Clear Sky Science · it
Editing di R-loop da parte della deaminasi della citosina del DNA APOBEC3B modula l’attività degli enhancer del recettore degli estrogeni
Perché questa ricerca è importante
Molti carcinomi mammari dipendono dall’ormone estrogeno per crescere. Gli stessi segnali che attivano geni vitali possono anche danneggiare il DNA, favorendo l’evoluzione del tumore e la resistenza alle terapie. Questo studio rivela come un enzima naturale che modifica il DNA, APOBEC3B, collabori con i recettori degli estrogeni in interruttori regolatori del DNA chiamati enhancer. Mostrando esattamente dove e come agisce questo enzima, il lavoro collega il controllo genico normale guidato dagli ormoni alle mutazioni e alle rotture che destabilizzano il genoma tumorale e suggerisce nuovi modi per colpire i tumori dipendenti dagli ormoni.
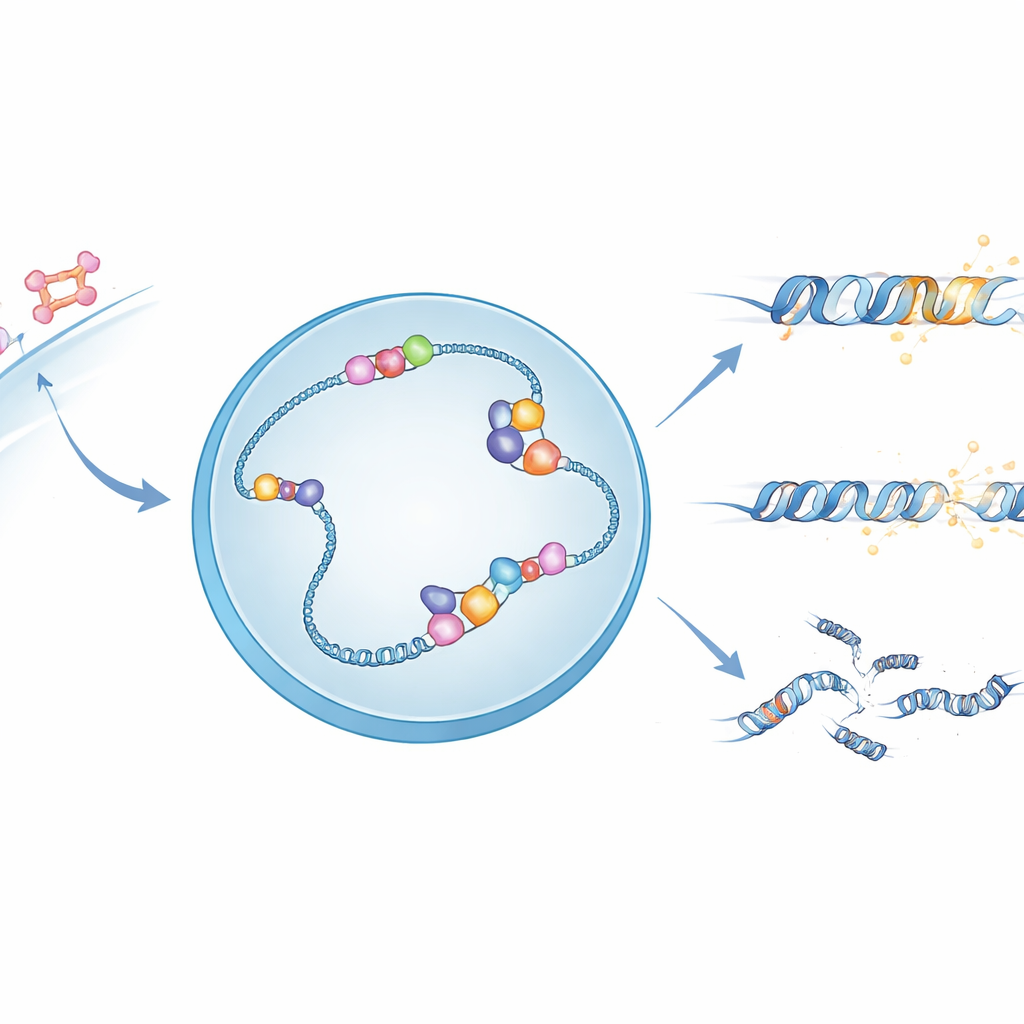
Segnali ormonali e strutture fragili del DNA
Quando l’estrogeno entra in una cellula, attiva il recettore degli estrogeni, una proteina che si sposta nel nucleo e si lega a siti specifici del DNA per controllare i geni vicini. In molti di questi siti, l’atto di trascrivere il DNA in RNA genera strutture insolite a tre filamenti chiamate R-loop, in cui il nuovo RNA si attacca a un filamento di DNA lasciando l’altro esposto. Queste R-loop possono contribuire a regolare i geni, ma rendono anche il DNA più fragile e soggetto a rotture. Gli autori hanno ipotizzato che APOBEC3B, un enzima già noto per modificare chimicamente il DNA a singolo filamento, possa usare il filamento esposto nelle R-loop come superficie preferenziale di azione.
Localizzare dove agisce l’editor del DNA
Per vedere l’impronta genomica di APOBEC3B, il gruppo ha ingegnerizzato cellule di cancro al seno in cui una via chiave di riparo del DNA, la base excision repair, era bloccata. Questo ha reso le modifiche chimiche introdotte da APOBEC3B visibili abbastanza a lungo da essere catturate dal sequenziamento dell’intero genoma. Hanno scoperto che le mutazioni caratteristiche di questo enzima si raggruppavano non nelle regioni che codificano proteine, ma nel DNA regolatorio vicino agli inizi genici e agli enhancer, in particolare nelle zone che si replicano presto e sono molto attive. Questi siti modificati tendevano a trovarsi in sequenze favorevoli alla formazione di R-loop, suggerendo che APOBEC3B sia strettamente legato a queste strutture transitorie DNA:RNA.
Prova diretta che APOBEC3B agisce sulle R-loop
I ricercatori hanno quindi usato due saggi a livello genomico per osservare APOBEC3B e le R-loop in azione. Un metodo ha isolato gli ibridi DNA:RNA, mentre un altro ha catturato i filamenti singoli di DNA legati all’APOBEC3B marcato. Insieme, hanno mostrato che l’enzima si trova proprio all’interno delle R-loop e converte chimicamente le basi citosina in uracile sul filamento di DNA esposto. Quando è stato sovraespresso un enzima che elimina le R-loop (RNase H1), il legame di APOBEC3B è calato drasticamente, confermando che le R-loop sono piattaforme essenziali di aggancio. Dopo una breve stimolazione con estrogeno, sia le R-loop sia il legame di APOBEC3B aumentavano nei promotori e, in particolare, negli enhancer trascritti attivamente usati dal recettore degli estrogeni, collegando il segnale ormonale a ondate di editing del DNA dipendenti dalle R-loop.
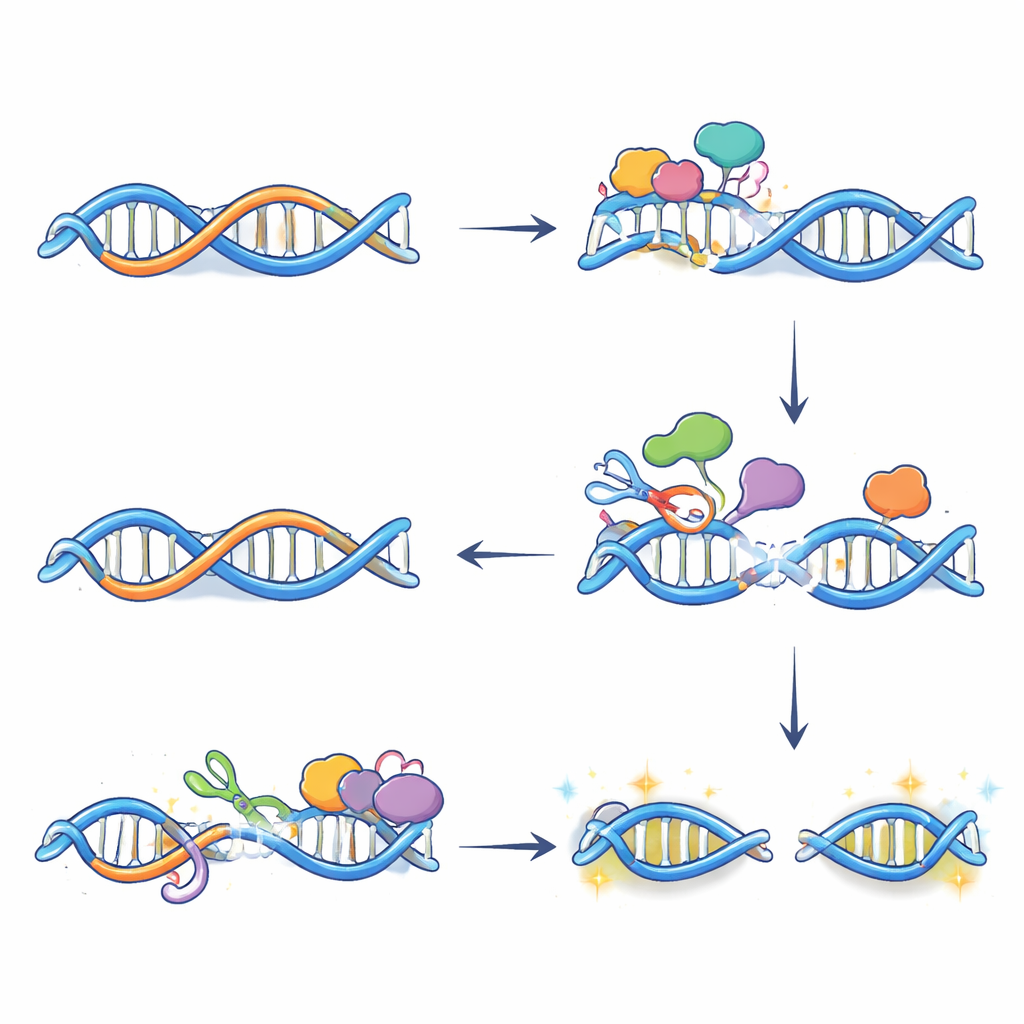
Dalle modifiche chimiche alle rotture del DNA e all’attivazione genica
L’editing da solo non rompe il DNA; il danno emerge quando i sistemi di riparo processano queste basi alterate. Utilizzando una tecnica che etichetta le estremità del DNA rotto, gli autori hanno mostrato che molte rotture a doppio filamento comparse dopo il trattamento con estrogeno dipendono da APOBEC3B e si verificano esattamente dove coincidono R-loop e enzima. Ulteriori esperimenti hanno rivelato che due vie di riparo—base excision repair e transcription-coupled nucleotide excision repair—agiscono insieme in questi siti. Ognuna introduce incisioni su filamenti opposti del DNA vicino alla R-loop; quando le incisioni si incontrano si forma una rottura completa. Bloccare l’attività di APOBEC3B o i passaggi di riparo ha ridotto queste rotture e attenuato il normale picco di espressione di molti geni sensibili all’estrogeno, indicando che danni al DNA controllati con precisione contribuiscono a stabilire uno stato di cromatina più aperto e attivo in enhancer chiave.
Cosa significa per il cancro e la terapia
Questo lavoro descrive APOBEC3B come una spada a doppio taglio nel cancro mammario guidato dagli ormoni. Modificando il DNA nelle R-loop vicino agli enhancer del recettore degli estrogeni, contribuisce a creare rotture temporanee che rimodellano la cromatina e aumentano l’espressione di geni che promuovono la crescita. Allo stesso tempo, questi eventi lasciano cicatrici—mutazioni e cambiamenti strutturali—che alimentano l’instabilità genomica e l’evoluzione del tumore. Comprendere questo accoppiamento tra segnalazione ormonale, biologia delle R-loop e editing del DNA mette in evidenza APOBEC3B e i passaggi di riparo associati come potenziali bersagli farmacologici. Inibire questo circuito potrebbe attenuare l’attivazione genica dannosa e rallentare la diversificazione genetica alla base della resistenza a terapie come il tamoxifene.
Citazione: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Parole chiave: recettore degli estrogeni, APOBEC3B, R-loop, cancro al seno, danno al DNA