Clear Sky Science · sv
R-loop-redigering av DNA-cytosin-deaminas APOBEC3B modulerar östrogenreceptorers förstärkaraktivitet
Varför denna forskning är viktig
Många bröstcancerformer är beroende av hormonet östrogen för att växa. Samma signaler som slår på viktiga gener kan också skada DNA, vilket hjälper tumörer att utvecklas och motstå behandling. Denna studie avslöjar hur ett naturligt förekommande DNA-redigerande enzym, APOBEC3B, samarbetar med östrogenreceptorer vid regulatoriska DNA-brytare kallade förstärkare. Genom att visa exakt var och hur detta enzym verkar kopplar arbetet normalt hormonstyrt genreglering till de mutationer och brott som destabiliserar cancergenenomet och pekar på nya sätt att rikta in sig på hormonberoende tumörer.
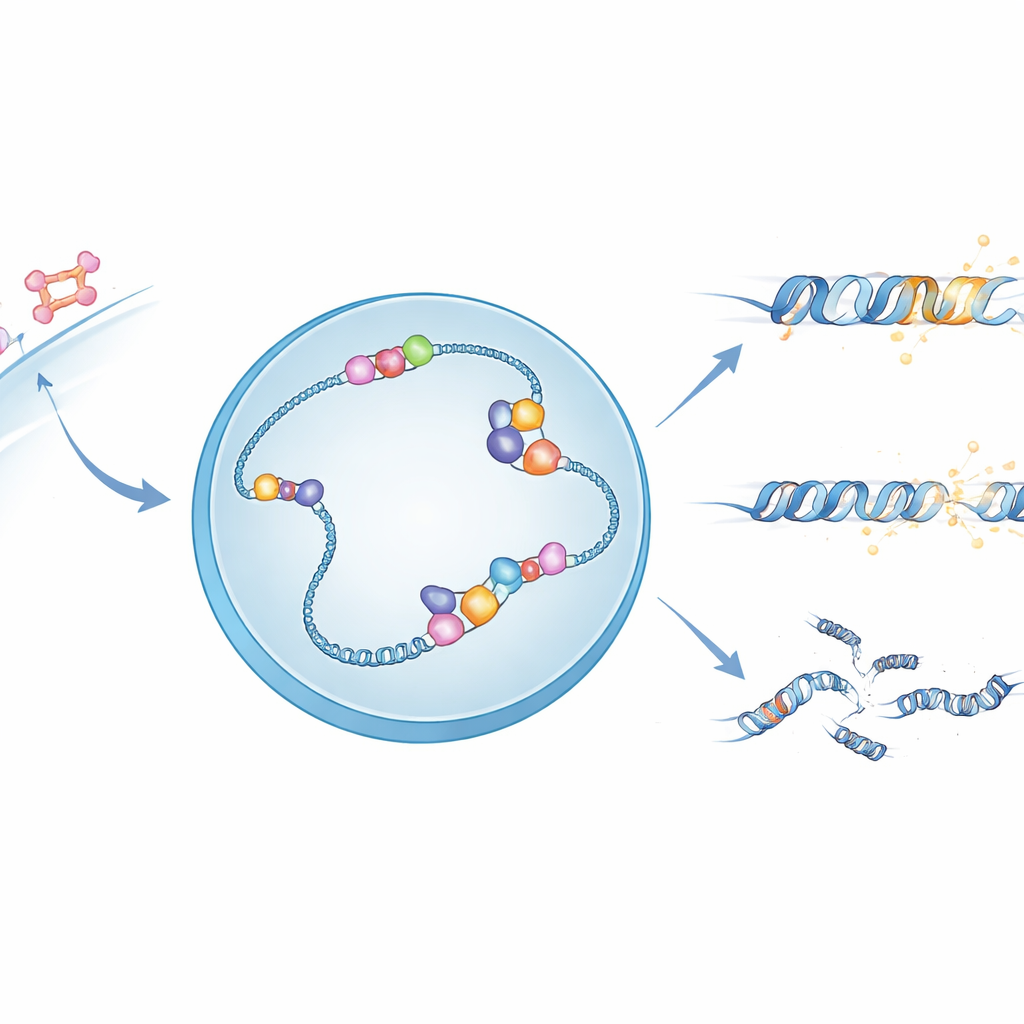
Hormonsignaler och sköra DNA-strukturer
När östrogen tar sig in i en cell aktiverar det östrogenreceptorn, ett protein som förflyttar sig till kärnan och binder specifika DNA‑platser för att styra närliggande gener. Vid många av dessa platser skapar själva processen att läsa av DNA till RNA ovanliga tretrådiga strukturer kallade R‑loopar, där den nya RNA‑kedjan fäster vid en DNA‑sträng och lämnar den andra tråden exponerad. Dessa R‑loopar kan hjälpa till att reglera gener, men de gör också DNA:t mer ömtåligt och benäget för brott. Författarna misstänkte att APOBEC3B, ett enzym som redan är känt för att kemiskt modifiera enkelsträngat DNA, kan använda den exponerade tråden i R‑loopar som sitt föredragna arbetsunderlag.
Kartläggning av var DNA-redigeraren slår till
För att se APOBEC3B:s fotavtryck över genomet konstruerade teamet bröstcancerceller där en viktig DNA-reparationsväg, basutsökningsreparation, blockerades. Det innebar att kemiska ändringar som gjorts av APOBEC3B förblev synliga tillräckligt länge för att fångas med helgenomsekvensering. De fann att de karakteristiska mutationerna som detta enzym ger upphov till inte klustrade i proteinkodande regioner, utan i regulatoriskt DNA nära genstartställen och förstärkare, särskilt i områden som replikerar tidigt och är mycket aktiva. Dessa redigerade platser låg ofta i sekvenser med en sammansättning som favoriserar R‑loopbildning, vilket antyder att APOBEC3B är intimt kopplat till dessa övergående DNA:RNA-strukturer.
Direkt bevis att APOBEC3B verkar på R-loopar
Forskarna använde sedan två genomomfattande metoder för att iaktta APOBEC3B och R‑loopar i arbete. En metod drogs ner DNA:RNA‑hybrider, medan en annan fångade enkelsträngat DNA bundet till taggat APOBEC3B. Tillsammans visade de att enzymet sitter inne i R‑looparna och kemiskt omvandlar cytosinbaser till uracil på den exponerade DNA‑tråden. När ett enzym som raderar R‑loopar (RNase H1) överproducerades, sjönk APOBEC3B‑bindningen kraftigt, vilket bekräftade att R‑loopar är nödvändiga anknytningsplattformar. Vid kort östrogenstimulering ökade både R‑loopar och APOBEC3B‑bindning kraftigt vid promotorer och särskilt vid aktivt transkriberade förstärkare som används av östrogenreceptorn, vilket knyter hormonsignalering till utbrott av R‑loop‑beroende DNA‑redigering.
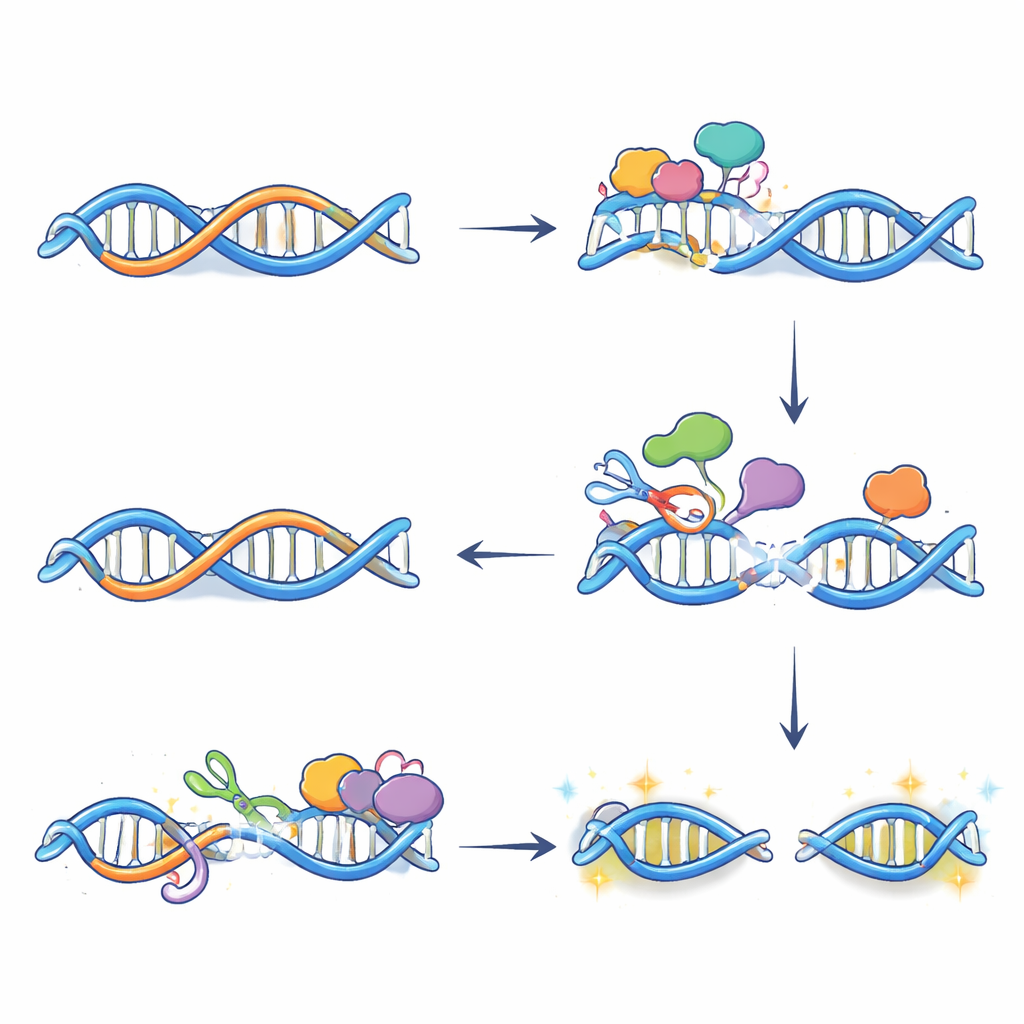
Från kemiska ändringar till DNA‑brott och genaktivering
Redigering i sig bränner inte av DNA; skadan uppstår när reparationssystem bearbetar dessa modifierade baser. Med en teknik som märker ändarna på brutet DNA visade författarna att många dubbelsträngsbrott som uppträder efter östrogenbehandling beror på APOBEC3B och inträffar exakt där R‑loopar och enzymet sammanfaller. Ytterligare experiment visade att två reparationsvägar—basutsökningsreparation och transkriptionskopplad nukleotidutbytesreparation—samarbetar vid dessa platser. Var och en introducerar snitt på motsatta DNA‑strängar nära R‑loopen; när snitten möts bildas ett fullständigt brott. Att blockera antingen APOBEC3B:s aktivitet eller reparationsstegen minskade dessa brott och dämpade den normala ökningen i uttryck av många östrogen‑responsiva gener, vilket tyder på att noggrant kontrollerade DNA‑skador faktiskt hjälper till att etablera ett mer öppet, aktivt kromatinläge vid viktiga förstärkare.
Vad detta betyder för cancer och terapi
Denne studie skildrar APOBEC3B som ett tveeggat svärd i hormonstyrd bröstcancer. Genom att redigera DNA vid R‑loopar nära östrogenreceptorförstärkare bidrar det till tillfälliga DNA‑brott som omformar kromatin och stärker uttrycket av tillväxtfrämjande gener. Samtidigt lämnar dessa händelser ärr—mutationer och strukturella förändringar—som driver genomisk instabilitet och tumöruveckling. Att förstå denna koppling mellan hormonsignalering, R‑loopbiologi och DNA‑redigering framhäver APOBEC3B och dess associerade reparationssteg som potentiella läkemedelsmål. Att hämma denna krets skulle kunna dämpa skadlig genaktivering och bromsa den genetiska diversifiering som ligger bakom resistens mot behandlingar som tamoxifen.
Citering: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Nyckelord: östrogenreceptor, APOBEC3B, R-loop, bröstcancer, DNA-skada