Clear Sky Science · de
R-Loop-Bearbeitung durch die DNA-Cytosin-Deaminase APOBEC3B moduliert die Aktivität von Östrogenrezeptor-Enhancern
Warum diese Forschung wichtig ist
Viele Brustkrebserkrankungen sind für ihr Wachstum auf das Hormon Östrogen angewiesen. Dieselben Signale, die lebenswichtige Gene anschalten, können auch DNA schädigen und damit Tumoren helfen, sich weiterzuentwickeln und Therapien zu widerstehen. Diese Studie entblößt, wie ein natürlich vorkommendes DNA‑Editierungsenzym, APOBEC3B, mit Östrogenrezeptoren an regulatorischen DNA‑Schaltern, den Enhancern, zusammenwirkt. Indem gezeigt wird, wo und wie dieses Enzym tätig ist, verknüpft die Arbeit die normale hormongetriebene Genregulation mit den Mutationen und Brüchen, die das Krebsgenom destabilisieren, und deutet neue Ansätze an, hormonabhängige Tumoren gezielt zu behandeln.
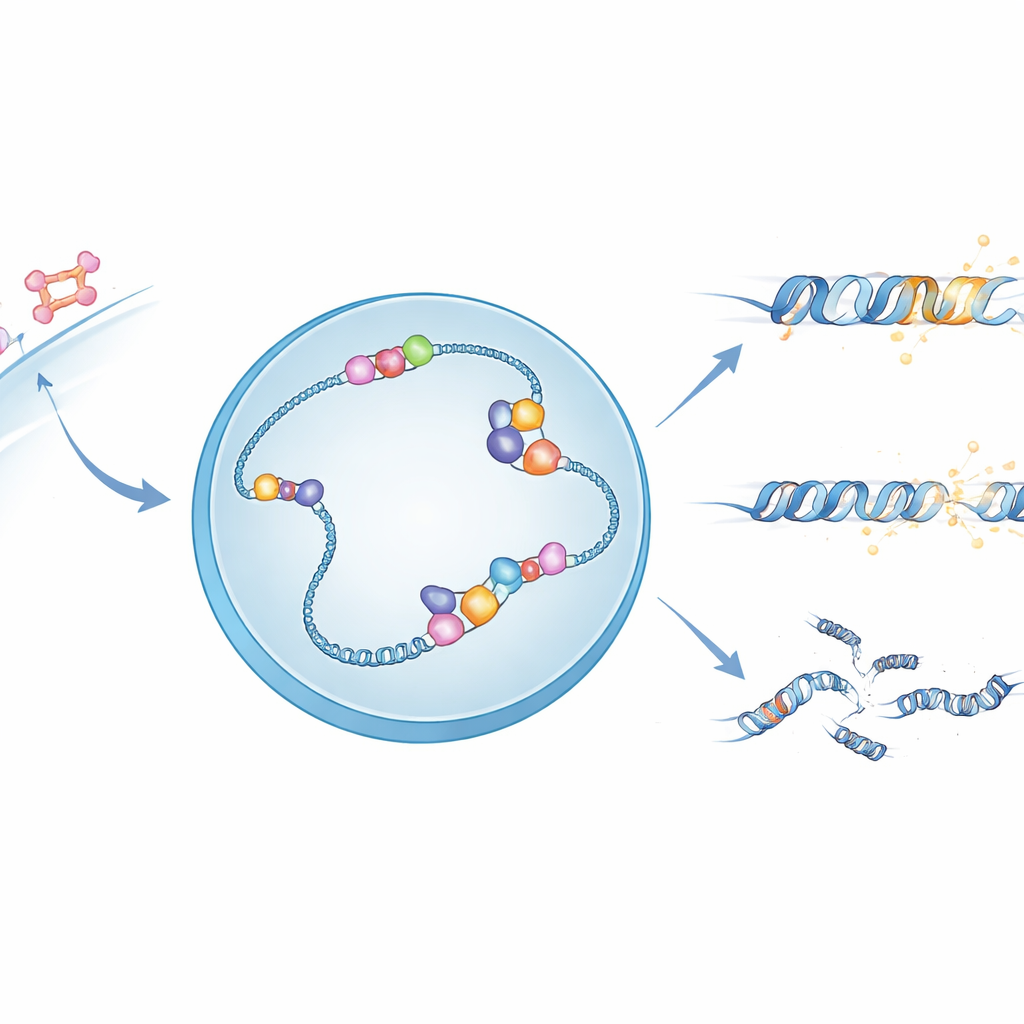
Hormonelle Signale und fragile DNA-Strukturen
Wenn Östrogen in eine Zelle eintritt, aktiviert es den Östrogenrezeptor, ein Protein, das in den Zellkern wandert und an spezifische DNA‑Stellen bindet, um benachbarte Gene zu steuern. An vielen dieser Stellen erzeugt das Ablesen der DNA in RNA ungewöhnliche dreisträngige Strukturen, sogenannte R‑Schleifen, bei denen die neu gebildete RNA an einen DNA‑Strang bindet und den anderen Strang freilegt. Diese R‑Schleifen können Genregulation unterstützen, machen die DNA aber auch fragiler und anfälliger für Brüche. Die Autoren vermuteten, dass APOBEC3B, ein Enzym, das bereits dafür bekannt ist, einzelsträngige DNA chemisch zu verändern, die freiliegende Strangstelle in R‑Schleifen als bevorzugte Angriffsstelle nutzt.
Kartierung, wo der DNA-Editor zuschlägt
Um APOBEC3Bs Fußabdruck im Genom sichtbar zu machen, erzeugte das Team Brustkrebszellen, in denen ein zentraler DNA‑Reparaturweg, die Basenexzisionsreparatur, blockiert war. Dadurch blieben chemische Modifikationen durch APOBEC3B lange genug bestehen, um mittels Ganzgenomsequenzierung erfasst zu werden. Sie fanden, dass die charakteristischen Mutationen dieses Enzyms nicht in protein‑kodierenden Regionen, sondern in regulatorischer DNA in der Nähe von Genanfängen und Enhancern gehäuft auftreten, besonders in Bereichen, die früh replizieren und hochaktiv sind. Diese editieren Stellen lagen tendenziell in Sequenzen mit einer Zusammensetzung, die R‑Schleifen begünstigt, was nahelegt, dass APOBEC3B eng mit diesen transienten DNA:RNA‑Strukturen verbunden ist.
Direkter Nachweis, dass APOBEC3B auf R‑Schleifen wirkt
Die Forschenden verwendeten dann zwei genomweite Verfahren, um APOBEC3B und R‑Schleifen in Aktion zu beobachten. Ein Ansatz zog DNA:RNA‑Hybride heraus, während ein anderer einzelsträngige DNA fing, die an markiertes APOBEC3B gebunden war. Zusammengenommen zeigten sie, dass das Enzym direkt innerhalb von R‑Schleifen sitzt und Cytosin‑Basen auf dem freiliegenden DNA‑Strang chemisch in Uracil umwandelt. Wenn ein Enzym, das R‑Schleifen auflöst (RNase H1), überexprimiert wurde, nahm die Bindung von APOBEC3B stark ab, was bestätigte, dass R‑Schleifen essentielle Andockplattformen sind. Nach kurzer Östrogenstimulation stiegen sowohl R‑Schleifen als auch APOBEC3B‑Bindung an Promotoren und insbesondere an aktiv transkribierten Enhancern, die vom Östrogenrezeptor genutzt werden, an und verband so Hormon‑Signalgebung mit Schüben R‑Schleifen‑abhängiger DNA‑Bearbeitung.
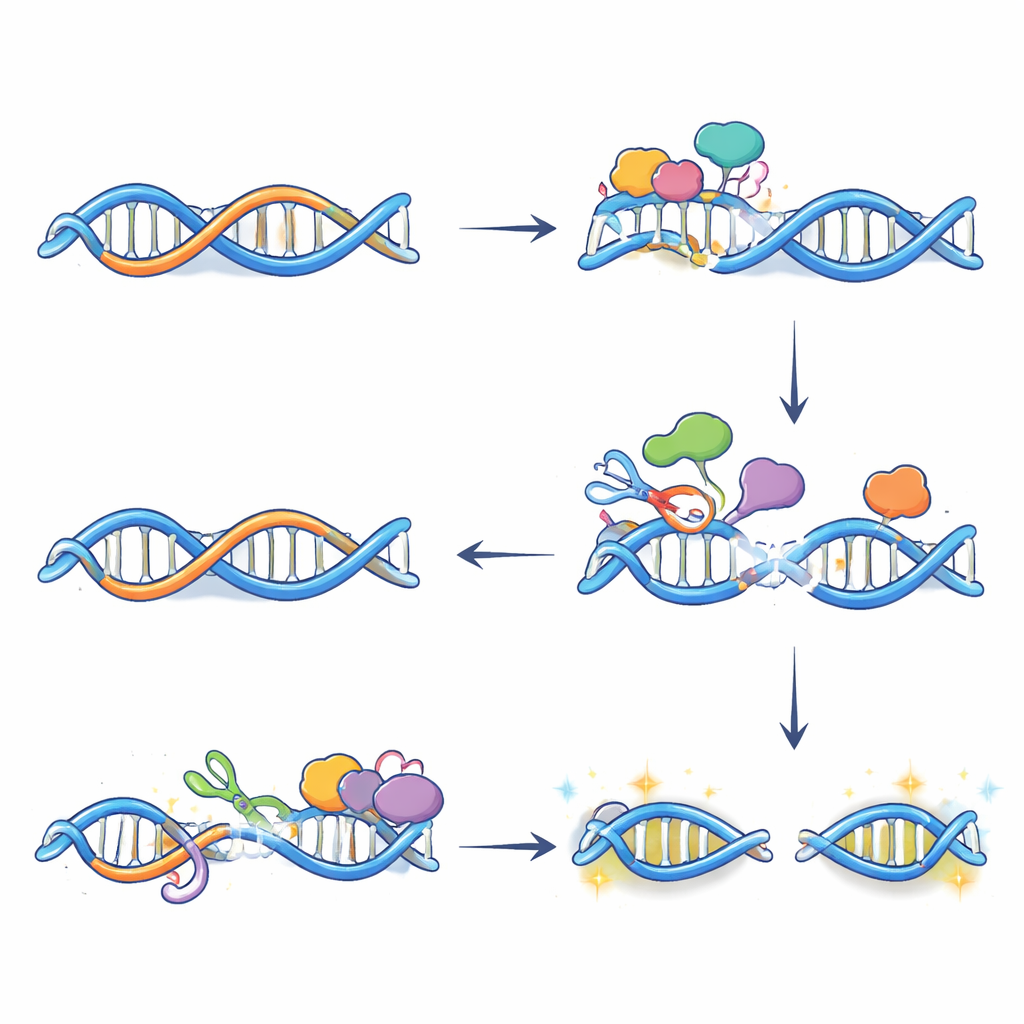
Von chemischen Editierungen zu DNA‑Brüchen und Genaktivierung
Allein die Editierung bricht die DNA nicht; der Schaden entsteht, wenn Reparatursysteme diese veränderten Basen verarbeiten. Mithilfe einer Technik, die die Enden gebrochener DNA markiert, zeigten die Autoren, dass viele Doppelstrangbrüche nach Östrogenbehandlung von APOBEC3B abhängen und genau dort auftreten, wo R‑Schleifen und das Enzym zusammenliegen. Weitere Experimente ergaben, dass zwei Reparaturwege — Basenexzisionsreparatur und transkriptionsgekoppelte Nukleotidexzisionsreparatur — an diesen Stellen zusammenwirken. Jeder führt Schnitte auf gegenüberliegenden DNA‑Strängen nahe der R‑Schleife ein; treffen diese Schnitte aufeinander, entsteht ein vollständiger Bruch. Die Hemmung entweder der APOBEC3B‑Aktivität oder der Reparaturschritte verringerte diese Brüche und dämpfte den üblichen Anstieg der Expression vieler östrogen‑responsiver Gene, was darauf hindeutet, dass kontrollierte DNA‑Schädigung tatsächlich dazu beiträgt, an wichtigen Enhancern einen offeneren, aktiveren Chromatin‑Zustand zu etablieren.
Was das für Krebs und Therapie bedeutet
Diese Arbeit zeichnet ein Bild von APOBEC3B als zweischneidiges Schwert beim hormongetriebenen Brustkrebs. Indem es die DNA an R‑Schleifen nahe Östrogenrezeptor‑Enhancern editiert, trägt es zur Entstehung temporärer DNA‑Brüche bei, die das Chromatin umgestalten und die Expression wachstumsfördernder Gene verstärken. Gleichzeitig hinterlassen diese Ereignisse Narben — Mutationen und strukturelle Veränderungen — die genomische Instabilität und Tumorentwicklung vorantreiben. Das Verständnis dieser Kopplung zwischen Hormon‑Signalgebung, R‑Schleifen‑Biologie und DNA‑Editierung macht APOBEC3B und die damit verbundenen Reparaturschritte zu potenziellen Wirkstoffzielen. Die Hemmung dieses Kreislaufs könnte schädliche Genaktivierung dämpfen und die genetische Diversifizierung verlangsamen, die der Resistenz gegenüber Therapien wie Tamoxifen zugrunde liegt.
Zitation: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Schlüsselwörter: Östrogenrezeptor, APOBEC3B, R-Schleifen, Brustkrebs, DNA-Schäden