Clear Sky Science · tr
DNA sitozin deaminazı APOBEC3B tarafından R-döngüsü düzenlemesi östrojen reseptör güçlendiricilerinin aktivitesini değiştirir
Bu araştırma neden önemli
Birçok meme kanseri büyümek için östrojen hormonu bağımlıdır. Hayati genleri açan aynı sinyaller aynı zamanda DNA’ya zarar vererek tümörlerin evrilmesine ve tedaviye direnç geliştirmesine yardım edebilir. Bu çalışma, doğal olarak bulunan bir DNA‑düzenleyici enzim olan APOBEC3B’nin, güçlendiriciler olarak adlandırılan düzenleyici DNA anahtarlarında östrojen reseptörleriyle nasıl işbirliği yaptığını ortaya koyuyor. Bu enzimin tam olarak nerede ve nasıl hareket ettiğini göstererek, normal hormon kaynaklı gen kontrolünü kanser genomunu istikrarsızlaştıran mutasyonlar ve kırılmalarla ilişkilendiriyor ve hormon‑bağımlı tümörleri hedeflemenin yeni yollarını öneriyor.
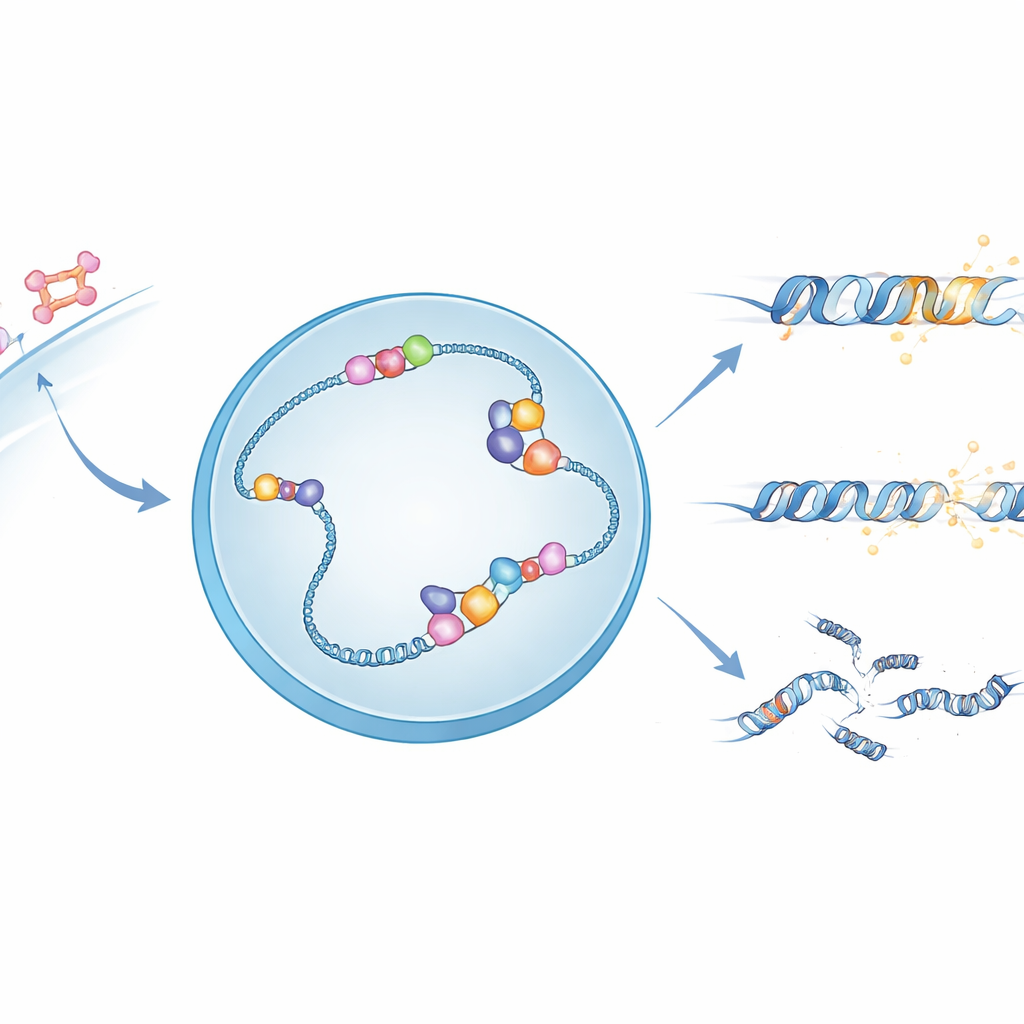
Hormon sinyalleri ve kırılgan DNA yapıları
Östrojen bir hücreye girdiğinde, östrojen reseptörünü aktive eder; bu protein çekirdeğe gidip yakındaki genleri kontrol etmek için belirli DNA bölgelerine bağlanır. Bu bölgelerin çoğunda, DNA’dan RNA’ya okuma işlemi R‑döngüleri adı verilen sıradışı üç iplikli yapılar oluşturur; burada yeni RNA, bir DNA ipliğine yapışır ve diğer iplik açığa çıkar. Bu R‑döngüleri genlerin düzenlenmesine yardımcı olabilir, ancak aynı zamanda DNA’yı daha kırılgan ve kırılmaya yatkın hale getirir. Yazarlar, zaten tek iplikli DNA’yı kimyasal olarak değiştirdiği bilinen APOBEC3B’nin, R‑döngülerde açığa çıkan ipliği tercih edilen çalışma yüzeyi olarak kullanıyor olabileceğinden şüpheleniyordu.
DNA düzenleyicinin vurduğu yerleri haritalamak
APOBEC3B’nin genom genelindeki ayak izini görmek için ekip, baz çıkarma onarımı adı verilen temel bir DNA onarım yolunu engelleyecek şekilde meme kanseri hücreleri tasarladı. Bu, APOBEC3B tarafından yapılan kimyasal düzeltmelerin yeterince uzun süre görünür kalmasını ve tüm genom dizilemesi ile yakalanmasını sağladı. Enzimin karakteristik mutasyonlarının protein kodlayan bölgelerde değil, gen başlama bölgeleri ve güçlendiriciler gibi düzenleyici DNA’da kümelendiğini; özellikle erken replike olan ve yüksek aktivite gösteren bölgelerde yoğunlaştığını buldular. Bu düzenlenmiş noktalar, R‑döngüsü oluşumunu destekleyen yapı taşlarına eğilimli dizilerde yer alma eğilimindeydi; bu da APOBEC3B’nin bu geçici DNA:RNA yapılarına sıkı bir şekilde bağlı olduğunu düşündürüyor.
APOBEC3B’nin R-döngüleri üzerinde çalıştığına dair doğrudan kanıt
Araştırmacılar daha sonra APOBEC3B ve R‑döngülerini eylem halinde izlemek için iki genom çapında assay kullandı. Bir yöntem DNA:RNA hibritlerini çekip aldı; diğeriyse etiketlenmiş APOBEC3B’nin bağlandığı tek DNA ipliklerini yakaladı. Birlikte, enzimin R‑döngülerinin tam içinde yer aldığını ve açığa çıkan DNA ipliğinde sitozin bazlarını urasil’e kimyasal olarak çevirdiğini gösterdiler. R‑döngülerini temizleyen bir enzim (RNase H1) fazla üretilince, APOBEC3B bağlanması keskin biçimde düştü; bu da R‑döngülerinin temel yerleşme platformları olduğunu doğruladı. Kısa sürelı östrojen uyarımıyla promotörlerde ve özellikle östrojen reseptörünün kullandığı aktif transkribe edilen güçlendiricilerde hem R‑döngüleri hem de APOBEC3B bağlanması artış gösterdi; bu da hormon sinyalini R‑döngüsü bağımlı DNA düzenlemelerinin patlamalarına bağlıyor.
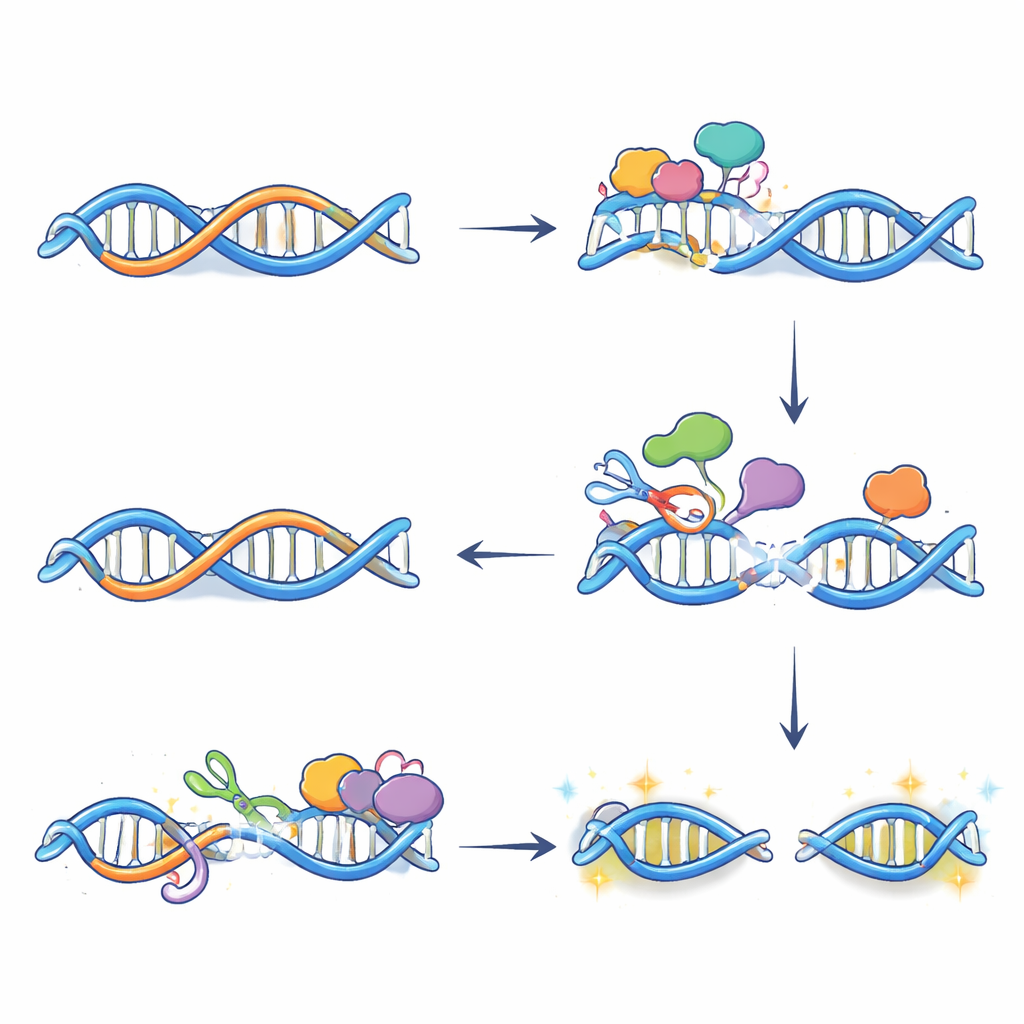
Kimyasal düzenlemelerden DNA kırılmalarına ve gen aktivasyonuna
Sadece düzenleme DNA’yı kırmaz; hasar, onarım sistemleri bu değiştirilmiş bazları işlediğinde ortaya çıkar. Kırık DNA uçlarını etiketleyen bir teknik kullanarak, yazarlar östrojen tedavisinden sonra görülen birçok çift iplikli kırığın APOBEC3B’ye bağlı olduğunu ve R‑döngüleri ile enzimin örtüştüğü tam yerlerde oluştuğunu gösterdi. Daha ileri deneyler, baz çıkarma onarımı ve transkripsiyona bağlı nükleotid çıkarma onarımının bu bölgelerde birlikte çalıştığını ortaya koydu. Her ikisi R‑döngüsünün yakınında karşıt DNA ipliklerinde kesikler oluşturuyor; kesikler karşılaştığında tam bir kırılma oluşuyor. Ya APOBEC3B’nin aktivitesi ya da onarım adımlarından herhangi biri engellenirse bu kırılmalar azaldı ve birçok östrojen‑yanıtlı genin normalde görülen ifade artışı kırıldı; bu, dikkatle kontrol edilen DNA hasarının anahtar güçlendiricilerde daha açık, aktif bir kromatin durumunun kurulmasına yardımcı olduğunu gösterir.
Bu, kanser ve tedavi açısından ne anlama geliyor
Bu çalışma APOBEC3B’yi hormonla tetiklenen meme kanserinde iki ucu keskin bir kılıç olarak çiziyor. Östrojen reseptör güçlendiricileri yakınındaki R‑döngülerde DNA’yı düzenleyerek, geçici DNA kırılmaları yaratarak kromatini yeniden şekillendiriyor ve büyümeyi destekleyen genlerin ifadesini artırıyor. Aynı zamanda bu olaylar izler bırakıyor—mutasyonlar ve yapısal değişiklikler—ki bunlar genomik istikrarsızlığı ve tümör evrimini besliyor. Hormon sinyallemesi, R‑döngü biyolojisi ve DNA düzenlemesi arasındaki bu bağlantının anlaşılması, APOBEC3B ve ilişkili onarım adımlarını potansiyel ilaç hedefleri olarak öne çıkarıyor. Bu devreyi inhibe etmek zararlı gen aktivasyonunu azaltabilir ve tamoksifen gibi tedavilere karşı direnç temelini oluşturan genetik çeşitlenmeyi yavaşlatabilir.
Atıf: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Anahtar kelimeler: östrojen reseptörü, APOBEC3B, R-döngüleri, meme kanseri, DNA hasarı