Clear Sky Science · ru
Редактирование R-циклов дезаминазой цитозина ДНК APOBEC3B модулирует активность энхансеров рецептора эстрогена
Почему это исследование важно
Многие опухоли молочной железы зависят от гормона эстрогена для роста. Те же сигналы, которые включают жизненно важные гены, могут также повреждать ДНК, помогая опухолям эволюционировать и становиться резистентными к лечению. В этом исследовании раскрывается, как естественная ферментная система редактирования ДНК — APOBEC3B — взаимодействует с рецепторами эстрогена на регуляторных ДНК-переключателях, называемых энхансерами. Показав точно, где и как действует этот фермент, работа связывает нормальное гормонозависимое регулирование генов с мутациями и разрывами, которые дестабилизируют геном рака, и намечает новые подходы к таргетированию гормонозависимых опухолей.
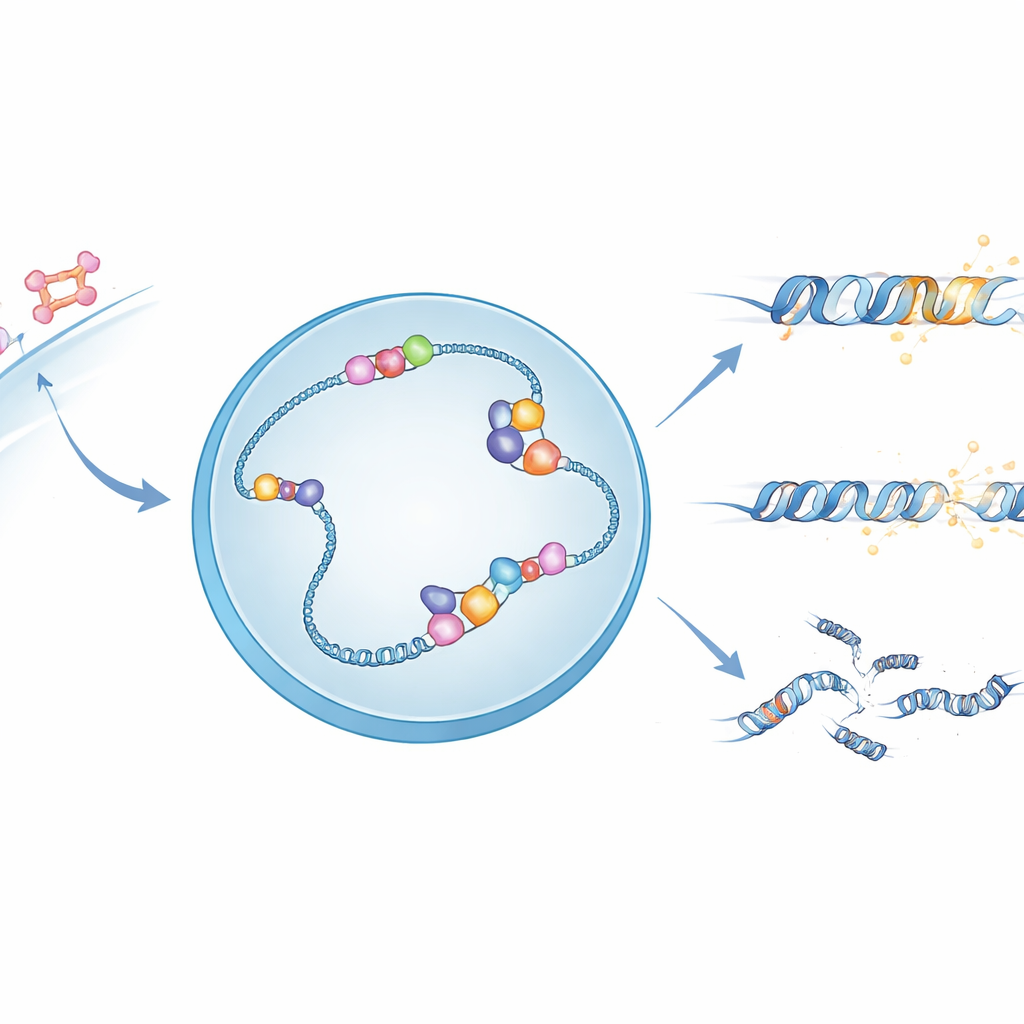
Гормональные сигналы и хрупкие структуры ДНК
Когда эстроген попадает в клетку, он активирует рецептор эстрогена — белок, который перемещается в ядро и связывается с определёнными участками ДНК для управления близлежащими генами. На многих из этих участков процесс транскрипции ДНК в РНК порождает необычные трёхцепочечные структуры, называемые R-циклы, где новая РНК комплементарно прилегает к одной цепи ДНК, оставляя другую цепь обнажённой. Эти R-циклы могут помогать в регуляции генов, но при этом делают ДНК более уязвимой к разрывам. Авторы предположили, что APOBEC3B — фермент, известный своей способностью химически модифицировать одноцепочечную ДНК — может использовать оголённую цепь в R-циклах как предпочтительную мишень.
Картирование мест атак редактора ДНК
Чтобы увидеть следы APOBEC3B по всему геному, команда создала клетки рака молочной железы, в которых был заблокирован ключевой путь восстановления оснований — базовый эксцизионный ремонт. Это позволило химическим изменениям, вносимым APOBEC3B, сохраняться достаточно долго, чтобы их зафиксировать при секвенировании всего генома. Они обнаружили, что характерные мутации этого фермента скапливаются не в белок-кодирующих областях, а в регуляторной ДНК рядом с участками старта транскрипции и энхансерами, особенно в зонах, которые реплицируются рано и являются высокоактивными. Эти изменённые участки склонялись к последовательностям, благоприятным для образования R-циклов, что указывает на тесную связь APOBEC3B с этими временными структурами ДНК:РНК.
Прямые доказательства того, что APOBEC3B действует на R‑циклах
Исследователи затем использовали два геномных метода, чтобы наблюдать APOBEC3B и R-циклы в действии. Один метод вытягивал гибриды ДНК:РНК, а другой захватывал одноцепочечные участки ДНК, связанные с меченым APOBEC3B. Вместе они показали, что фермент располагается прямо в R-циклах и химически конвертирует основания цитозина в урацил на обнажённой цепи ДНК. При сверхэкспрессии фермента, разрушающего R-циклы (RNase H1), связывание APOBEC3B резко падало, подтверждая, что R-циклы являются необходимыми точками привязки. При кратковременной стимуляции эстрогеном и R-циклы, и связывание APOBEC3B резко возрастали в промоторах и особенно в активно транскрибируемых энхансерах, используемых рецептором эстрогена, связывая гормональную сигнализацию с всплесками R-цикл-зависимого редактирования ДНК.
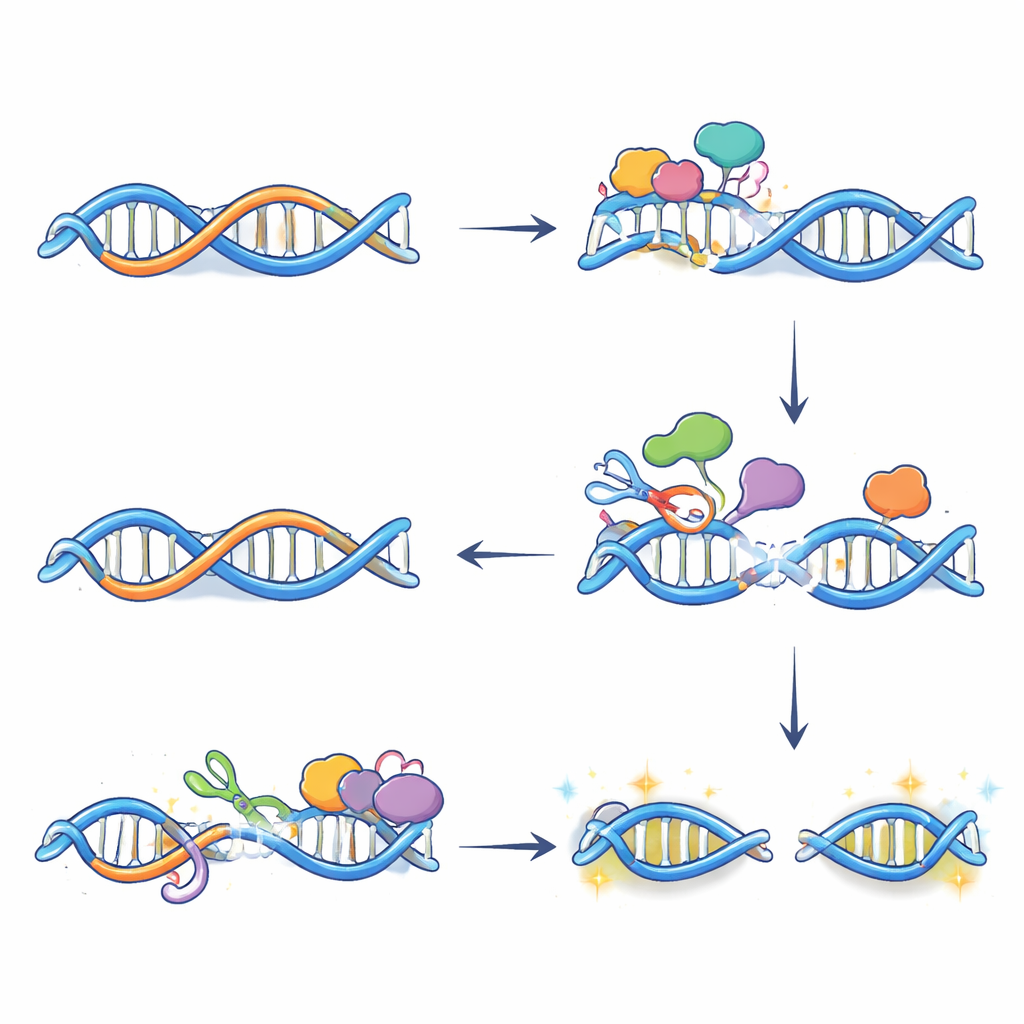
От химических правок к разрывам ДНК и активации генов
Само по себе редактирование не разрывает ДНК; повреждение возникает, когда системы ремонта обрабатывают эти изменённые основания. С применением метода маркировки концов разорванной ДНК авторы показали, что многие двуспиральные разрывы, возникающие после обработки эстрогеном, зависят от APOBEC3B и появляются точно там, где совпадают R-циклы и фермент. Дальнейшие эксперименты выявили, что два пути репарации — базовый эксцизионный ремонт и транскрипционно-сопряжённый нуклеотидный эксцизионный ремонт — действуют совместно в этих участках. Каждый вносит разрез на противоположной цепи ДНК рядом с R-циклом; когда разрезы встречаются, формируется полный разрыв. Блокирование либо активности APOBEC3B, либо шагов ремонта уменьшало число этих разрывов и ослабляло обычный всплеск экспрессии многих эстроген‑ответных генов, что указывает на то, что контролируемые повреждения ДНК фактически способствуют созданию более открытого, активного состояния хроматина в ключевых энхансерах.
Что это значит для рака и терапии
Эта работа рисует APOBEC3B как двуликий меч при гормонозависимом раке молочной железы. Редактируя ДНК в R-циклах рядом с энхансерами рецептора эстрогена, он способствует возникновению временных разрывов ДНК, которые перестраивают хроматин и усиливают экспрессию генов, стимулирующих рост. В то же время эти события оставляют шрамы — мутации и структурные изменения — которые подпитывают геномную нестабильность и эволюцию опухоли. Понимание этой связи между гормональной сигнализацией, биологией R-циклов и редактированием ДНК выделяет APOBEC3B и связанные с ним этапы репарации как потенциальные мишени для лекарств. Инактивация этого контура может ослабить вредную активацию генов и замедлить генетическую диверсификацию, лежащую в основе резистентности к таким препаратам, как тамоксифен.
Цитирование: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
Ключевые слова: рецептор эстрогена, APOBEC3B, R-циклы, рак молочной железы, повреждение ДНК