Clear Sky Science · ar
تحرير R-loop بواسطة ديأميناز السيتوزين في الحمض النووي APOBEC3B يغير نشاط محفزات مستقبل الإستروجين
لماذا يهم هذا البحث
تعتمد العديد من سرطانات الثدي على هرمون الإستروجين للنمو. الإشارات نفسها التي تشغل جينات حيوية يمكن أن تلحق أيضًا ضررًا بالحمض النووي، مما يساعد الأورام على التطور ومقاومة العلاج. يكشف هذا البحث كيف يعمل إنزيم تحرير الحمض النووي الطبيعي APOBEC3B بالتعاون مع مستقبلات الإستروجين عند مفاتيح تنظيمية في الحمض النووي تُسمى المحفزات. من خلال توضيح أماكن عمل هذا الإنزيم وطريقته بدقة، يربط العمل بين التحكم الطبيعي في الجينات المدفوع بالهرمونات والطفرات والانقطاعات التي تزعزع استقرار جينوم السرطان، ويقترح طرقًا جديدة لاستهداف الأورام المعتمدة على الهرمونات.
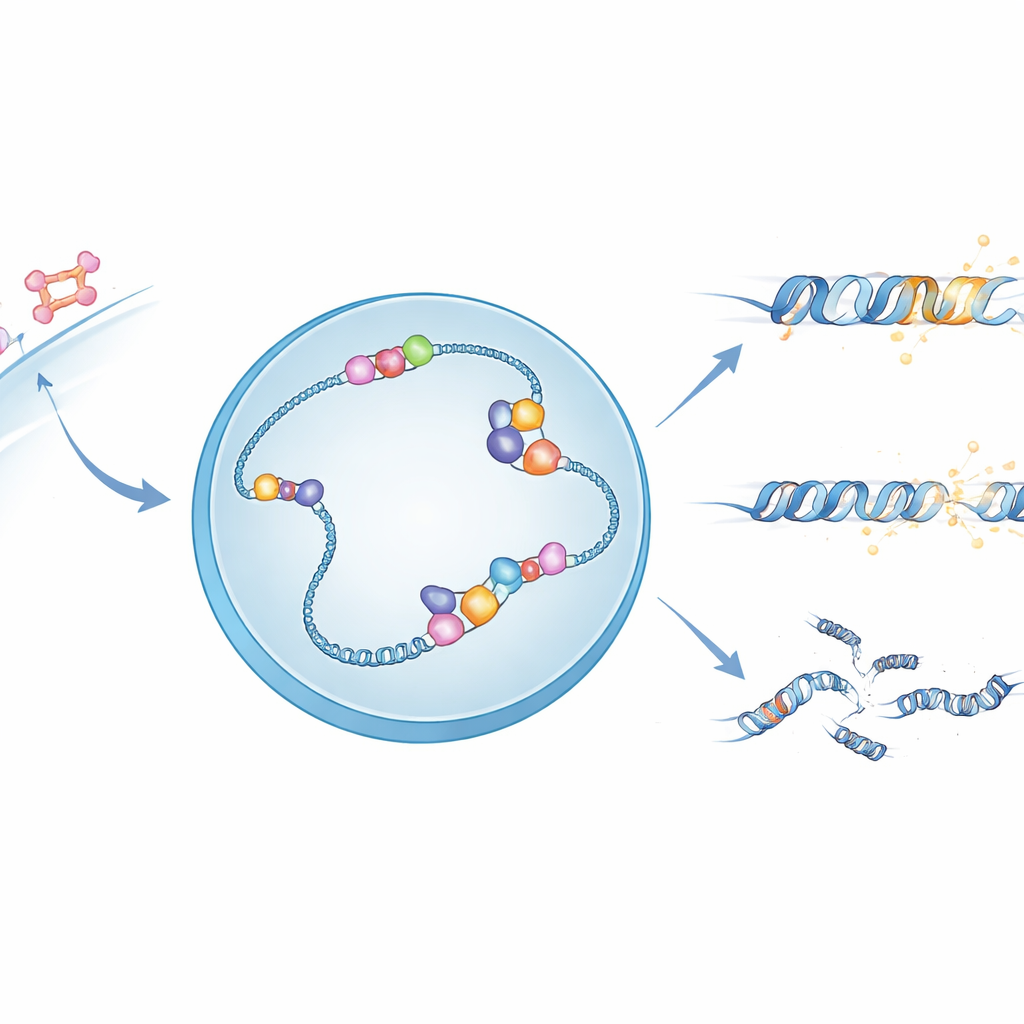
إشارات هرمونية وهياكل حمض نووي هشة
عند دخول الإستروجين إلى الخلية، يُفعّل مستقبل الإستروجين، وهو بروتين ينتقل إلى النواة ويرتبط بمواقع محددة في الحمض النووي للتحكم في الجينات القريبة. عند العديد من هذه المواقع، تؤدي عملية نسخ الحمض النووي إلى الحمض النووي الريبي إلى تكوين هياكل غير عادية ثلاثية الخيوط تُسمى R-loops، حيث يلتصق الحمض النووي الريبي الجديد بأحد شطري الحمض النووي ويترك الشطر الآخر مكشوفًا. يمكن أن تساعد هذه الـ R-loops في تنظيم الجينات، لكنها تجعل الحمض النووي أيضًا أكثر هشاشة وعرضة للكسر. اشتبه المؤلفون في أن APOBEC3B، وهو إنزيم معروف بتعديل السلاسل الأحادية للحمض النووي كيميائيًا، قد يستخدم الشطر المكشوف في R-loops كسطح عمل مفضل له.
رسم خريطة أماكن هجوم محرر الحمض النووي
لمعرفة بصمة APOBEC3B عبر الجينوم، صمّم الفريق خلايا سرطان ثدي تعطل فيها مسار إصلاح حمض نووي رئيسي، وهو إصلاح القواعد بآلية الإزالة والاستبدال. هذا جعل التعديلات الكيميائية التي يجريها APOBEC3B تظهر مدة كافية لتُلتقط بواسطة تسلسل الجينوم الكامل. وجدوا أن الطفرات المميزة التي يسببها هذا الإنزيم تتجمع ليس في مناطق ترميز البروتين، بل في الحمض النووي التنظيمي قرب مواقع بدء الجينات والمحفزات، خاصة في مناطق تتكرر مبكرًا وتكون نشطة بكثافة. كانت هذه البقع المعدلة تميل إلى التوضع في تسلسلات غنية بالوحدات التي تُفضّل تكوّن R-loops، مما يوحي بارتباط وثيق بين APOBEC3B وهذه الهياكل المؤقتة للحمض النووي:الحمض النووي الريبي.
دليل مباشر أن APOBEC3B يعمل على R-loops
استخدم الباحثون بعد ذلك تجربتين على مستوى الجينوم لمراقبة APOBEC3B وR-loops أثناء العمل. جذبت إحدى الطريقتين الهجينات الحمض النووي:الحمض النووي الريبي، بينما التقطت الأخرى الشُّظُف الأحادية للحمض النووي المرتبطة بـ APOBEC3B الموسوم. أظهرت النتائج معًا أن الإنزيم يتموضع داخل R-loops ويحوّل كيميائيًا قواعد السيتوزين إلى يوراسيل على الشطر المكشوف من الحمض النووي. عند الإفراط في إنتاج إنزيم يزيل R-loops (RNase H1)، انخفض ارتباط APOBEC3B بشكل حاد، مما يؤكد أن R-loops هي منصات ترسيب أساسية. عقب تحفيز قصير بالإستروجين، ازداد كل من R-loops وارتباط APOBEC3B عند المحفزات وبخاصة عند المحفزات المكثفة النَّشاط التي تستخدمها مستقبلات الإستروجين، رابطًا الإشارة الهرمونية بانفجارات من تحرير الحمض النووي المعتمد على R-loop.
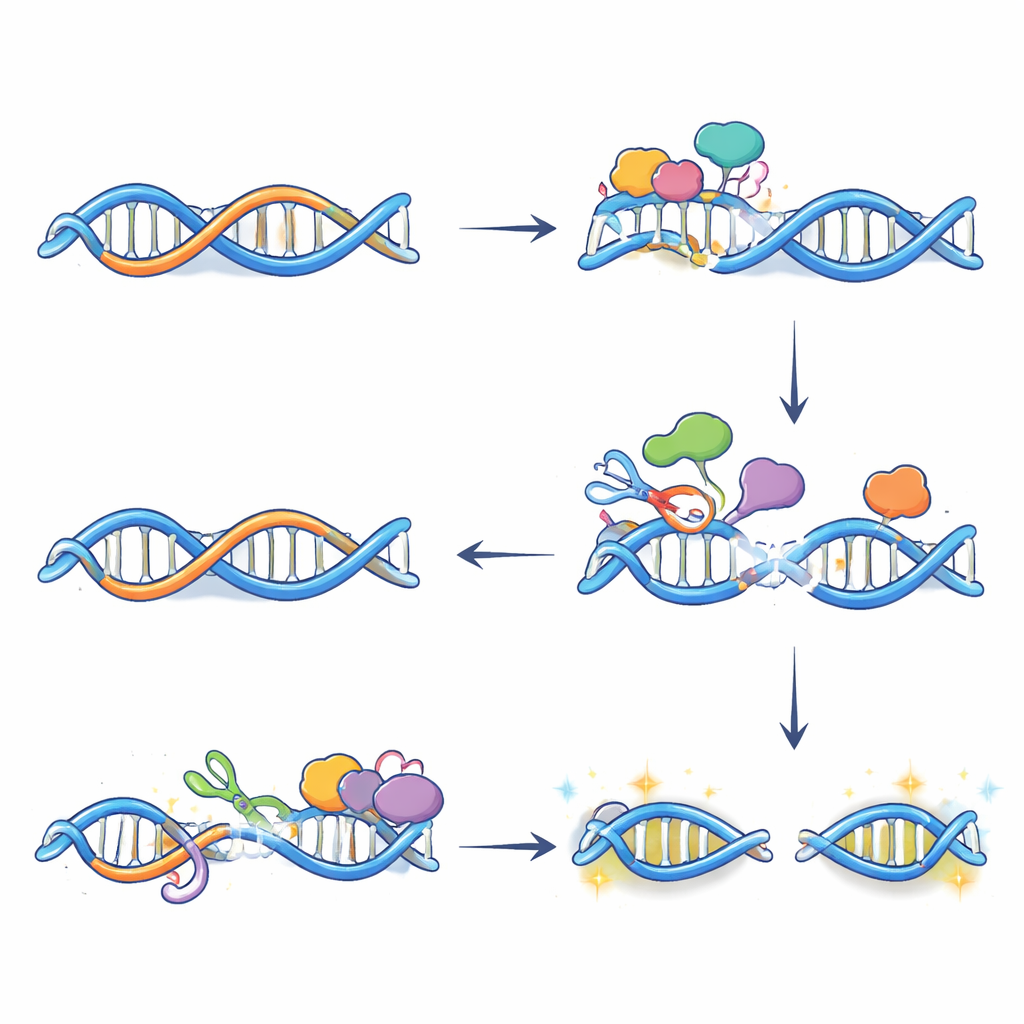
من التعديلات الكيميائية إلى كسور الحمض النووي وتفعيل الجينات
لا يؤدي التحرير بمفرده إلى كسر الحمض النووي؛ التنكس يحدث عندما تعالج أنظمة الإصلاح هذه القواعد المعدلة. باستخدام تقنية تضع علامة على نهايات الحمض النووي المكسور، أظهر المؤلفون أن العديد من كسور السلاسل المزدوجة التي تظهر بعد معالجة بالإستروجين تعتمد على APOBEC3B وتحدث تمامًا حيث تتزامن R-loops والإنزيم. كشفت تجارب إضافية أن مسارين للإصلاح—إصلاح القواعد عبر الإزالة والاستبدال وإصلاح نكليوتيدات مرتبط بالنسخ—يعملان معًا في هذه المواقع. يقوم كل منهما بإحداث قصات على شطرين متقابلين من الحمض النووي قرب الـ R-loop؛ وعندما تلتقي هذه القصات يتكوّن كسر كامل. أدت إعاقة نشاط APOBEC3B أو خطوات الإصلاح إلى تقليل هذه الكسور وتخفيف الزيادة الطبيعية في تعبير العديد من الجينات المستجيبة للإستروجين، مما يشير إلى أن الضرر المدروس بعناية للحمض النووي يساعد بالفعل على إرساء حالة كروماتين أكثر انفتاحًا ونشاطًا عند المحفزات الرئيسية.
ماذا يعني هذا للسرطان والعلاج
يصوّر هذا العمل APOBEC3B كرمح ذو حدين في سرطان الثدي المعتمد على الهرمونات. عن طريق تحرير الحمض النووي عند R-loops قرب محفزات مستقبل الإستروجين، يساعد على خلق كسور مؤقتة تعيد تشكيل الكروماتين وتزيد تعبير الجينات المحفزة للنمو. وفي الوقت نفسه، تترك هذه الأحداث ندوبًا—طفرات وتغيرات تركيبية—تغذي عدم استقرار الجينوم وتطور الورم. إن فهم هذا الارتباط بين الإشارة الهرمونية، بيولوجيا R-loop والتحرير الكيميائي للحمض النووي يبرز APOBEC3B وخطوات الإصلاح المصاحبة له كأهداف دوائية محتملة. قد يؤدي تثبيط هذا المسار إلى كبح التفعيل الجيني الضار وإبطاء التنوع الجيني الذي يقوم عليه تطور مقاومة علاجات مثل تاموكسيفين.
الاستشهاد: Zhang, C., Lu, Yj., Chen, B. et al. R-loop editing by DNA cytosine deaminase APOBEC3B modulates the activity of oestrogen receptor enhancers. Nat Commun 17, 2887 (2026). https://doi.org/10.1038/s41467-026-69679-4
الكلمات المفتاحية: مستقبل الإستروجين, APOBEC3B, R-loops, سرطان الثدي, ضرر الحمض النووي