Clear Sky Science · zh
膜蛋白的时空组织控制细菌的细胞外电子传递
细菌如何在细胞外输送电流
一些细菌可以字面意义上“呼吸”矿物或电极而非氧气,通过将微小的电荷从细胞内移动到细胞外或反向移动来生存。这种电学技巧支持它们在缺氧环境中的存活,并为微生物燃料电池和用于污染处理的生物反应器等技术提供动力。本文研究提出了一个看似简单的问题:在微生物细胞内,关键蛋白如何在空间和时间上组织自身,才使得这种远距离的电子流能够顺利进行?
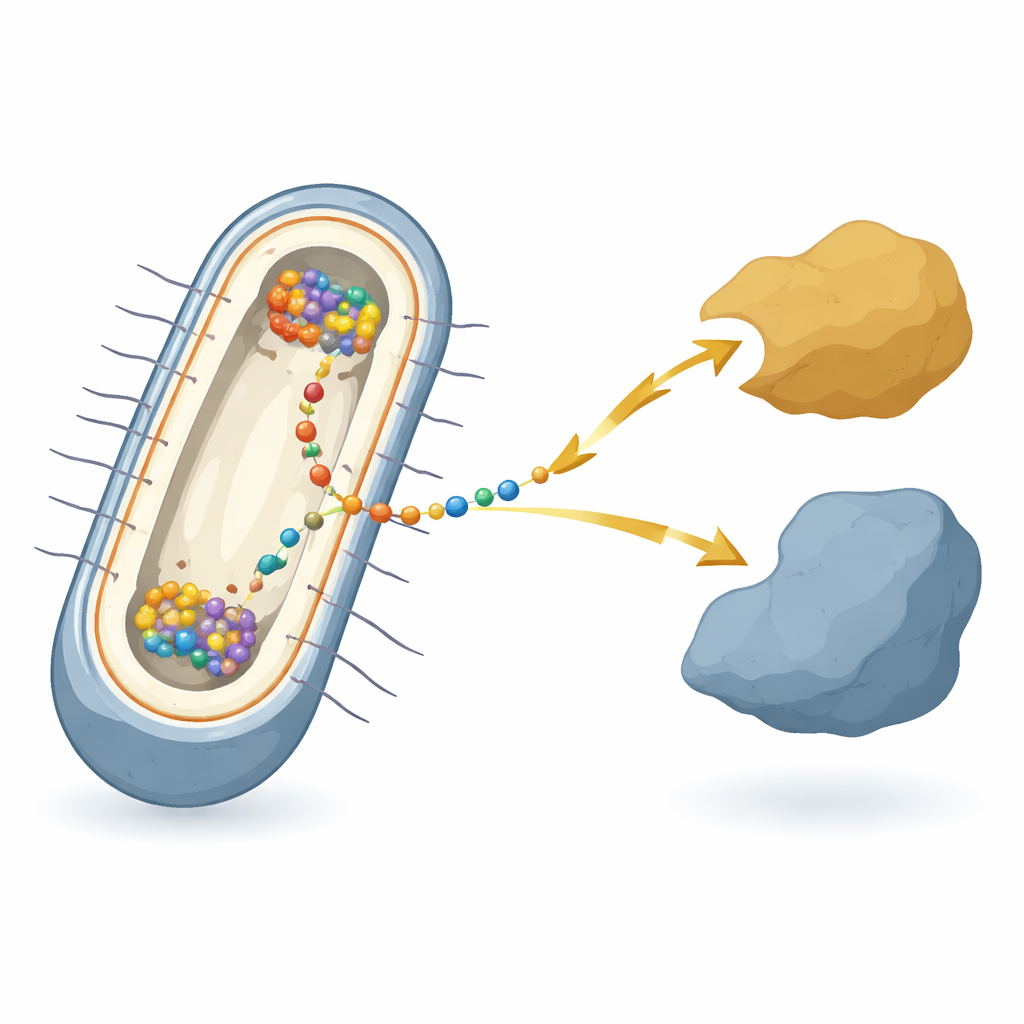
以铁锈和金属为食的微生物
研究聚焦于细菌Shewanella oneidensis,这是一种著名的模型物种,以其“细胞外电子传递”能力闻名——能够向细胞外的金属、矿物或电极交付或从中接收电子。在这些细菌中,电子必须穿过两层膜及其间的空隙,经过由多种不同蛋白组成的中继链。在这条中继的中心,位于内膜处,有一个名为CymA的枢纽蛋白。CymA一方面与细胞内部代谢对话,另一方面与膜间空间的穿梭蛋白交换电子。尽管对各个部件已有数十年的研究,但在细菌实际进行电呼吸时,这些组分在活细胞内如何协同组织仍不清楚。
蛋白自组装成明亮的点状簇
研究者使用可跟踪单个蛋白的先进荧光显微镜,将CymA标记为发光探针,并在不同生长条件下观察其行为。当细菌在有氧环境生长时,CymA处于闲置状态,蛋白均匀分布在内膜上。但当细胞在无氧条件下被迫依赖细胞外电子传递时,CymA出人意料地聚集成明显的明亮点或“斑点”,常见于细胞极端附近。无论电子是向外输送到矿物还是从金属或电极进入细胞,这种重组都会发生。重要的是,CymA的总量并未显著改变;变化的是它的空间分布。
动态簇促进更强的电子流
通过对大量细胞随时间的观察,团队发现任一时刻只有部分细胞形成CymA簇,且形成时间各有差异。然而在单个细胞中,一旦开始从均匀分布转变为斑点,这一过程出乎意料地迅速,表明在可变的延迟之后发生了突发性的内部重组。为检验这些斑点是否真的影响电性能,研究者将光激活电极与显微镜结合,测量单个细胞产生的极微小光电流。形成CymA斑点的细胞比未形成斑点的细胞表现出明显更强的电极电子摄取能力,即便两类细胞的CymA含量相当。这表明促成高效细胞外电子传递的关键是蛋白的聚集,而非单纯的蛋白丰度。
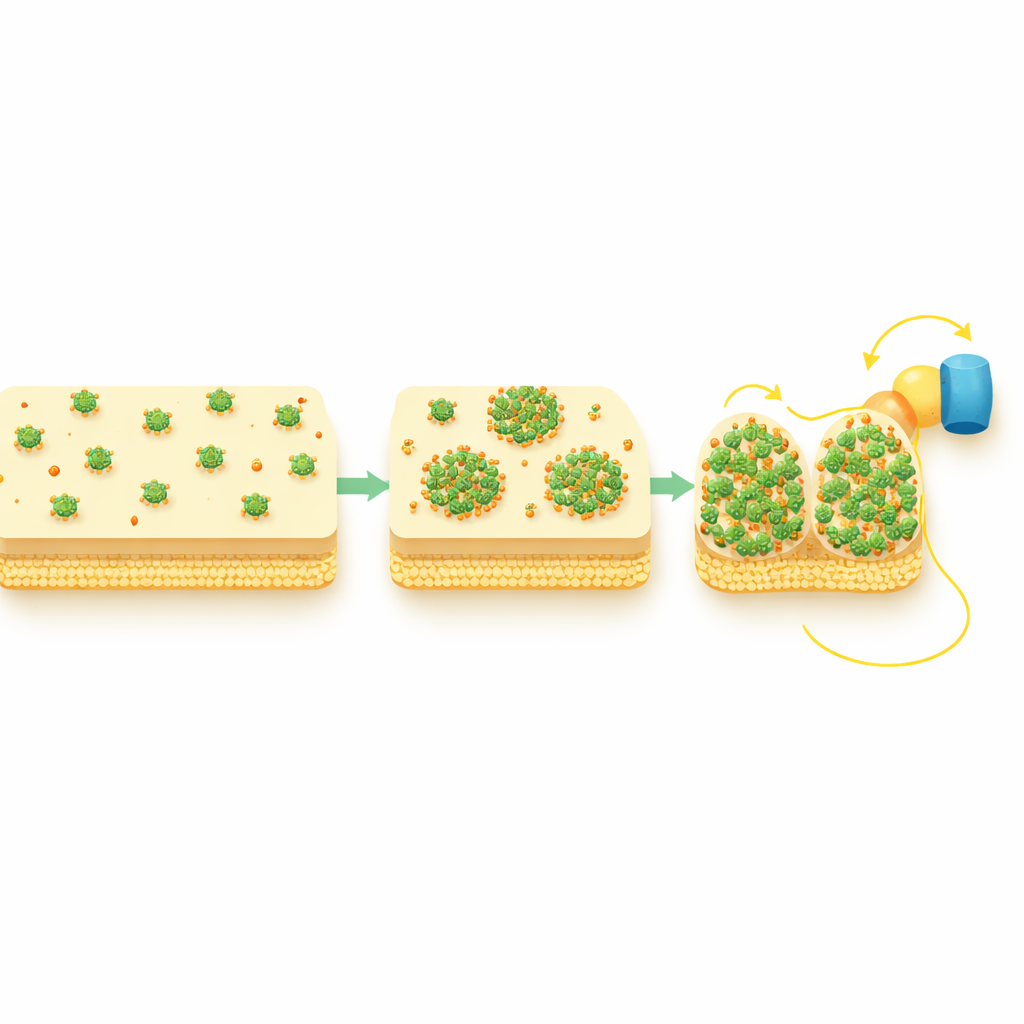
在细胞包膜上构建更短的通路
研究还跟踪了两种周质(periplasmic)穿梭蛋白STC和FccA,这些蛋白直接与CymA交换电子,并将电子传递到外膜方向。在富氧条件下,这些穿梭蛋白呈均匀分布;但在活跃的细胞外电子传递过程中,它们也呈现斑点状,并在空间上与CymA簇重叠。遗传学测试显示是CymA先发生重组,然后吸引这些伙伴蛋白,而不是相反。换言之,CymA斑点作为枢纽,将下游穿梭蛋白聚拢成紧凑的高流量节点,有效缩短并强化了从细胞内部到表面的电子通路。
由膜化学驱动的类液体凝聚体
通过追踪单个CymA分子,研究者发现斑点内的蛋白仍保持流动性,能够进出簇体,且簇体本身可随生长条件出现或消散。这些特征是“生物分子凝聚体”的标志——由蛋白及其他分子集合形成的类液滴,而非刚性复合体或损伤性聚集体。对一种称为甲萘醌(menaquinone)的小型膜分子的测量显示,其水平随着CymA斑点的出现而上升。作者提出,膜上富集甲萘醌的区域充当支架,招募CymA进入类似凝聚体的域,尤其是在细胞极端附近。
这对自然和技术意味着什么
总体而言,该研究表明Shewanella控制细胞外电子传递不仅依赖于其合成哪些蛋白,还取决于这些蛋白何时何地聚集成动态簇。由局部膜化学组织的CymA凝聚体吸引伙伴蛋白,形成暂时的“电热点”,从而增强电子穿过细胞包膜的流动。对普通读者来说,这意味着即便是细菌也在使用一种自组装的电路,按需重排内部部件以连接岩石、金属或电极。理解并最终控制这种蛋白自组织方式,可能帮助科学家设计更高效的微生物燃料电池、更有效的生物电化学工厂,以及用于清理金属和污染物的新策略。
引用: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
关键词: 细胞外电子传递, 谢瓦内拉 (Shewanella), 细菌生物电, 生物分子凝聚体, 微生物燃料电池