Clear Sky Science · nl
Ruimtelijke en temporele organisatie van membraaneiwitten regelt bacteriële extracellulaire elektronenoverdracht
Hoe bacteriën elektriciteit buiten hun cellen verplaatsen
Sommige bacteriën kunnen letterlijk mineralen of elektroden ‘ademen’ in plaats van zuurstof, waarbij ze kleine elektrische ladingen in en uit hun cellen verplaatsen. Deze elektrische truc voedt hun overleving in zuurstofarme omgevingen en drijft technologieën zoals microbiële brandstofcellen en bioreactoren die verontreiniging opruimen. De hier beschreven studie stelt een ogenschijnlijk eenvoudige vraag: hoe rangschikken de sleuteleiwitten in een microbiele cel zich in ruimte en tijd zodat dit langafstandselektronenverkeer daadwerkelijk werkt?
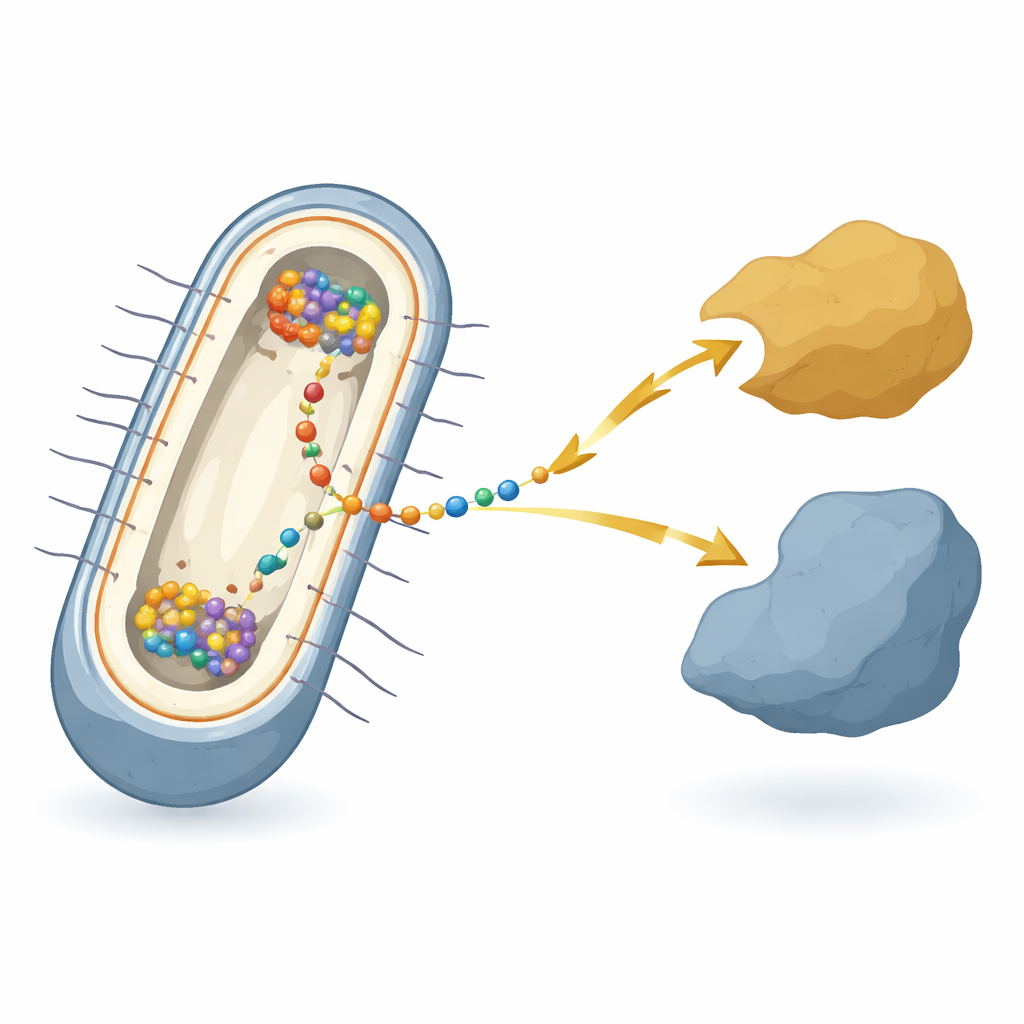
Een microbe die op roest en draden leeft
Het werk richt zich op de bacterie Shewanella oneidensis, een modelsoort die bekendstaat om “extracellulaire elektronenoverdracht” — het afgeven van elektronen aan of opnemen van elektronen van metalen, mineralen of elektroden buiten de cel. In deze bacteriën moeten elektronen twee membranen en de ruimte ertussen overbruggen, door een relais van veel verschillende eiwitten. In het hart van dit relais, in het binnenmembraan, bevindt zich een hub-eiwit genaamd CymA. CymA communiceert aan de ene kant met de interne stofwisseling van de cel en aan de andere kant met shuttle-eiwitten in de periplasmatische ruimte. Ondanks decennia onderzoek naar de afzonderlijke onderdelen was het niet duidelijk hoe al deze componenten in elke levende cel coördineren wanneer de bacterie deze elektrische ademhaling daadwerkelijk uitvoert.
Eiwitten organiseren zichzelf in heldere puntsgewijze clusters
Met behulp van geavanceerde fluorescentiemicroscopie die individuele eiwitten in individuele cellen kan volgen, markeerden de onderzoekers CymA met lichtgevende labels en keken naar het gedrag onder verschillende groeicondities. Wanneer de bacteriën met zuurstof groeiden — een toestand waarin CymA rust — verspreidde het eiwit zich gelijkmatig rond het binnenmembraan. Maar wanneer de cellen gedwongen werden te vertrouwen op extracellulaire elektronenoverdracht onder zuurstofvrije omstandigheden, verzamelde CymA zich onverwacht in duidelijke heldere plekken, of “puncta”, vaak in de buurt van de celpolen. Deze reorganisatie trad op ongeacht of elektronen uit de cel naar mineralen stroomden of de cel in werden gevoerd vanaf ijzer of elektroden. Belangrijk is dat de totale hoeveelheid CymA niet veel veranderde; wat veranderde was de ruimtelijke ordening.
Dynamische clusters versterken de elektronenstroom
Door veel cellen in de tijd te volgen, vonden de onderzoekers dat slechts een fractie van de cellen op een gegeven moment CymA-clusters vormde, en dat het tijdstip per cel varieerde. In individuele cellen verliep de overgang van een uniforme verdeling naar puncta echter opvallend snel zodra die begon, wat duidt op een plotselinge interne reorganisatie na een variabele vertraging. Om te testen of deze puncta daadwerkelijk van belang zijn voor de elektrische prestaties, combineerden de onderzoekers lichtgestuurde elektroden met microscopie en maten ze minieme photocurrents van individuele cellen. Cellen die CymA-puncta hadden gevormd, toonden aanzienlijk sterkere elektrische opname van de elektrode dan cellen zonder puncta, hoewel beide typen vergelijkbare hoeveelheden CymA bevatten. Dit wijst erop dat clustering, niet louter eiwitabundantie, efficiënte extracellulaire elektronenoverdracht mogelijk maakt.
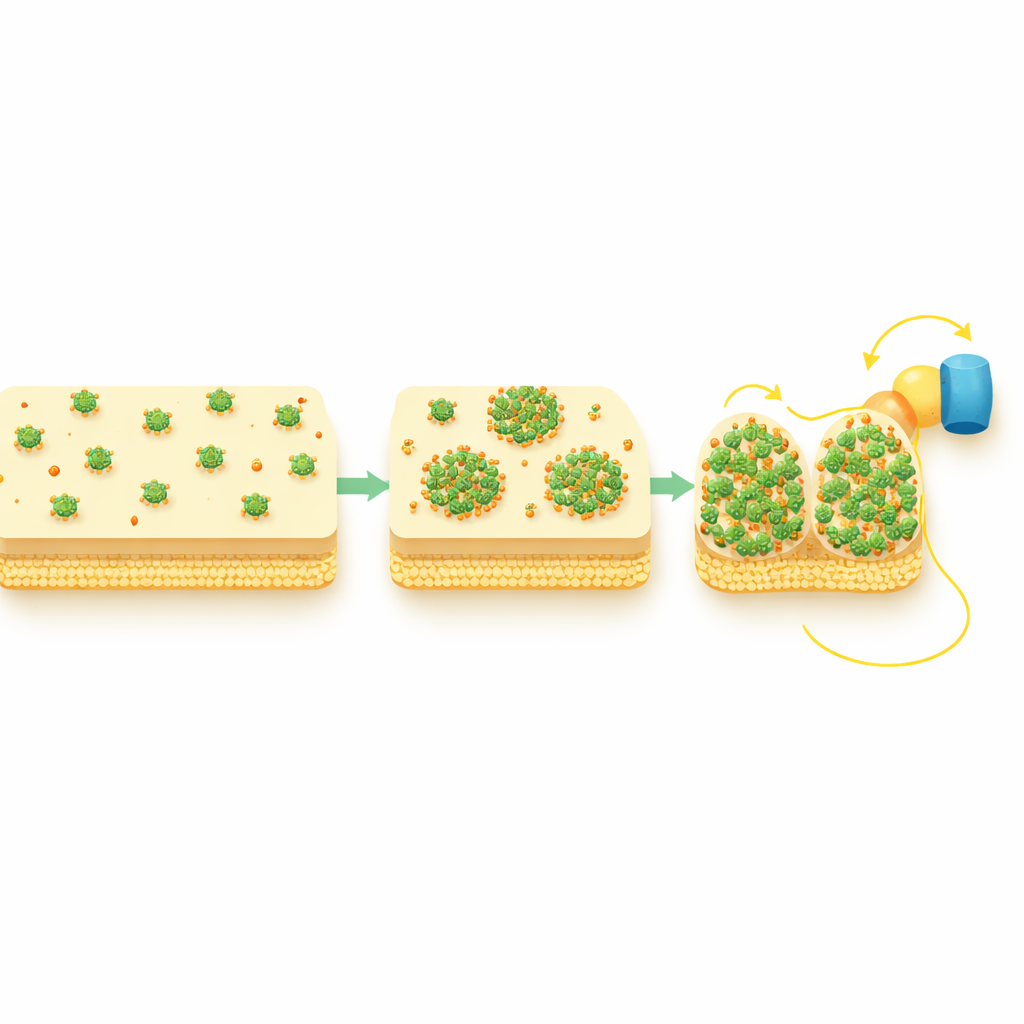
Kortere routes bouwen door het cellemembraan
De studie volgde ook twee periplasmatische shuttle-eiwitten, STC en FccA, die rechtstreeks elektronen met CymA uitwisselen en deze doorgeven richting het buitenmembraan. Onder zuurstofrijke omstandigheden waren deze shuttles gelijkmatig verspreid, maar tijdens actieve extracellulaire elektronenoverdracht namen zij eveneens een punctaat patroon aan en overlappen zij ruimtelijk met CymA-clusters. Genetische proeven toonden aan dat CymA zich eerst reorganiseert en daarna deze partners aantrekt, niet andersom. Met andere woorden: de CymA-puncta functioneren als hubs die de downstream shuttles bijeenbrengen in compacte, drukbezochte knooppunten, waarmee de elektronendoorgang van het celinterieur naar het oppervlak effectief wordt verkort en versterkt.
Vloeistofachtige condensaten aangedreven door membraanchemie
Door individuele CymA-moleculen te volgen ontdekten de onderzoekers dat eiwitten binnen puncta mobiel bleven en in en uit clusters konden bewegen, en dat de clusters zelf konden verschijnen en verdwijnen afhankelijk van de groeicondities. Dit zijn kenmerken van “biomoleculaire condensaten”, vloeistofachtige druppels gevormd door verzamelingen van eiwitten en andere moleculen in plaats van stijve complexen of beschadigde aggregaten. Metingen van een klein membraanmolecuul genaamd menaquinon, dat elektronen vervoert binnen het binnenmembraan, toonden aan dat de niveaus ervan stijgen in samenhang met het verschijnen van CymA-puncta. De auteurs stellen voor dat regio’s van het membraan die verrijkt zijn in menaquinon fungeren als scaffolden die CymA in condensaatachtige domeinen rekruteren, vooral nabij de celpolen.
Waarom dit belangrijk is voor natuur en technologie
Alles bij elkaar laat de studie zien dat Shewanella niet alleen afhankelijk is van welke eiwitten het produceert om extracellulaire elektronenoverdracht te regelen; het hangt ook af van wanneer en waar deze eiwitten zich verzamelen in dynamische clusters. CymA-condensaten, waarschijnlijk georganiseerd door lokale membraanchemie, trekken partnereiwitten aan om tijdelijke “elektrische hot spots” te vormen die de doorgang van elektronen door het cellemembraan versterken. Voor de geïnteresseerde lezer betekent dit dat zelfs bacteriën een soort zelfgeregeld schakelsysteem gebruiken, waarbij ze hun interne onderdelen op verzoek herschikken om contact te maken met gesteentes, metalen of elektroden. Het begrijpen en uiteindelijk sturen van dit soort eiwitzelforganisatie kan onderzoekers helpen bij het ontwerpen van betere microbiële brandstofcellen, efficiëntere bio-elektrochemische fabrieken en nieuwe strategieën voor het opruimen van metalen en verontreinigende stoffen.
Bronvermelding: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Trefwoorden: extracellulaire elektronenoverdracht, Shewanella, bacteriële bio-elektriciteit, biomoleculaire condensaten, microbiële brandstofcellen