Clear Sky Science · de
Räumlich-zeitliche Organisation eines Membranproteins steuert bakterielle extrazelluläre Elektronenübertragung
Wie Bakterien Elektrizität außerhalb ihrer Zellen bewegen
Manche Bakterien können buchstäblich Mineralien oder Elektroden anstelle von Sauerstoff „atmen“ und dabei winzige elektrische Ladungen in ihre Zellen hinein- oder aus ihnen herausbewegen. Dieser elektrische Trick sichert ihr Überleben in sauerstoffarmen Umgebungen und treibt Technologien wie mikrobielle Brennstoffzellen und Bioreaktoren zur Schadstoffbeseitigung an. Die hier beschriebene Studie stellt eine auf den ersten Blick einfache Frage: Wie ordnen sich die zentralen Proteine einer mikrobellen Zelle räumlich und zeitlich so an, dass dieser langreichweitige Elektronenfluss tatsächlich funktioniert?
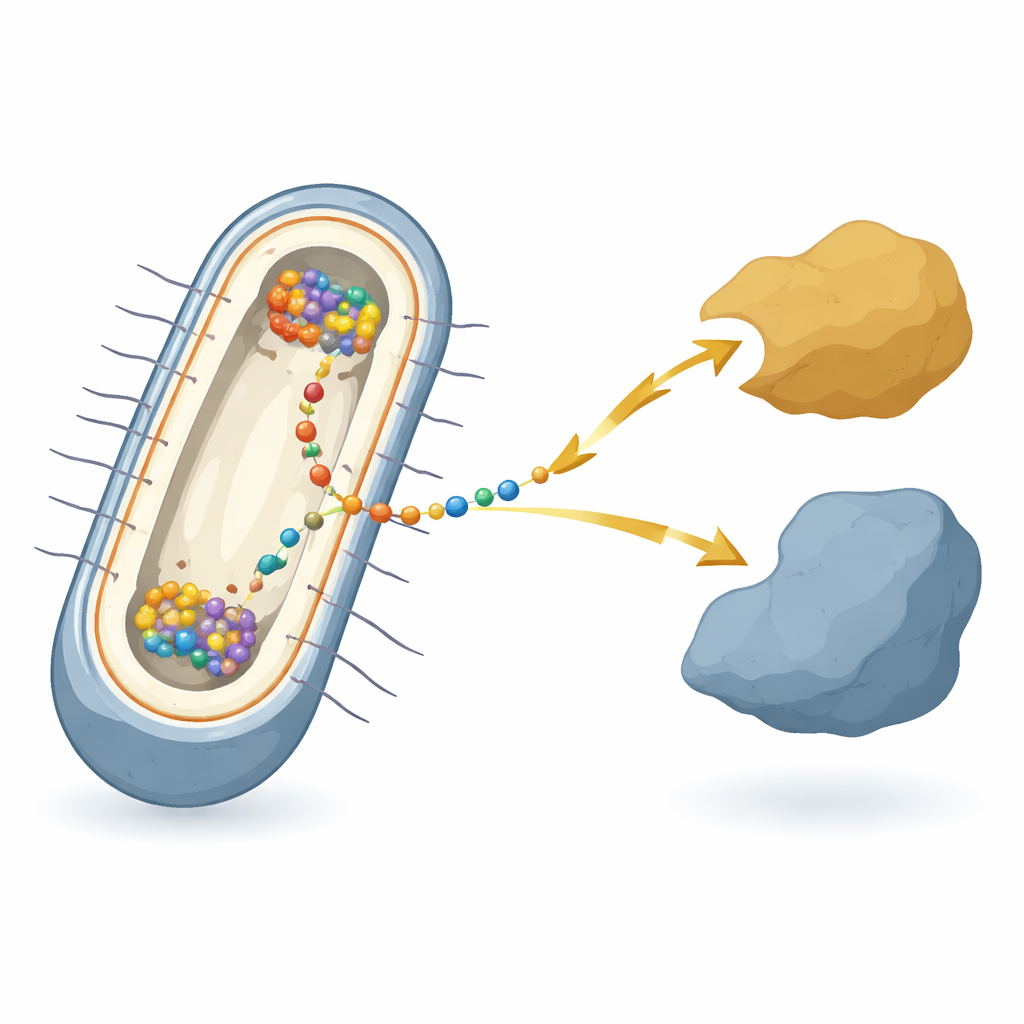
Ein Mikroorganismus, der von Rost und Drähten lebt
Die Arbeit konzentriert sich auf das Bakterium Shewanella oneidensis, eine Modellart, die für ihre „extrazelluläre Elektronenübertragung“ bekannt ist — das Übergeben von Elektronen an oder von Metallen, Mineralien oder Elektroden außerhalb der Zelle. Bei diesen Bakterien müssen Elektronen zwei Membranen und den dazwischenliegenden Raum überwinden und passieren dabei eine Kette verschiedener Proteine. Im Zentrum dieser Kette, in der inneren Membran, sitzt ein Hub-Protein namens CymA. CymA kommuniziert einerseits mit dem inneren Stoffwechsel der Zelle und andererseits mit Shuttle-Proteinen im Periplasma. Trotz jahrzehntelanger Untersuchungen der Einzelkomponenten war lange unklar, wie all diese Bestandteile in lebenden Zellen koordiniert sind, wenn das Bakterium tatsächlich diese elektrische Atmung durchführt.
Proteine organisieren sich zu hellen Punkten
Mithilfe fortschrittlicher Fluoreszenzmikroskopie, die einzelne Proteine in einzelnen Zellen verfolgen kann, markierten die Forscher CymA mit Leuchtmarkern und beobachteten sein Verhalten unter verschiedenen Wachstumsbedingungen. Wenn die Bakterien mit Sauerstoff wuchsen, einem Zustand, in dem CymA inaktiv ist, verteilte sich das Protein gleichmäßig in der inneren Membran. Sobald die Zellen jedoch unter sauerstofffreien Bedingungen auf extrazelluläre Elektronenübertragung angewiesen waren, sammelte sich CymA überraschend in deutlichen hellen Punkten oder „Punkta“, oft in der Nähe der Zellpole. Diese Umorganisation trat sowohl auf, wenn Elektronen aus der Zelle an Mineralien abgegeben wurden, als auch wenn Elektronen von Metall-Eisen oder Elektroden in die Zelle flossen. Wichtig ist, dass die Gesamtmenge an CymA kaum variierte; verändert hatte sich seine räumliche Anordnung.
Dynamische Cluster ermöglichen stärkeren Elektronenfluss
Bei der Beobachtung vieler Zellen über die Zeit fanden die Forscher, dass zu jedem Zeitpunkt nur ein Bruchteil der Zellen CymA-Cluster bildete und dass das Timing von Zelle zu Zelle variierte. In einzelnen Zellen war der Übergang von einer gleichmäßigen Verteilung zu Punkta jedoch überraschend schnell, sobald er eingesetzt hatte, was auf eine plötzliche interne Umorganisation nach einer variablen Verzögerungszeit hindeutet. Um zu prüfen, ob diese Punkta tatsächlich die elektrische Leistung beeinflussen, kombinierten die Forscher lichtaktivierte Elektroden mit Mikroskopie und maßen winzige Photoströme einzelner Zellen. Zellen mit CymA-Punkta zeigten eine deutlich stärkere Elektronenaufnahme von der Elektrode als solche ohne Punkta, obwohl beide Zelltypen ähnliche CymA-Mengen enthielten. Das deutet darauf hin, dass Clustering — nicht bloße Proteinmenge — die effiziente extrazelluläre Elektronenübertragung ermöglicht.
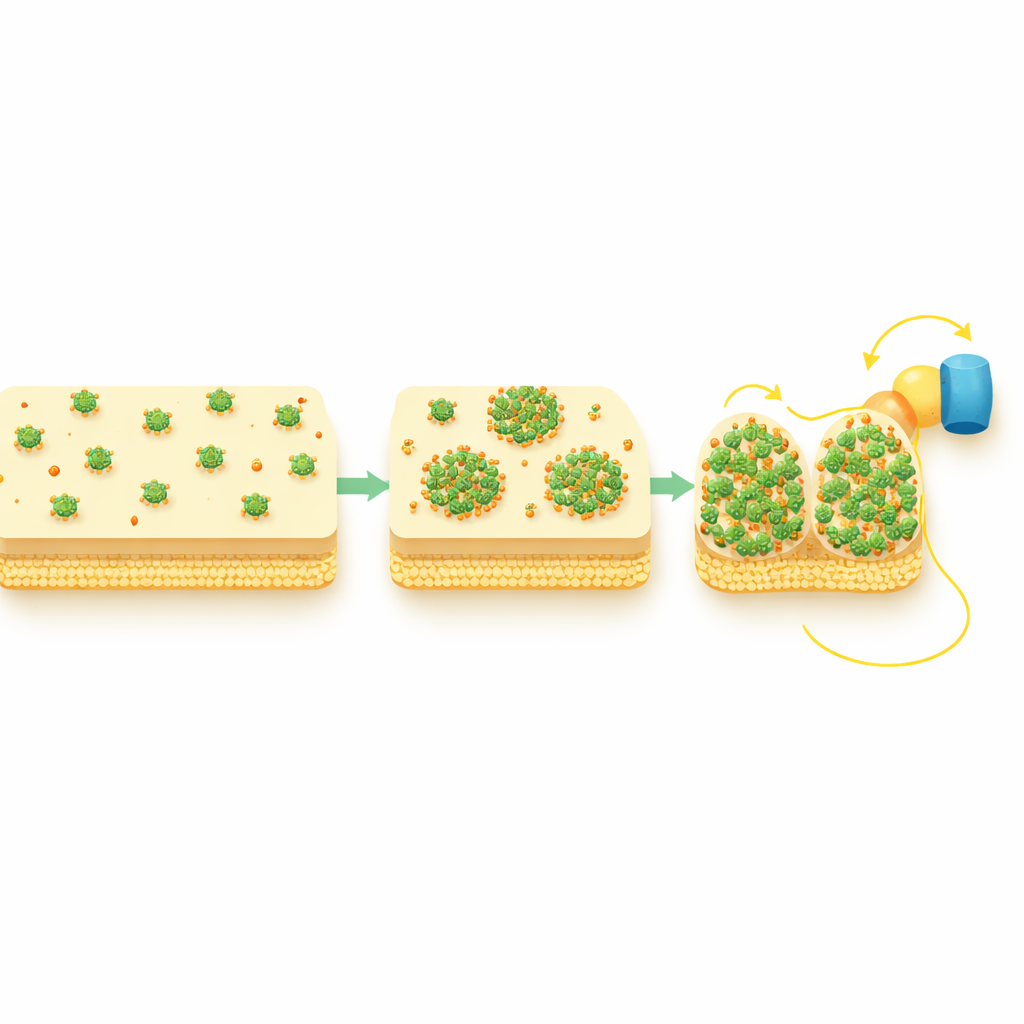
Kürzere Wege durch die Zellhülle bauen
Die Studie verfolgte außerdem zwei periplasmatische Shuttle-Proteine, STC und FccA, die direkt Elektronen mit CymA austauschen und sie weiter zur äußeren Membran leiten. Unter sauerstoffreichen Bedingungen waren diese Shuttles gleichmäßig verteilt, während sie bei aktiver extrazellulärer Elektronenübertragung ebenfalls punktförmige Muster annahmen und räumlich mit CymA-Clustern überlappten. Genetische Tests zeigten, dass sich CymA zuerst reorganisiert und dann diese Partner anzieht, nicht umgekehrt. Mit anderen Worten wirken die CymA-Punkta als Hubs, die die nachgeschalteten Shuttles in kompakte, stark frequentierte Knoten zusammenziehen und dadurch den Elektronenweg vom Zellinneren zur Oberfläche effektiv verkürzen und verstärken.
Flüssigartige Kondensate, angetrieben durch Membranchemie
Durch die Verfolgung einzelner CymA-Moleküle entdeckten die Forscher, dass Proteine innerhalb der Punkta mobil blieben und hinein- und herauswandern konnten und dass die Cluster selbst je nach Wachstumsbedingungen erscheinen und verschwinden konnten. Das sind Kennzeichen von „biomolekularen Kondensaten“ — flüssigartigen Tröpfchen, die sich aus Ansammlungen von Proteinen und anderen Molekülen bilden, im Gegensatz zu starren Komplexen oder beschädigten Aggregaten. Messungen eines kleinen Membranmoleküls namens Menaquinon, das Elektronen innerhalb der inneren Membran transportiert, zeigten, dass sein Gehalt parallel zum Auftreten der CymA-Punkta anstieg. Die Autoren schlagen vor, dass Membranregionen, die in Menaquinon angereichert sind, als Gerüst fungieren und CymA in kondensatähnliche Bereiche rekrutieren, besonders in Zellpolnähe.
Warum das für Natur und Technik wichtig ist
Insgesamt zeigt die Studie, dass Shewanella sich nicht allein darauf verlässt, welche Proteine sie herstellt, um die extrazelluläre Elektronenübertragung zu steuern; entscheidend ist auch, wann und wo diese Proteine zu dynamischen Clustern zusammenkommen. CymA-Kondensate, wahrscheinlich durch lokale Membranchemie organisiert, ziehen Partnerproteine an, um temporäre „elektrische Hotspots“ zu bilden, die den Elektronenfluss über die Zellhülle verstärken. Für eine allgemein verständliche Leserschaft bedeutet das: Selbst Bakterien nutzen eine Art selbstaufgebauter Verschaltung, indem sie ihre inneren Komponenten bei Bedarf umordnen, um sich an Gesteine, Metalle oder Elektroden anzuschließen. Das Verständnis und die gezielte Steuerung dieser Protein-Selbstorganisation könnte Forschern helfen, bessere mikrobielle Brennstoffzellen zu entwickeln, effizientere bioelektrochemische Fabriken zu bauen und neue Strategien zur Reinigung von Metall- und Schadstoffkontaminationen zu entwerfen.
Zitation: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Schlüsselwörter: extrazelluläre Elektronenübertragung, Shewanella, bakterielle Bioelektrizität, biomolekulare Kondensate, mikrobielle Brennstoffzellen