Clear Sky Science · tr
Hücre zarı proteinlerinin uzaysal ve zamansal düzeni bakteriyel hücre dışı elektron transferini kontrol ediyor
Bakteriler Elektriği Hücre Dışına Nasıl Taşır?
Bazı bakteriler gerçekten oksijen yerine mineralleri veya elektrotları “nefes alır” gibi kullanır; hücrelerine küçük elektrik yükleri alıp verirler. Bu elektriksel hile, oksijenden yoksun ortamlarda hayatta kalmalarını sağlar ve mikrobiyal yakıt hücreleri ile kirlilik temizleyen biyoreaktörler gibi teknolojileri çalıştırır. Burada anlatılan çalışma, görünüşte basit bir soruyu soruyor: bir mikrob hücresindeki kilit proteinler, uzun mesafeli elektron akışının gerçekten işlemesi için kendilerini uzayda ve zamanda nasıl düzenler?
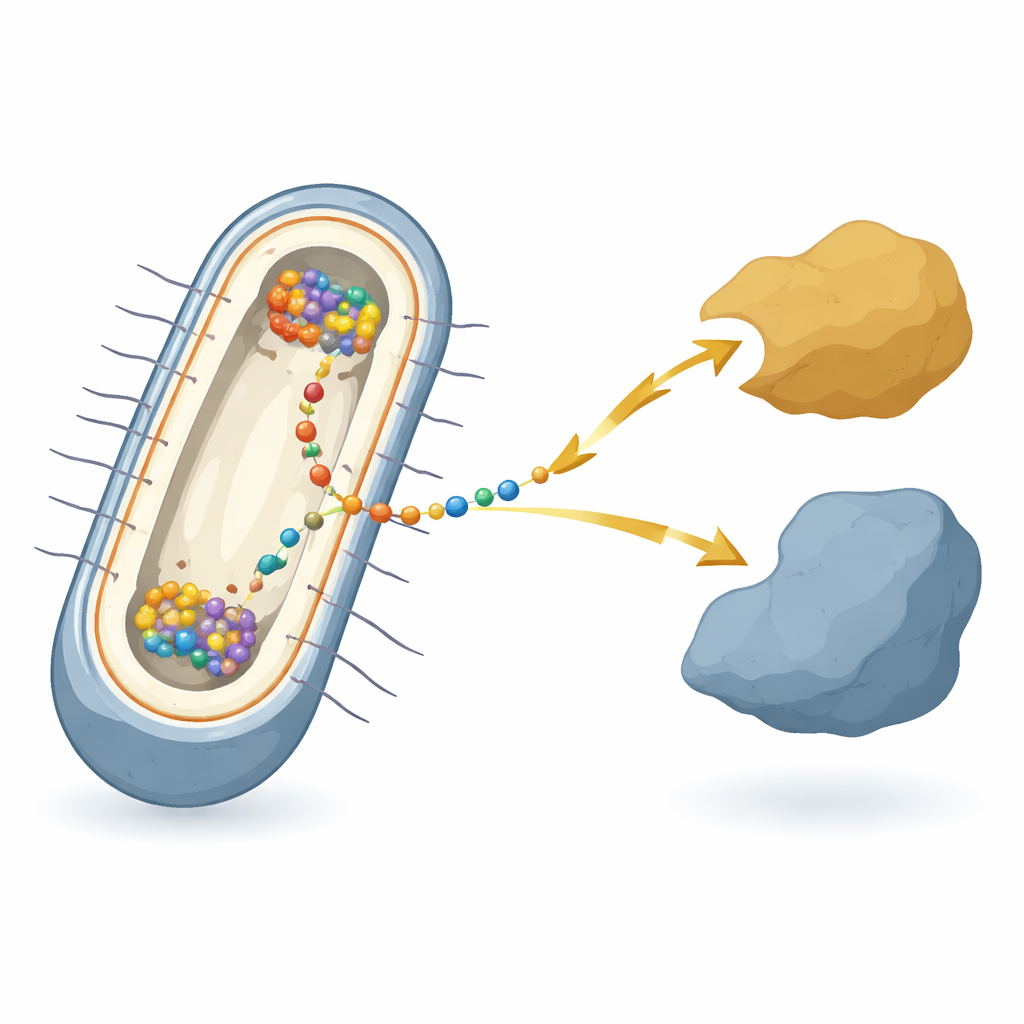
Pasa ve Teller Üzerinde Yaşayan Bir Mikrop
Çalışma, "hücre dışı elektron transferi" ile ünlü model bakteri Shewanella oneidensis üzerine odaklanıyor — elektronları hücre dışındaki metallere, minerallere veya elektrotlara verip alan bir tür. Bu bakterilerde elektronlar iki zarı ve aralarındaki boşluğu geçmeli, birçok farklı proteinin oluşturduğu bir röle üzerinden aktarılmalıdır. Bu rölenin merkezinde, iç zarında, CymA adlı bir merkezi protein bulunur. CymA bir tarafta hücrenin iç metabolizmasıyla, diğer tarafta zarlar arasındaki bölgede bulunan taşıyıcı proteinlerle konuşur. Bireysel bileşenler üzerine on yıllık çalışmalar olmasına rağmen, bakteri gerçekten bu elektriksel solunumu gerçekleştirdiğinde tüm bu bileşenlerin her yaşayan hücre içinde nasıl koordine edildiği açık değildi.
Proteinler Kendiliğinden Parlak Noktalar Oluşturuyor
Tek proteinleri tek hücrede izleyebilen ileri düzey floresan mikroskopisi kullanarak araştırmacılar CymA’yı parlayan işaretlerle etiketleyip farklı büyüme koşullarında davranışını gözlemlediler. Bakteriler oksijenle büyüdüğünde, CymA’nın atıl olduğu durumda, protein iç zarda eşit şekilde yayılıyordu. Ancak hücreler oksijensiz koşullarda hücre dışı elektron transferine zorlandığında, CymA beklenmedik şekilde genellikle hücre kutuplarına yakın belirgin parlak noktalar veya “puncta” halinde toplandı. Bu yeniden düzenlenme, elektronlar hücreden minerallere doğru akarken veya metal demir ya da elektrottan hücre içine akarken de gerçekleşti. Önemli olarak, toplam CymA miktarı çok değişmedi; değişen şey onun uzaysal düzenlenişiydi.
Dinamik Kümeler Daha Güçlü Elektron Akışı Sağlıyor
Birçok hücreyi zaman içinde izleyen ekip, herhangi bir anda sadece bir kısmının CymA kümeleri oluşturduğunu ve zamanlamanın hücreden hücreye değiştiğini buldu. Ancak tek tek hücrelerde, homojen dağılımdan punctalara geçiş başladıktan sonra şaşırtıcı derecede hızlıydı; bu da değişken bir gecikmenin ardından ani bir iç reorganizasyon olduğunu düşündürüyor. Bu punctaların gerçekten elektriksel performans için önemli olup olmadığını test etmek için araştırmacılar ışıkla aktive edilen elektrotları mikroskopiyle birleştirip tek hücrelerden çok küçük fotokurtakımlar ölçtüler. CymA punctaları oluşturmuş hücreler, puncta olmayan hücrelere göre elektrottan daha güçlü elektron alımı gösterdi; her iki tipte de benzer miktarda CymA olmasına rağmen. Bu, verimli hücre dışı elektron transferini sağlayanın protein bolluğu değil kümelenme olduğunu gösteriyor.
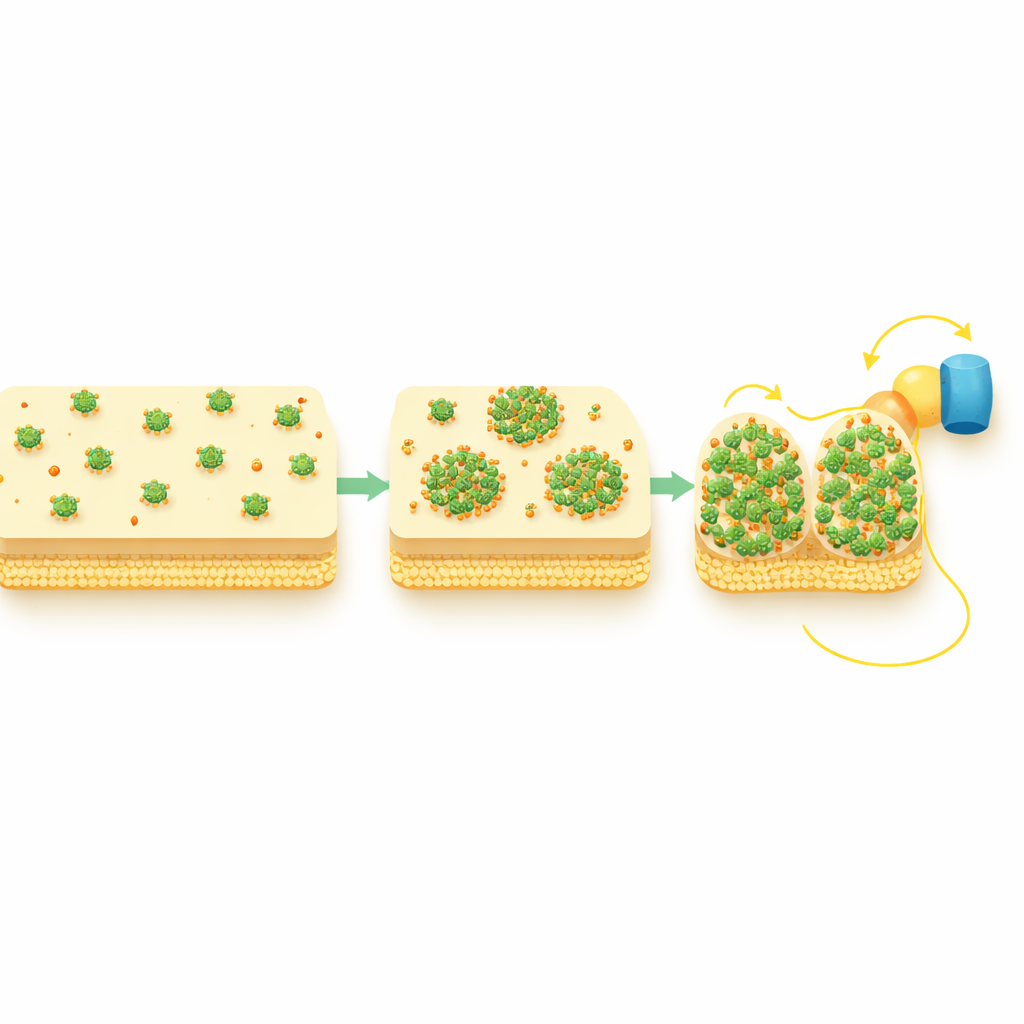
Hücre Zarı Boyunca Daha Kısa Yollar Oluşturmak
Çalışma ayrıca doğrudan CymA ile elektron alışverişi yapan ve onları dış zara doğru ileten iki periplazmik taşıyıcı protein STC ve FccA’yı da izledi. Oksijen bakımından zengin koşullarda bu taşıyıcılar eşit şekilde yayılıyordu, ancak aktif hücre dışı elektron transferi sırasında onlar da noktasal desenler benimsedi ve mekansal olarak CymA kümeleriyle örtüştü. Genetik testler, CymA’nın ilk olarak yeniden düzenlendiğini ve ardından bu ortakları çektiğini, tersinin olmadığını gösterdi. Başka bir deyişle, CymA punctaları aşağı doğru giden taşıyıcıları kompakt, yoğun trafikli bağlantı noktalarına toplayan merkezler gibi davranarak hücrenin içinden yüzeyine olan elektron yolunu etkili biçimde kısaltır ve güçlendirir.
Zar Kimyasıyla Sürülen Sıvıya Benzer Kondansatlar
Bireysel CymA moleküllerini izleyerek araştırmacılar, punctalar içindeki proteinlerin hareketli kaldığını ve kümelerin içeri girip çıkabildiğini, ayrıca kümelerin büyüme koşullarına bağlı olarak ortaya çıkıp kaybolabildiğini keşfettiler. Bunlar, katı kompleksler veya hasarlı agregalar yerine protein ve diğer moleküllerden oluşan sıvıya benzer “biyomoleküler kondansatlar”ın ayırt edici özellikleridir. İç zar içinde elektron taşıyan küçük bir membran molekülü olan menakinonun ölçümleri, seviyelerinin CymA punctalarının ortaya çıkmasıyla birlikte arttığını gösterdi. Yazarlar, menakinon açısından zengin membran bölgelerinin özellikle hücre kutuplarına yakın CymA’yı kondansat benzeri alanlara çeken bir iskelet görevi gördüğünü öne sürüyor.
Doğa ve Teknoloji İçin Neden Önemli?
Genel olarak çalışma, Shewanellanın hücre dışı elektron transferini kontrol etmek için yalnızca hangi proteinleri ürettiğine güvenmediğini; aynı zamanda bu proteinlerin dinamik kümelere ne zaman ve nerede toplandığına da bağlı olduğunu gösteriyor. Muhtemelen yerel zar kimyası tarafından organize edilen CymA kondansatları, ortak proteinleri çekerek geçici “elektriksel sıcak noktalar” oluşturur ve hücre zarfı boyunca elektron akışını artırır. Bir okuyucu için bunun anlamı şudur: bakteriler bile kendiliğinden bir tür devre kurarak iç parçalarını talep üzerine yeniden düzenleyip kayalara, metallere veya elektrotlara bağlanabiliyor. Bu tür protein kendi kendine örgütlenmesini anlamak ve sonunda yönlendirmek, daha iyi mikrobiyal yakıt hücreleri, daha verimli biyoelektrokimyasal fabrikalar ve metal ile kirletici temizliği için yeni stratejiler tasarlamada bilimcilere yardımcı olabilir.
Atıf: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Anahtar kelimeler: hücre dışı elektron transferi, Shewanella, bakteriyel biyoelektrik, biyomoleküler kondansatlar, mikrobiyal yakıt hücreleri