Clear Sky Science · es
La organización espaciotemporal de una proteína de membrana controla la transferencia extracelular de electrones en bacterias
Cómo las bacterias mueven electricidad fuera de sus células
Algunas bacterias pueden literalmente «respirar» minerales o electrodos en lugar de oxígeno, moviendo pequeñas cargas eléctricas hacia dentro y fuera de sus células. Este truco eléctrico alimenta su supervivencia en ambientes pobres en oxígeno y sirve para tecnologías como pilas de combustible microbianas y biorreactores que limpian la contaminación. El estudio descrito aquí plantea una pregunta aparentemente simple: ¿cómo se disponen en el espacio y el tiempo las proteínas clave en una célula microbiana para que este flujo de electrones a larga distancia funcione realmente?
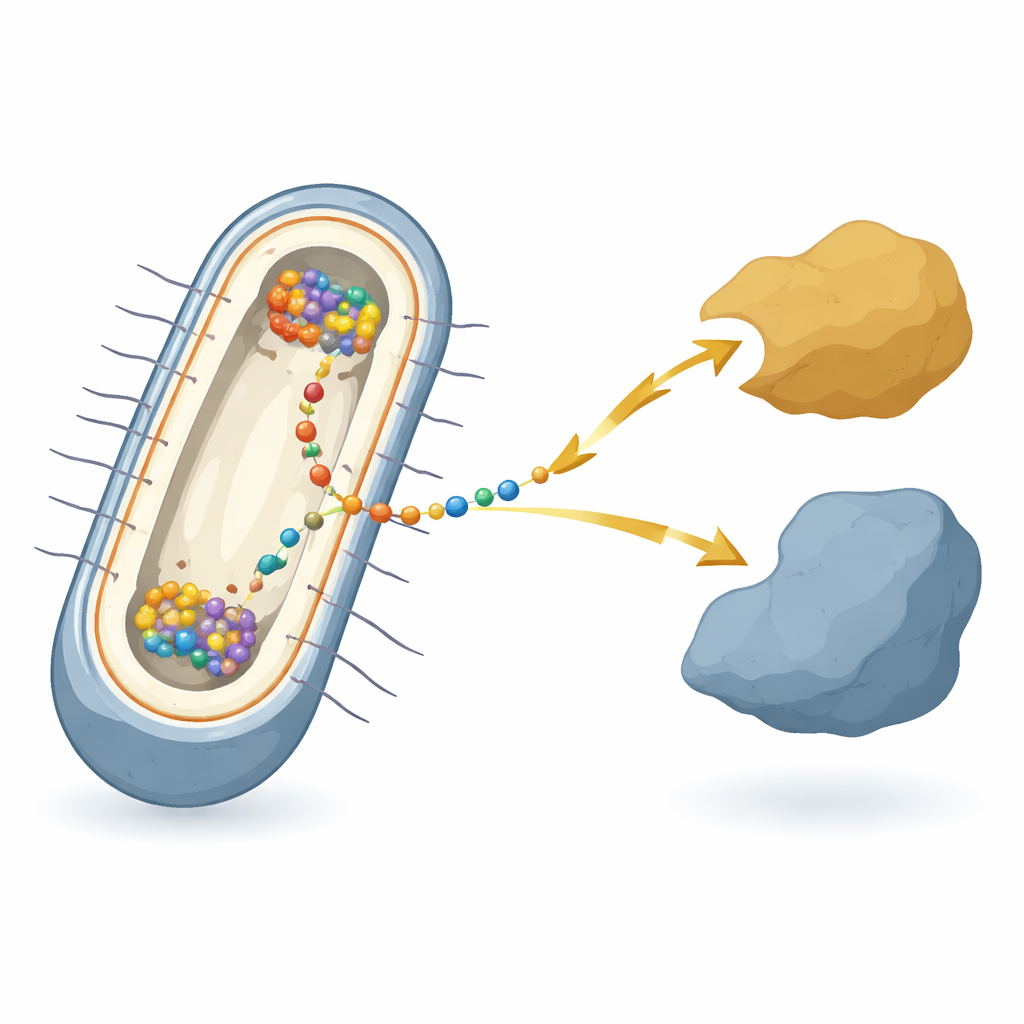
Un microbio que vive de óxido de hierro y cables
El trabajo se centra en la bacteria Shewanella oneidensis, una especie modelo famosa por la «transferencia extracelular de electrones»: ceder o recibir electrones a partir de metales, minerales o electrodos fuera de la célula. En estas bacterias, los electrones deben atravesar dos membranas y un espacio intermembrana, pasando por un relevo de muchas proteínas diferentes. En el centro de ese relevo, en la membrana interna, se encuentra una proteína central llamada CymA. CymA comunica el metabolismo interno de la célula por un lado y a las proteínas transportadoras en el espacio periplásmico por el otro. A pesar de décadas de trabajo sobre las piezas individuales, no estaba claro cómo se coordinan todos estos componentes dentro de cada célula viva cuando la bacteria realiza efectivamente esta respiración eléctrica.
Las proteínas se autoorganizan en puntos brillantes
Usando microscopía de fluorescencia avanzada capaz de seguir proteínas individuales en células individuales, los investigadores marcaron CymA con indicadores luminosos y observaron su comportamiento bajo distintas condiciones de crecimiento. Cuando las bacterias crecían con oxígeno, un estado en que CymA está inactiva, la proteína se distribuía de manera uniforme por la membrana interna. Pero cuando las células se vieron obligadas a depender de la transferencia extracelular de electrones en condiciones sin oxígeno, CymA se agrupó inesperadamente en puntos brillantes distintivos, o «puntos» (puncta), a menudo cerca de los polos celulares. Esta reorganización ocurrió tanto cuando los electrones salían de la célula hacia minerales como cuando entraban desde hierro metálico o electrodos. Importante: la cantidad total de CymA no cambió mucho; lo que cambió fue su distribución espacial.
Los cúmulos dinámicos permiten un flujo de electrones más fuerte
Al observar muchas células a lo largo del tiempo, el equipo encontró que solo una fracción de las células formaba cúmulos de CymA en un momento dado, y el momento variaba entre células. Sin embargo, en células individuales, la transición de una distribución uniforme a los puncta fue sorprendentemente rápida una vez iniciada, lo que sugiere una reorganización interna súbita tras un retraso variable. Para comprobar si esos puncta importaban realmente para el rendimiento eléctrico, los investigadores combinaron electrodos activados por luz con microscopía y midieron fotocorrientes diminutas de células individuales. Las células que habían formado puncta de CymA mostraron una captación de electrones desde el electrodo significativamente mayor que las que no presentaban puncta, pese a que ambos tipos contenían cantidades similares de CymA. Esto indica que la agrupación, y no la mera abundancia proteica, es lo que permite una transferencia extracelular de electrones eficiente.
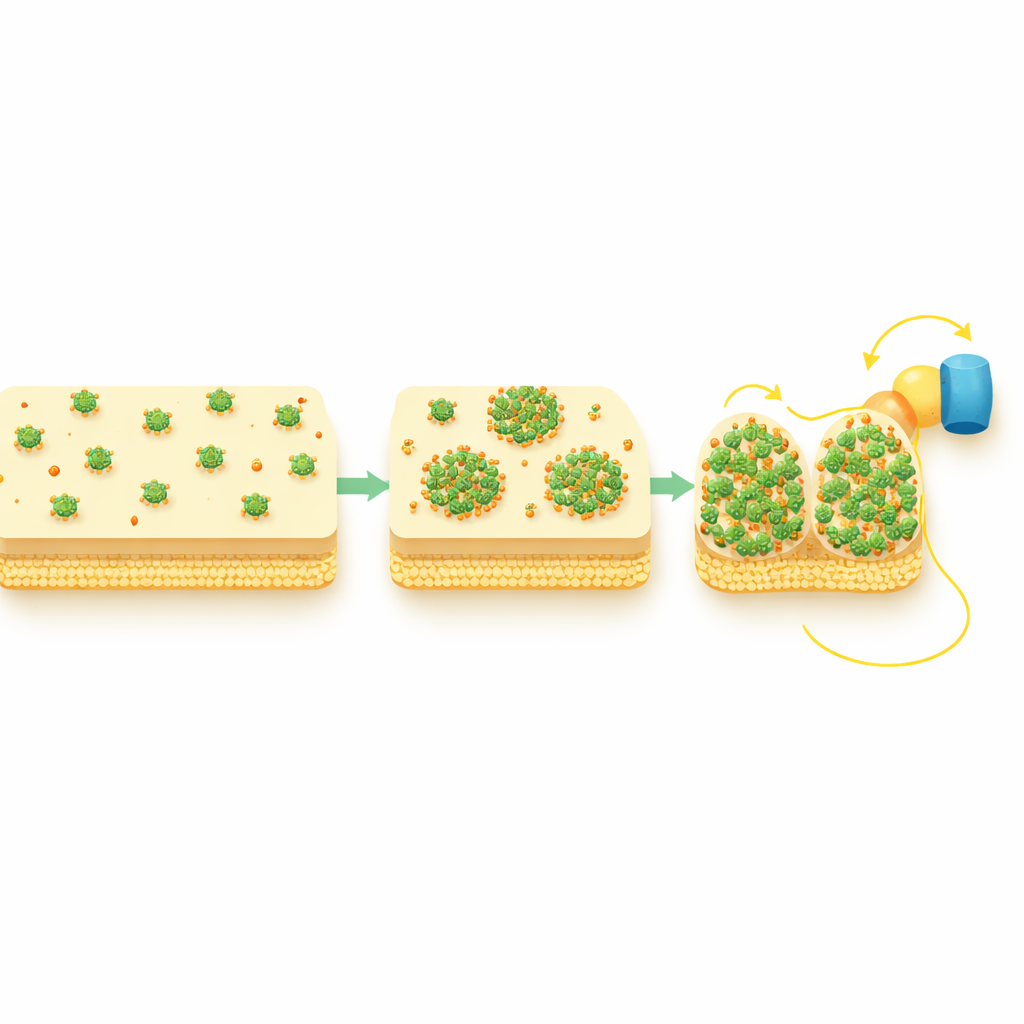
Construir rutas más cortas a través del envoltorio celular
El estudio también siguió a dos proteínas transportadoras periplásmicas, STC y FccA, que intercambian electrones directamente con CymA y los transmiten hacia la membrana externa. En condiciones ricas en oxígeno, estas transportadoras se distribuían de forma homogénea, pero durante la transferencia extracelular activa adoptaron patrones punteados y se solaparon espacialmente con los cúmulos de CymA. Pruebas genéticas mostraron que CymA se reorganiza primero y luego atrae a estos colaboradores, no al revés. En otras palabras, los puncta de CymA actúan como centros que reúnen a las transportadoras descendentes en intersecciones compactas y de alto tránsito, acortando y reforzando efectivamente la vía de electrones desde el interior de la célula hasta su superficie.
Condensados de tipo líquido impulsados por la química de la membrana
Al seguir moléculas individuales de CymA, los investigadores descubrieron que las proteínas dentro de los puncta permanecían móviles y podían entrar y salir de los cúmulos, y que los cúmulos mismos podían aparecer y desaparecer según las condiciones de crecimiento. Estas son señas de identidad de los «condensados biomoleculares», gotículas de tipo líquido formadas por colecciones de proteínas y otras moléculas en lugar de complejos rígidos o agregados dañados. Mediciones de una pequeña molécula de membrana llamada menaquinona, que transporta electrones dentro de la membrana interna, mostraron que sus niveles aumentan a la par de la aparición de los puncta de CymA. Los autores proponen que regiones de la membrana enriquecidas en menaquinona actúan como andamiajes que reclutan a CymA en dominios similares a condensados, especialmente cerca de los polos celulares.
Por qué importa esto para la naturaleza y la tecnología
En conjunto, el estudio muestra que Shewanella no depende solo de qué proteínas sintetiza para controlar la transferencia extracelular de electrones; también depende de cuándo y dónde estas proteínas se agrupan en cúmulos dinámicos. Los condensados de CymA, probablemente organizados por la química local de la membrana, atraen a proteínas asociadas para formar «puntos eléctricos calientes» temporales que aumentan el flujo de electrones a través del envoltorio celular. Para un lector general, esto significa que incluso las bacterias emplean una especie de circuito autoensamblado, reorganizando sus componentes internos bajo demanda para conectarse a rocas, metales o electrodos. Comprender y, eventualmente, dirigir este tipo de autoorganización proteica podría ayudar a diseñar mejores pilas de combustible microbianas, fábricas bioelectroquímicas más eficientes y nuevas estrategias para limpiar contaminación por metales y otros poluentes.
Cita: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Palabras clave: transferencia extracelular de electrones, Shewanella, bioelectricidad bacteriana, condensados biomoleculares, pilas de combustible microbianas