Clear Sky Science · ja
膜タンパク質の時空間的な配列が細菌の細胞外電子移動を制御する
細菌はどうやって細胞外に電気を移動させるのか
一部の細菌は酸素の代わりに鉱物や電極に“呼吸”しており、微小な電荷を細胞の内外にやり取りすることができます。この電気的な仕組みは酸素が乏しい環境での生存を支え、微生物燃料電池や汚染物質を分解するバイオリアクターといった技術の基盤にもなっています。本研究は一見単純な問いを立てます:微生物細胞内の主要なタンパク質群は、どのように時空間的に配置されることで、この長距離の電子輸送が実際に機能するのか?
さびや電極を“食べる”微生物
研究はモデル種である Shewanella oneidensis に焦点を当てています。この種は「細胞外電子移動」で有名で、細胞外の金属や鉱物、電極に電子を渡したり、逆に受け取ったりします。これらの細菌では、電子は二重膜とその間の空隙を越えて移動する必要があり、多様なタンパク質のリレーを経由します。そのリレーの中心に膜内タンパク質CymAがあります。CymAは一方で細胞内の代謝とやり取りし、他方で膜間スペースにいるシャトルタンパク質と連携します。個々の要素については何十年もの研究がありますが、細菌が実際にこの電気的呼吸を行うときに、これら全ての成分が生きた細胞内でどのように協調しているかは明らかではありませんでした。
タンパク質が明るい点(スポット)に自己組織化する
単一タンパク質を単一細胞で追跡できる高感度蛍光顕微鏡を用いて、研究者たちはCymAに蛍光タグを付け、さまざまな増殖条件下でその振る舞いを観察しました。酸素存在下、CymAが休止状態にあるときは、このタンパク質は内膜を均一に取り囲んでいました。しかし、細胞が酸素なしで細胞外電子移動に頼らざるを得ない状況になると、CymAは予想外に明瞭な明るい点、いわゆる“パンクタ”に集まり、しばしば細胞の極付近に出現しました。この再編成は電子が細胞から鉱物へ流れる場合でも、金属イオンや電極から細胞へ流れる場合でも起こりました。重要なのは、CymAの総量は大きく変わらなかったことで、変化したのは量ではなくその空間的配置でした。
動的なクラスターが電子流を強化する
多数の細胞を長時間観察すると、ある瞬間にCymAクラスターを形成するのは細胞の一部だけであり、形成のタイミングは細胞ごとにばらつきがあることが分かりました。ただし、個々の細胞内では、均一分布からパンクタへの転換が始まると驚くほど速く進行し、可変の遅延の後に急激な内部再編成が起きることが示唆されました。これらのパンクタが実際に電気的性能に寄与するかを検証するために、研究者たちは光で作動する電極と顕微鏡を組み合わせ、単一細胞からの微弱な光電流を測定しました。CymAパンクタを形成した細胞は、同程度のCymA量を持ちながらパンクタを形成していない細胞よりも電極からの電子取り込みが有意に強かった。これは効率的な細胞外電子移動を可能にしているのがタンパク質量そのものではなく、クラスタリング(集積)であることを示しています。
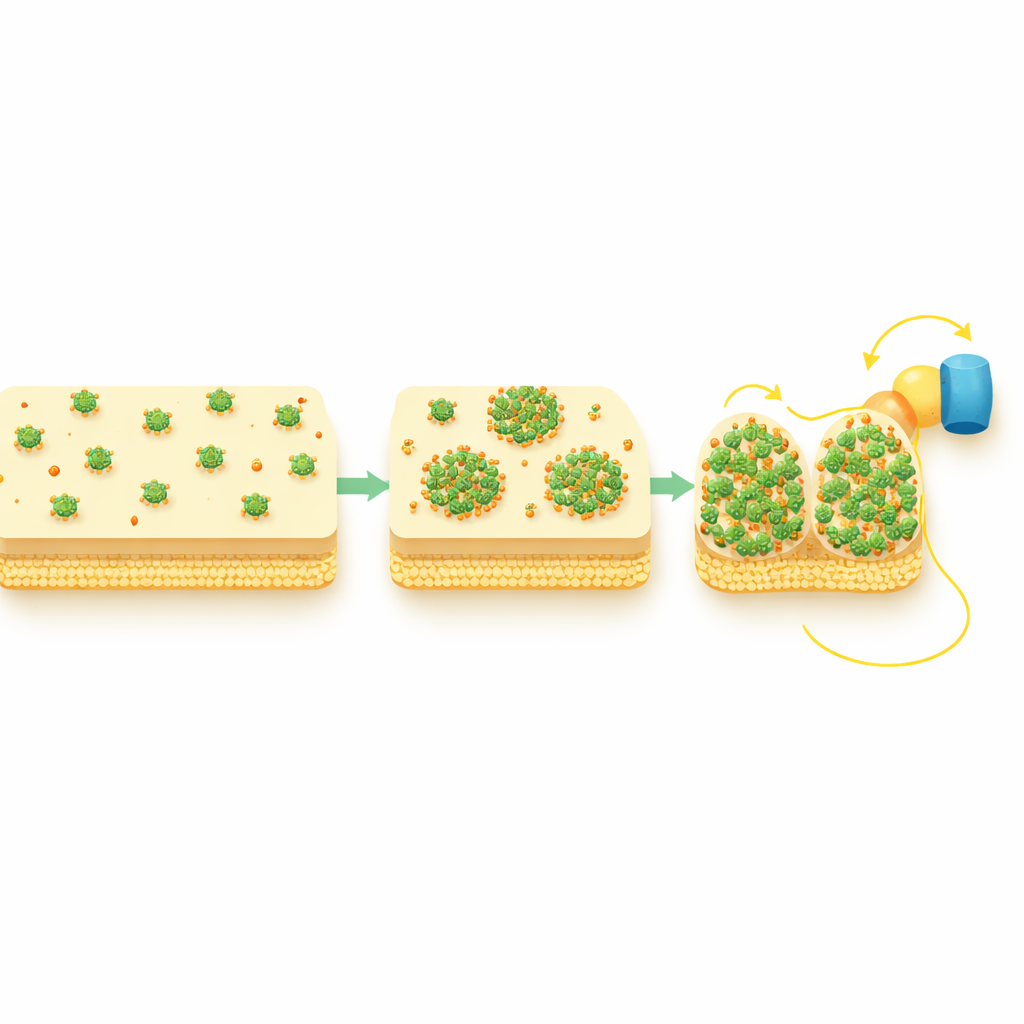
細胞包膜を越えるより短い経路を構築する
研究では、CymAと直接電子をやり取りして外膜へと渡す二つのペリプラズム(膜間)シャトルタンパク質、STCとFccAも追跡しました。酸素が豊富な条件下ではこれらのシャトルは均一に分布していましたが、活発な細胞外電子移動時にはパンクタ状になり、CymAクラスターと空間的に重なることが分かりました。遺伝学的検証により、まずCymAが再編成してからこれらのパートナーを引き寄せることが示され、逆は成り立ちませんでした。言い換えれば、CymAのパンクタはハブとして機能し、下流のシャトルを集めてコンパクトで交通量の多い接合点を形成し、細胞内から表面への電子経路を実質的に短くかつ強化しているのです。
膜化学が駆動する液状の凝縮体
CymA分子を個別に追跡したところ、パンクタ内のタンパク質は移動性を保ちクラスターの内外を出入りでき、クラスター自体も増殖条件によって出現・消失することがわかりました。これらは剛直な複合体や損傷した凝集体ではなく、タンパク質や他の分子の集合により形成される“生体分子凝縮体”に典型的な性質です。内膜内で電子を運ぶ小さな膜分子メナキノンの測定は、メナキノン量がCymAパンクタ出現とともに増加することを示しました。著者らは、メナキノンが局所的に豊富な膜領域が足場となってCymAを凝縮体様のドメインへと誘引し、特に細胞極付近でこれを組織化していると提案しています。
自然と技術にとっての意義
総じて本研究は、Shewanellaが細胞外電子移動を制御する際に単にどのタンパク質を作るかだけでなく、これらのタンパク質がいつどこに集まるかという時空間的な自己組織化にも依存していることを示しています。局所的な膜化学により組織化されると考えられるCymA凝縮体は、パートナータンパク質を引き寄せて一時的な「電気のホットスポット」を形成し、細胞包膜を越えた電子の流れを増強します。一般読者にとっては、細菌でさえ自己組織化した回路のように内部部品を必要に応じて並べ替え、岩石や金属、電極に“接続”しているということです。こうしたタンパク質の自己組織化を理解し、最終的には制御できるようになれば、微生物燃料電池の性能向上や効率的なバイオ電気化学工場の設計、金属や汚染物質の浄化の新たな戦略につながる可能性があります。
引用: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
キーワード: 細胞外電子移動, シワネラ, 細菌性バイオ電気, 生体分子凝縮体, 微生物燃料電池