Clear Sky Science · ru
Пространственно-временная организация мембранного белка контролирует внеклеточный перенос электронов у бактерий
Как бактерии перемещают электричество за пределы своих клеток
Некоторые бактерии буквально «дышат» минералами или электродами вместо кислорода, перенося крошечные электрические заряды внутрь и наружу своих клеток. Этот электрический трюк поддерживает их выживание в условиях малого содержания кислорода и питает технологии типа микробных топливных элементов и биореакторов для очистки загрязнений. Описанное здесь исследование задаёт на первый взгляд простой вопрос: как ключевые белки микробной клетки организуются в пространстве и времени, чтобы этот дальнодействующий поток электронов действительно работал?
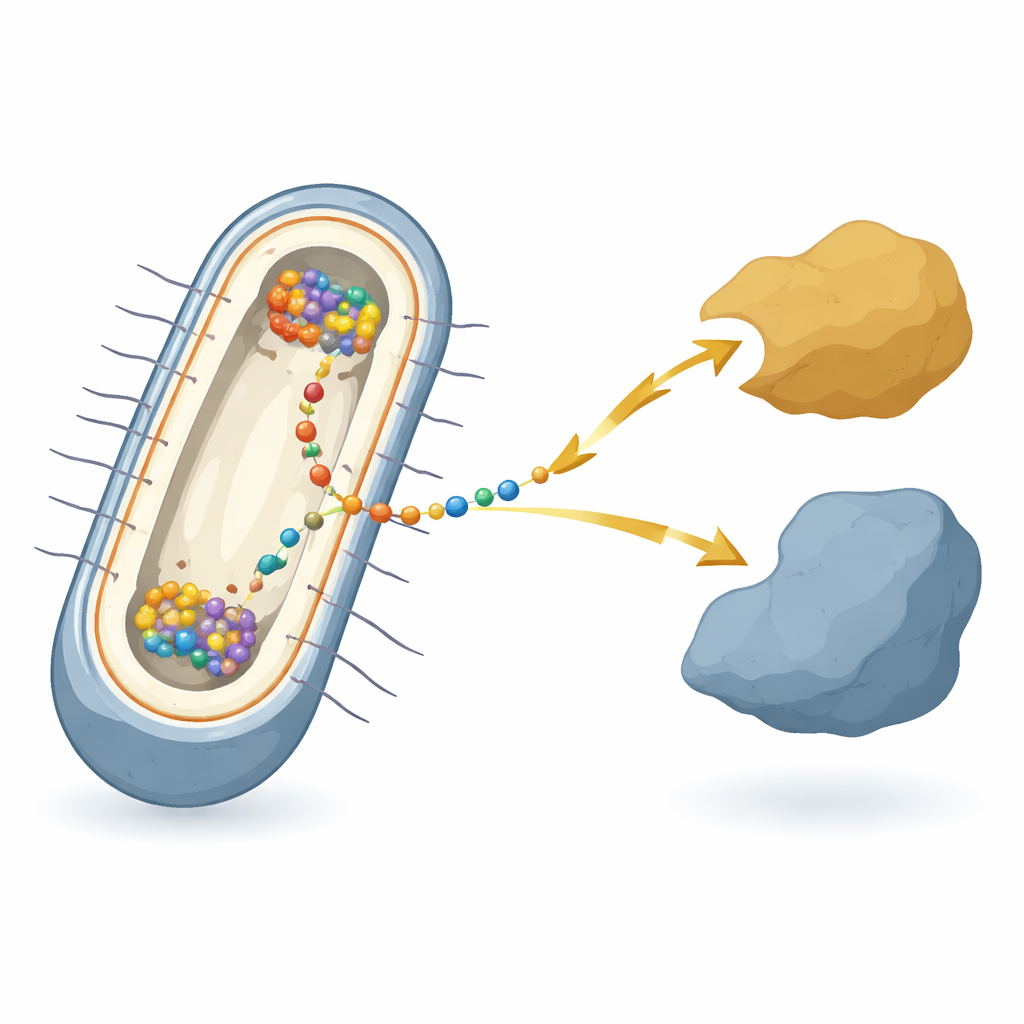
Микроб, живущий на ржавчине и проводах
Работа посвящена бактерии Shewanella oneidensis — модельному виду, известному своим «внеклеточным переносом электронов» — передачей электронов металлам, минералам или электродам за пределами клетки. В этих бактериях электроны должны пересечь две мембраны и пространство между ними, проходя через цепочку разных белков. В центре этой цепочки, во внутренней мембране, находится узловой белок CymA. CymA связывает внутренний метаболизм клетки с шевелящимися переносчиками в периплазме. Несмотря на многолетние исследования отдельных компонентов, оставалось неясным, как все эти элементы координируются внутри живой клетки в момент электрического дыхания.
Белки самособираются в яркие точки
С помощью продвинутой флуоресцентной микроскопии, способной отслеживать отдельные белки в отдельных клетках, исследователи пометили CymA светящимися маркерами и наблюдали за её поведением в разных условиях роста. При выращивании с кислородом, когда CymA неактивна, белок равномерно распределялся по внутренней мембране. Но когда клетки были вынуждены полагаться на внеклеточный перенос электронов в бескислородных условиях, CymA неожиданно собиралась в отдельные яркие пятна, или «пунктa», часто у полюсов клетки. Такая реорганизация происходила как при отдаче электронов клеткой минералам, так и при их приёме из металлического железа или электродов. Важно, что общее количество CymA почти не менялось; изменялось её пространственное расположение.
Динамичные кластеры усиливают поток электронов
Наблюдая многие клетки с течением времени, команда обнаружила, что в любой момент только часть клеток формировала кластеры CymA, а момент их появления различался от клетки к клетке. В отдельных клетках переход от равномерного распределения к пунктa происходил удивительно быстро после начала, что указывает на внезапную внутреннюю реорганизацию после переменной задержки. Чтобы проверить, действительно ли эти пунктa важны для электрической активности, исследователи сочетали светоуправляемые электроды с микроскопией и измеряли крошечные фототоки от отдельных клеток. Клетки с образовавшимися пунктa CymA демонстрировали существенно более сильный приём электронов с электрода, чем клетки без пунктa, хотя обе группы содержали схожее количество CymA. Это указывает на то, что именно кластеризация, а не просто количество белка, обеспечивает эффективный внеклеточный перенос электронов.
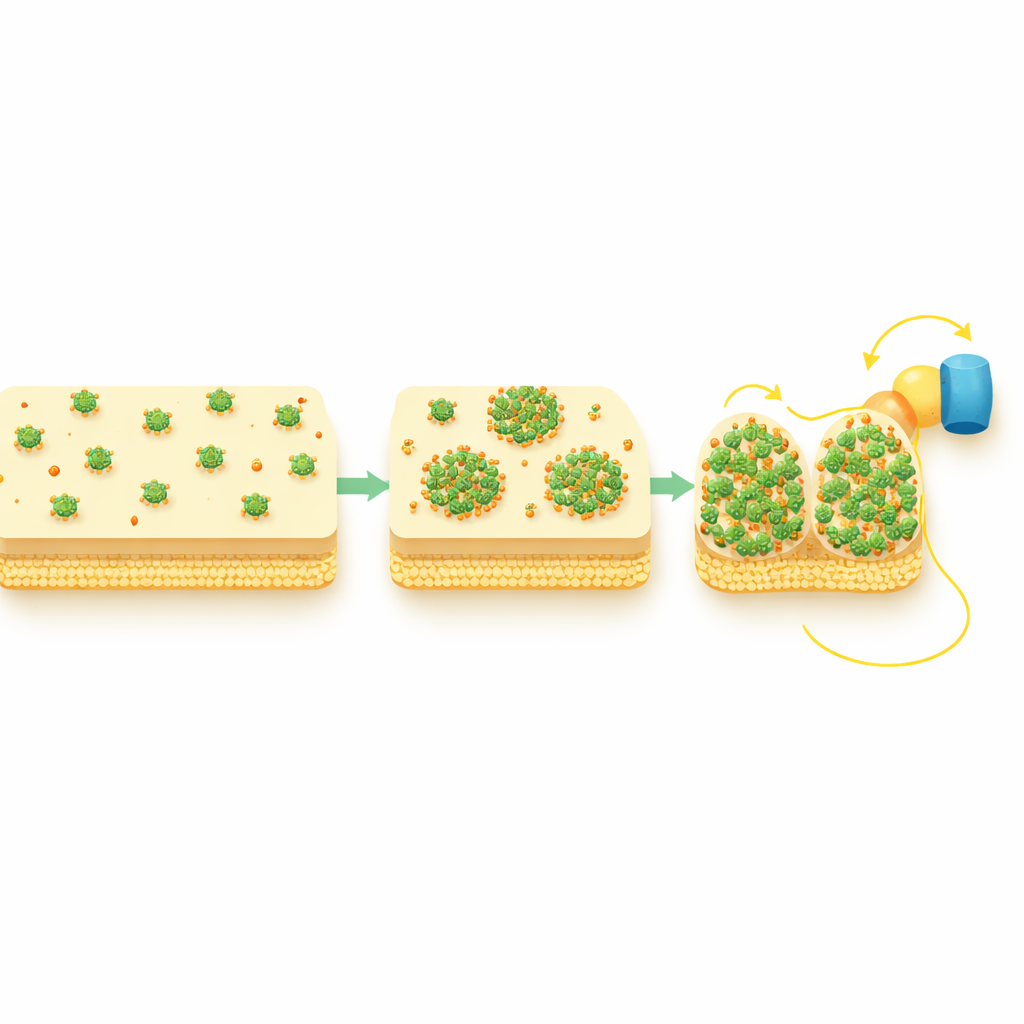
Построение более коротких путей через оболочку клетки
Исследование также отслеживало два периплазматических переносчика, STC и FccA, которые напрямую обмениваются электронами с CymA и передают их дальше к наружной мембране. В условиях, богатых кислородом, эти переносчики распределялись равномерно, но при активном внеклеточном переносе электронов они также приобретали пунктатные рисунки и пространственно совпадали с кластерами CymA. Генетические тесты показали, что CymA реорганизуется первой и затем привлекает этих партнёров, а не наоборот. Иными словами, пунктa CymA действуют как узлы, собирающие последующие переносчики в компактные, интенсивно используемые узлы, эффективно укорачивая и усиливая путь электронов от внутренности клетки к её поверхности.
Жидкоподобные конденсаты, управляемые химией мембраны
Отслеживая отдельные молекулы CymA, исследователи обнаружили, что белки внутри пунктa остаются подвижными и могут переходить внутрь и наружу кластеров, а сами кластеры могут появляться и исчезать в зависимости от условий роста. Это характерные признаки «биомолекулярных конденсатов» — жидкоподобных капелек, образующихся коллекциями белков и других молекул, а не жёстких комплексов или повреждённых агрегатов. Измерения небольшого мембранного молекулы менакинона, который переносит электроны внутри внутренней мембраны, показали, что его уровень растёт одновременно с появлением пунктa CymA. Авторы предполагают, что участки мембраны, обогащённые менакиноном, выступают в роли каркасов, привлекающих CymA в домены, похожие на конденсаты, особенно у полюсов клетки.
Почему это важно для природы и технологий
В целом исследование показывает, что Shewanella управляет внеклеточным переносом электронов не только через набор синтезируемых белков, но и через то, когда и где эти белки собираются в динамичные кластеры. Конденсаты CymA, вероятно организованные локальной химией мембраны, втягивают партнёрские белки, формируя временные «электрические горячие точки», которые усиливают поток электронов через оболочку клетки. Для непрофессионального читателя это значит, что даже бактерии используют нечто вроде самоорганизующихся схем: они перестраивают свои внутренние элементы по требованию, чтобы «подключиться» к камням, металлам или электродам. Понимание и, в перспективе, управление такой самоорганизацией белков может помочь учёным создать более эффективные микробные топливные элементы, улучшить биоэлектрохимические фабрики и разработать новые стратегии для очистки от металлов и загрязняющих веществ.
Цитирование: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Ключевые слова: внеклеточный перенос электронов, Shewanella, бактериальная биоэлектричность, биомолекулярные конденсаты, микробные топливные элементы