Clear Sky Science · fr
Organisation spatiotemporelle des protéines membranaires contrôlant le transfert d’électrons extracellulaire bactérien
Comment les bactéries déplacent l’électricité à l’extérieur de leurs cellules
Certaines bactéries peuvent littéralement « respirer » des minéraux ou des électrodes au lieu de l’oxygène, transférant de minuscules charges électriques vers l’extérieur ou l’intérieur de leurs cellules. Ce tour électrique alimente leur survie en milieu pauvre en oxygène et alimente des technologies comme les piles microbiennes et les bioréacteurs de dépollution. L’étude décrite ici pose une question apparemment simple : comment les protéines clés d’une cellule microbienne s’organisent-elles dans l’espace et le temps pour que ce flux d’électrons sur de longues distances fonctionne réellement ?
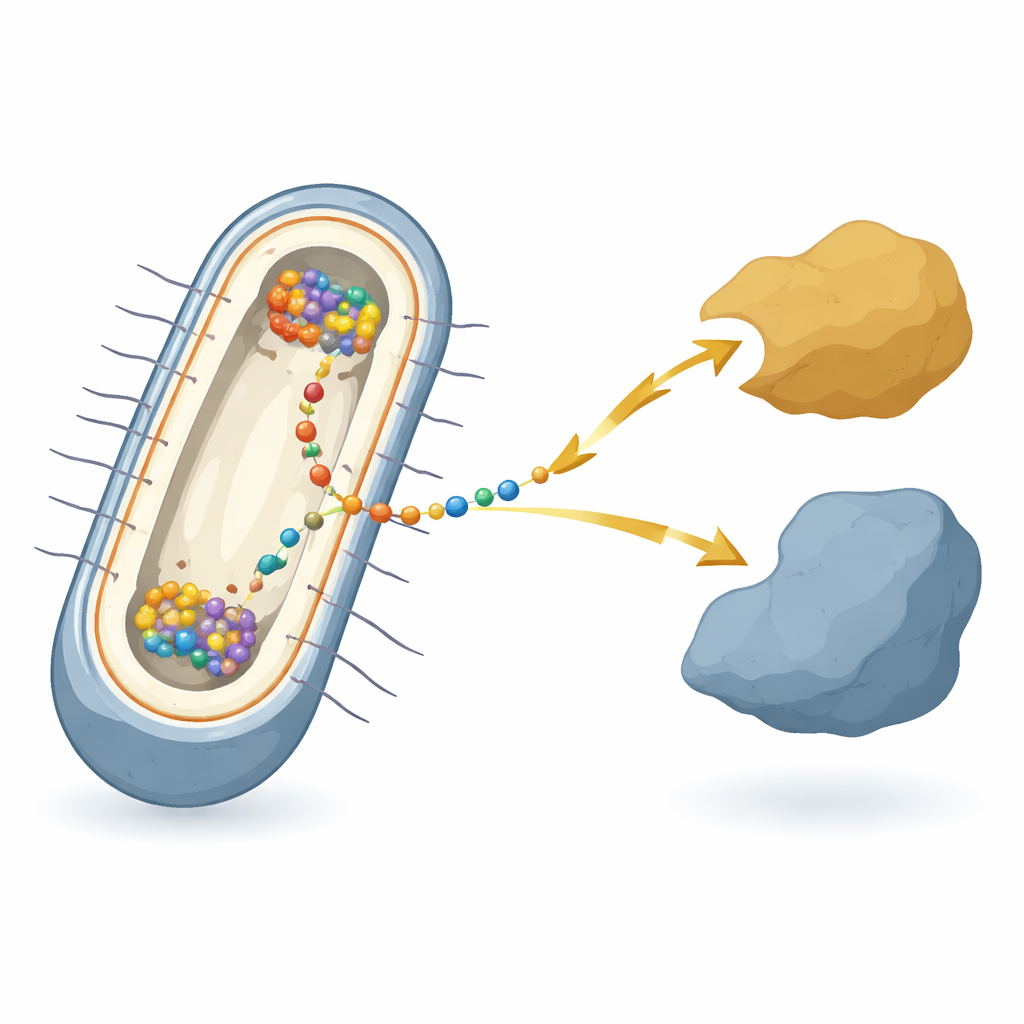
Un microbe qui vit sur la rouille et les fils
Le travail se concentre sur la bactérie Shewanella oneidensis, une espèce modèle célèbre pour le « transfert d’électrons extracellulaire » — le fait de céder ou de recevoir des électrons vers ou depuis des métaux, des minéraux ou des électrodes situés à l’extérieur de la cellule. Dans ces bactéries, les électrons doivent traverser deux membranes et l’espace entre elles, en passant par un relais composé de nombreuses protéines différentes. Au cœur de ce relais, dans la membrane interne, se trouve une protéine centrale appelée CymA. CymA communique d’un côté avec le métabolisme interne de la cellule et de l’autre avec des protéines navettes présentes dans l’espace périplasmique. Malgré des décennies d’études sur les parties individuelles, on ne comprenait pas clairement comment tous ces composants sont coordonnés à l’intérieur de chaque cellule vivante lorsque la bactérie réalise réellement cette respiration électrique.
Les protéines s’auto-organisent en taches lumineuses
À l’aide d’une microscopie à fluorescence avancée capable de suivre des protéines uniques dans des cellules uniques, les chercheurs ont marqué CymA avec des repères lumineux et observé son comportement selon différentes conditions de croissance. Lorsque les bactéries croissaient en présence d’oxygène, état où CymA est inactif, la protéine se répartissait uniformément sur la membrane interne. Mais lorsque les cellules étaient contraintes de dépendre du transfert d’électrons extracellulaire en l’absence d’oxygène, CymA se rassemblait de manière inattendue en taches distinctes, ou « puncta », souvent près des pôles cellulaires. Cette réorganisation survenait que les électrons sortent de la cellule vers des minéraux ou entrent dans la cellule depuis du fer métallique ou des électrodes. Il est important de noter que la quantité totale de CymA ne changeait pas beaucoup ; ce qui changeait, c’était sa répartition spatiale.
Des amas dynamiques permettent un flux d’électrons plus fort
En observant de nombreuses cellules au fil du temps, l’équipe a constaté qu’à un instant donné, seule une fraction des cellules formait des amas de CymA, et que le moment de leur apparition variait d’une cellule à l’autre. Dans les cellules individuelles, la transition d’une distribution uniforme à des puncta était cependant étonnamment rapide une fois qu’elle commençait, ce qui suggère une réorganisation interne soudaine après un délai variable. Pour tester si ces puncta ont un effet sur la performance électrique, les chercheurs ont combiné des électrodes activées par la lumière avec la microscopie et ont mesuré de minuscules photocourants provenant de cellules uniques. Les cellules ayant formé des puncta de CymA présentaient une prise d’électrons depuis l’électrode significativement plus forte que celles sans puncta, bien que les deux types contiennent des quantités similaires de CymA. Cela indique que c’est le regroupement, et non la simple abondance de la protéine, qui permet un transfert d’électrons extracellulaire efficace.
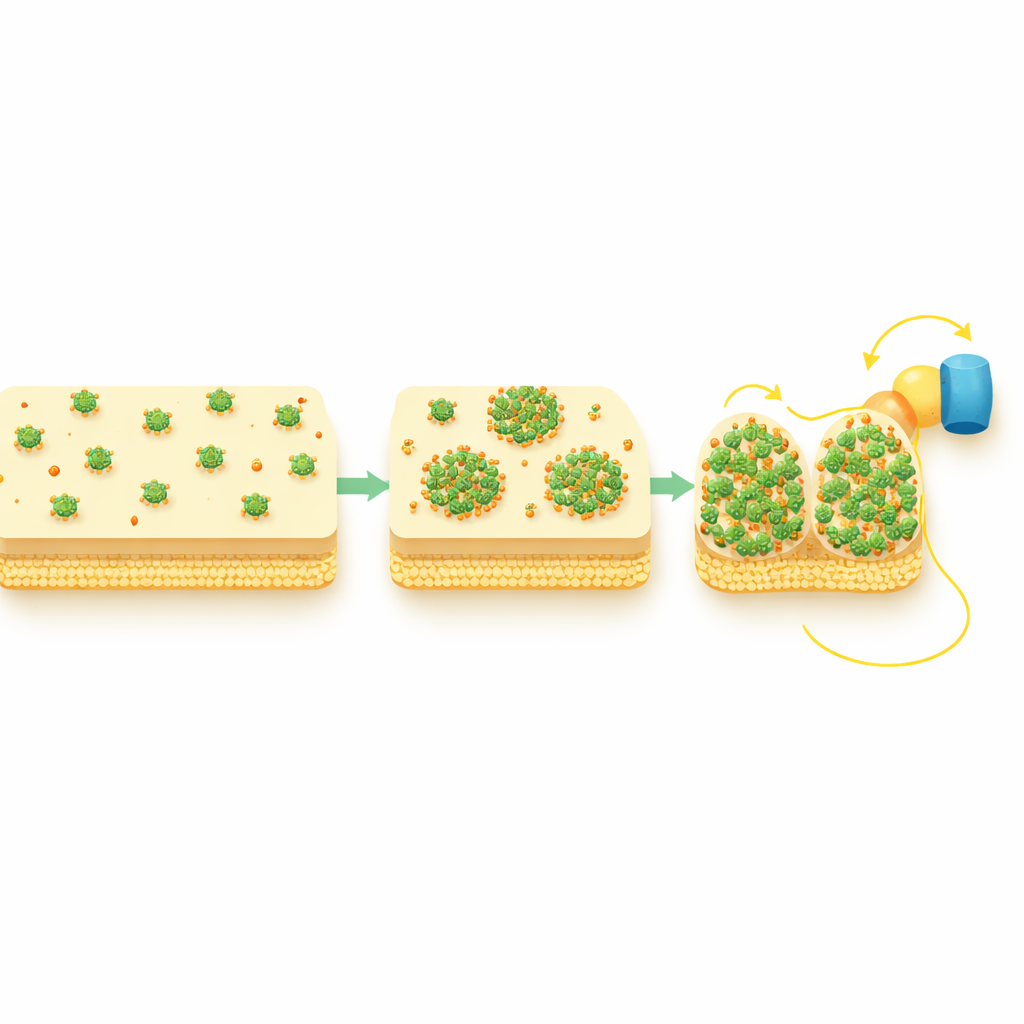
Construire des voies plus courtes à travers l’enveloppe cellulaire
L’étude a également suivi deux protéines navettes périplasmatiques, STC et FccA, qui échangent directement des électrons avec CymA et les transmettent vers la membrane externe. En présence d’oxygène, ces navettes étaient réparties uniformément, mais durant le transfert d’électrons extracellulaire actif elles adoptaient elles aussi des motifs ponctués et chevauchaient spatialement les amas de CymA. Des tests génétiques ont montré que CymA se réorganise en premier, puis attire ces partenaires, et non l’inverse. Autrement dit, les puncta de CymA agissent comme des centres qui concentrent les navettes en aval en jonctions compactes et très fréquentées, raccourcissant et renforçant ainsi la voie électronique de l’intérieur de la cellule vers sa surface.
Condensats de type liquide pilotés par la chimie membranaire
En suivant des molécules individuelles de CymA, les chercheurs ont découvert que les protéines à l’intérieur des puncta restaient mobiles et pouvaient entrer et sortir des amas, et que les amas eux-mêmes pouvaient apparaître et disparaître selon les conditions de croissance. Ce sont là des caractéristiques des « condensats biomoléculaires », des gouttelettes de type liquide formées par des collections de protéines et d’autres molécules plutôt que des complexes rigides ou des agrégats endommagés. Des mesures d’une petite molécule membranaire appelée menaquinone, qui transporte des électrons à l’intérieur de la membrane interne, ont montré que ses niveaux augmentent en parallèle de l’apparition des puncta de CymA. Les auteurs proposent que des régions de la membrane enrichies en menaquinone servent d’échafaudages qui recrutent CymA dans des domaines de type condensat, en particulier près des pôles cellulaires.
Pourquoi c’est important pour la nature et la technologie
Dans l’ensemble, l’étude montre que Shewanella ne dépend pas seulement des protéines qu’elle fabrique pour contrôler le transfert d’électrons extracellulaire ; elle dépend aussi du moment et du lieu où ces protéines se rassemblent en amas dynamiques. Les condensats de CymA, vraisemblablement organisés par la chimie membranaire locale, attirent des protéines partenaires pour former des « points chauds » électriques temporaires qui augmentent le flux d’électrons à travers l’enveloppe cellulaire. Pour le lecteur non spécialiste, cela signifie que même les bactéries utilisent une sorte de circuit auto-assemblé, réorganisant leurs composants internes à la demande pour se brancher sur des roches, des métaux ou des électrodes. Comprendre et éventuellement contrôler ce type d’auto-organisation protéique pourrait aider les scientifiques à concevoir de meilleures piles microbiennes, des usines bioélectrochimiques plus efficaces et de nouvelles stratégies pour dépolluer les métaux et les contaminants.
Citation: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Mots-clés: transfert d’électrons extracellulaire, Shewanella, bioélectricité bactérienne, condensats biomoléculaires, piles microbiennes