Clear Sky Science · pl
Przestrzenno‑czasowa organizacja białek błonowych kontroluje bakteryjny zewnątrzkomórkowy transfer elektronów
Jak bakterie przesyłają prąd poza swoje komórki
Niektóre bakterie potrafią dosłownie „oddychać” minerałami lub elektrodami zamiast tlenem, przemieszczając drobne ładunki elektryczne do wnętrza i na zewnątrz komórek. Ten elektryczny trik napędza ich przetrwanie w środowiskach ubogich w tlen i zasila technologie takie jak mikrobowe ogniwa paliwowe oraz bioreaktory oczyszczające zanieczyszczenia. Opisywane badanie stawia pozornie proste pytanie: jak kluczowe białka w komórce mikroba układają się w przestrzeni i czasie, aby ten długodystansowy przepływ elektronów mógł rzeczywiście zachodzić?
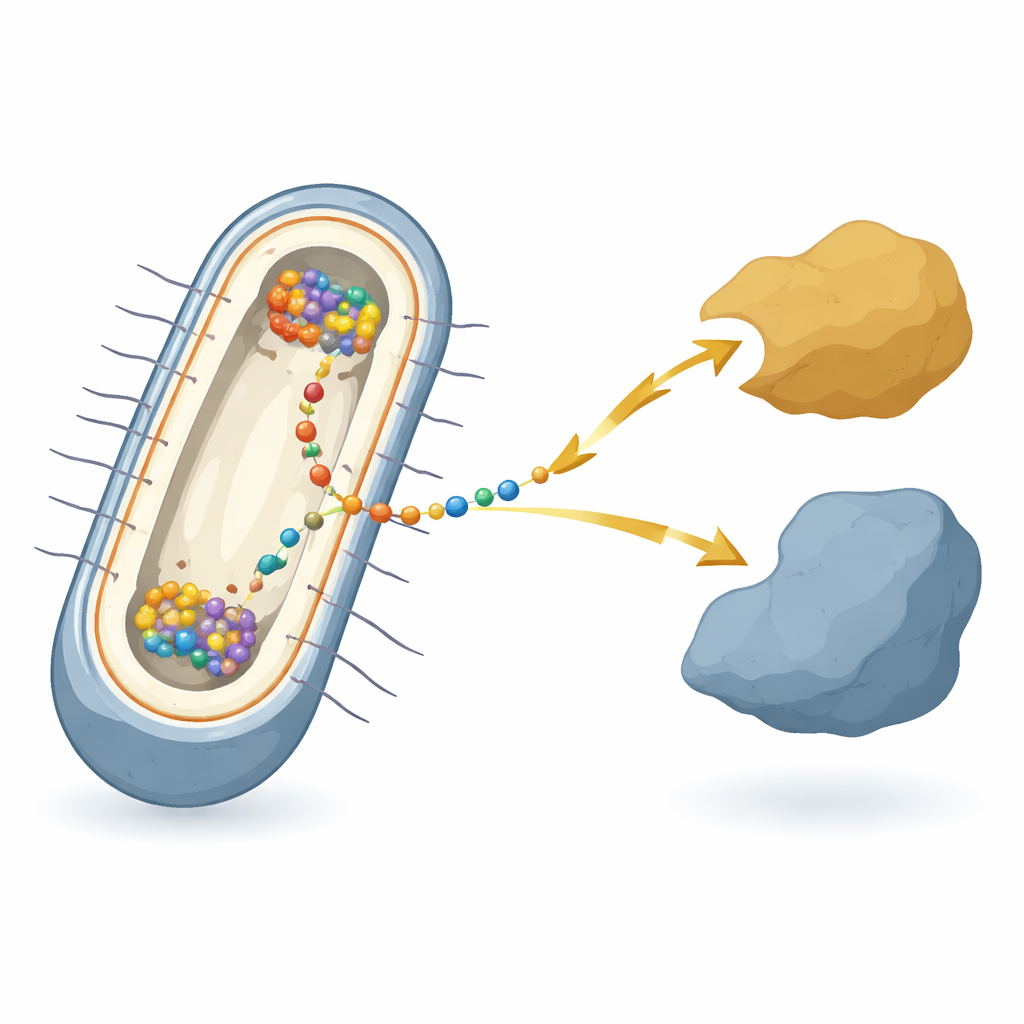
Mikrob żyjący na rdzy i przewodach
Praca koncentruje się na bakterii Shewanella oneidensis, gatunku modelowym znanym z „zewnątrzkomórkowego transferu elektronów” — przekazywania elektronów do lub z metali, minerałów czy elektrod poza komórką. W tych bakteriach elektrony muszą pokonać dwie błony i przestrzeń między nimi, przechodząc przez przekaźnik złożony z wielu różnych białek. W centrum tego przekaźnika, w błonie wewnętrznej, znajduje się białko‑węzeł o nazwie CymA. CymA łączy wewnętrzny metabolizm komórki z białkami transportującymi w przestrzeni periplazmatycznej. Pomimo dekad badań nad poszczególnymi elementami, nie było jasne, jak wszystkie te składniki są skoordynowane w żywej komórce, gdy bakteria rzeczywiście wykonuje to elektryczne „oddychanie”.
Białka samoorganizują się w jasne plamki
Wykorzystując zaawansowaną mikroskopię fluorescencyjną zdolną śledzić pojedyncze białka w pojedynczych komórkach, badacze znakowali CymA świecącymi markerami i obserwowali jego zachowanie w różnych warunkach wzrostu. Gdy bakterie rosły w obecności tlenu, w stanie, w którym CymA jest nieaktywny, białko rozkładało się równomiernie po błonie wewnętrznej. Jednak gdy komórki musiały polegać na zewnątrzkomórkowym transferze elektronów w warunkach beztlenowych, CymA niespodziewanie gromadził się w wyraźne jasne plamki, czyli „punkta”, często w pobliżu biegunów komórki. Ta reorganizacja zachodziła niezależnie od tego, czy elektrony wypływały na zewnątrz do minerałów, czy wpływały do komórki z żelaza lub elektrod. Co ważne, całkowita ilość CymA nie zmieniała się znacznie; zmieniało się jego rozmieszczenie przestrzenne.
Dynamiczne klastry wzmacniają przepływ elektronów
Analiza wielu komórek w czasie wykazała, że tylko część populacji tworzyła klastry CymA w danym momencie, a czas ich powstawania różnił się między komórkami. W poszczególnych komórkach przejście z równomiernego rozkładu do punktów następowało jednak zaskakująco szybko po rozpoczęciu, co sugeruje nagłą wewnętrzną reorganizację po zmiennej zwłoce. Aby sprawdzić, czy te punkta faktycznie wpływają na wydajność elektryczną, badacze połączyli aktywowane światłem elektrody z mikroskopią i zmierzyli maleńkie fotoprądy z pojedynczych komórek. Komórki, które utworzyły punkta CymA, wykazywały istotnie silniejsze przyjmowanie elektronów z elektrody niż te bez punkta, mimo że obie grupy zawierały podobne ilości CymA. To wskazuje, że to zagęszczenie, a nie sama obfitość białka, umożliwia wydajny zewnątrzkomórkowy transfer elektronów.
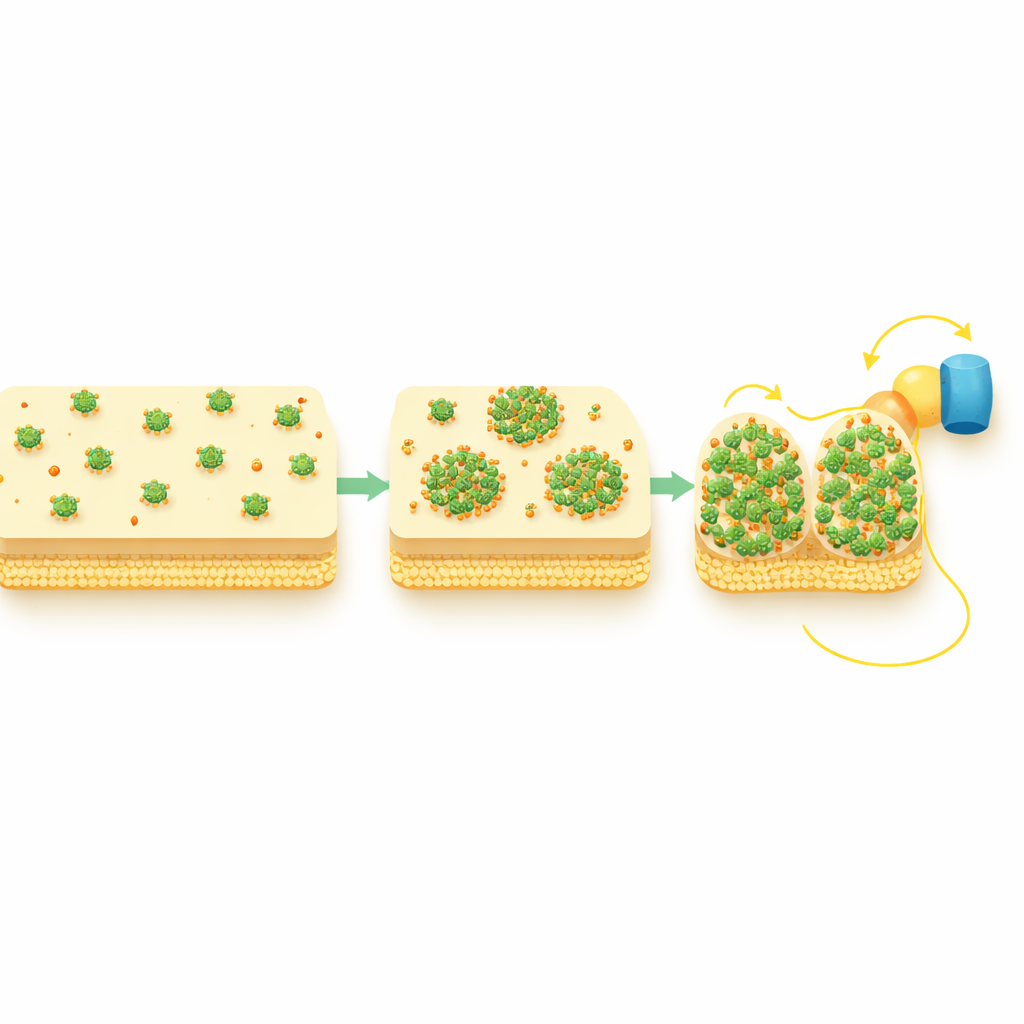
Tworzenie krótszych ścieżek przez osłonę komórkową
Badanie śledziło też dwa periplazmatyczne białka‑przewoźniki, STC i FccA, które bezpośrednio wymieniają elektrony z CymA i przekazują je w kierunku błony zewnętrznej. W warunkach bogatych w tlen te przekaźniki były rozłożone równomiernie, ale podczas aktywnego zewnątrzkomórkowego transferu elektronów również przybierały punktowe wzory i przestrzennie pokrywały się z klastrami CymA. Testy genetyczne wykazały, że to CymA reorganizuje się najpierw, a następnie przyciąga te partnerskie białka, a nie odwrotnie. Innymi słowy, punkta CymA działają jak węzły, które gromadzą downstreamowe przekaźniki w zwarte, intensywnie uczęszczane węzły, skutecznie skracając i wzmacniając szlak elektronowy od wnętrza komórki do jej powierzchni.
Kondensaty o płynnym charakterze napędzane chemią błony
Śledząc pojedyncze cząsteczki CymA, badacze odkryli, że białka wewnątrz punkta pozostawały ruchome i mogły wchodzić oraz wychodzić z klastrów, a same klastry mogły pojawiać się i znikać w zależności od warunków wzrostu. To cechy charakterystyczne „kondensatów biomolekularnych”, kropli o płynnym zachowaniu tworzonych przez zbiory białek i innych molekuł, a nie sztywne kompleksy czy zniszczone agregaty. Pomiary małej błonowej cząsteczki zwanej menachinonem, która przenosi elektrony wewnątrz błony wewnętrznej, wykazały, że jej poziomy rosną równolegle z pojawieniem się punkta CymA. Autorzy proponują, że regiony błony wzbogacone w menachinon działają jak rusztowania rekrutujące CymA do domen przypominających kondensaty, szczególnie w pobliżu biegunów komórki.
Dlaczego to ma znaczenie dla przyrody i technologii
Podsumowując, badanie pokazuje, że Shewanella nie polega wyłącznie na tym, jakie białka wytwarza, aby kontrolować zewnątrzkomórkowy transfer elektronów; ważne jest także to, kiedy i gdzie te białka zbierają się w dynamiczne klastry. Kondensaty CymA, prawdopodobnie zorganizowane przez lokalną chemię błony, przyciągają białka partnerskie, tworząc tymczasowe „elektryczne gorące punkty”, które zwiększają przepływ elektronów przez osłonę komórkową. Dla czytelnika nietechnicznego oznacza to, że nawet bakterie wykorzystują rodzaj samoorganizującego się układu, przestawiając swoje wewnętrzne elementy na żądanie, by podłączyć się do skał, metali czy elektrod. Zrozumienie i w końcu kontrolowanie tego typu samoorganizacji białek może pomóc naukowcom zaprojektować lepsze mikrobowe ogniwa paliwowe, wydajniejsze fabryki bioelektrochemiczne i nowe strategie oczyszczania zanieczyszczeń metalicznych i innych substancji.
Cytowanie: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Słowa kluczowe: zewnątrzkomórkowy transfer elektronów, Shewanella, bioelektryczność bakteryjna, kondensaty biomolekularne, mikrobowe ogniwa paliwowe