Clear Sky Science · pt
Organização espaço-temporal de proteína de membrana controla a transferência extracelular de elétrons bacteriana
Como as bactérias movem eletricidade para fora de suas células
Algumas bactérias conseguem literalmente “respirar” minerais ou eletrodos em vez de oxigênio, movendo pequenas cargas elétricas para dentro e fora de suas células. Esse truque elétrico alimenta sua sobrevivência em ambientes pobres em oxigênio e impulsiona tecnologias como células a combustível microbianas e biorreatores que removem poluentes. O estudo descrito aqui faz uma pergunta aparentemente simples: como as proteínas-chave em uma célula microbiana se organizam no espaço e no tempo para que esse fluxo de elétrons a longa distância funcione de fato?
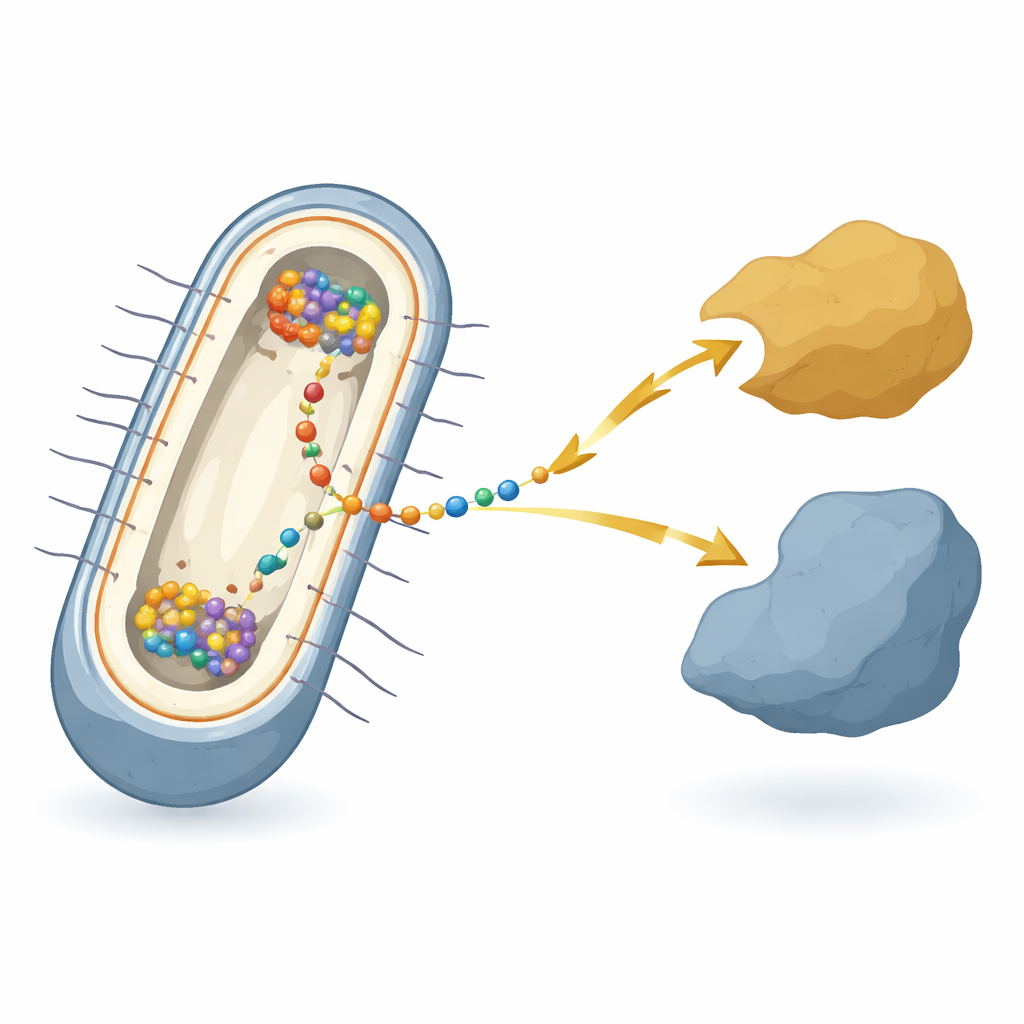
Um micróbio que vive de ferrugem e fios
O trabalho concentra-se na bactéria Shewanella oneidensis, uma espécie-modelo famosa pela “transferência extracelular de elétrons” — entregar elétrons para metais, minerais ou eletrodos fora da célula, ou recebê-los desses componentes. Nessas bactérias, os elétrons precisam atravessar duas membranas e o espaço entre elas, passando por um revezamento de proteínas distintas. No centro desse revezamento, na membrana interna, está uma proteína central chamada CymA. A CymA comunica-se com o metabolismo interno da célula de um lado e com proteínas shuttle no espaço periplasmático do outro. Apesar de décadas de estudos sobre as partes individuais, não estava claro como todos esses componentes se coordenam dentro de cada célula viva quando a bactéria realmente realiza essa respiração elétrica.
Proteínas se auto-organizam em pontos brilhantes
Usando microscopia de fluorescência avançada capaz de rastrear proteínas individuais em células únicas, os pesquisadores marcaram a CymA com marcadores fluorescentes e acompanharam seu comportamento em diferentes condições de crescimento. Quando as bactérias cresciam na presença de oxigênio, um estado em que a CymA fica inativa, a proteína se distribuía uniformemente pela membrana interna. Mas quando as células foram forçadas a depender da transferência extracelular de elétrons em condições sem oxigênio, a CymA surpreendentemente se reuniu em pontos brilhantes distintos, ou “puncta”, frequentemente próximos aos polos celulares. Essa reorganização ocorreu tanto quando elétrons saíam da célula para minerais quanto quando entravam na célula vindos de ferro metálico ou eletrodos. Importante: a quantidade total de CymA não mudou muito; o que mudou foi sua disposição espacial.
Agregados dinâmicos permitem fluxo de elétrons mais forte
Ao observar muitas células ao longo do tempo, a equipe descobriu que apenas uma fração das células formava aglomerados de CymA em qualquer momento, e que o timing variava de célula para célula. Em células individuais, contudo, a transição de uma distribuição uniforme para puncta foi surpreendentemente rápida uma vez iniciada, sugerindo uma reorganização interna súbita após um atraso variável. Para testar se esses puncta realmente importam para o desempenho elétrico, os pesquisadores combinaram eletrodos ativados por luz com microscopia e mediram minúsculas fotocorrentes de células singulares. Células que haviam formado puncta de CymA apresentaram captura de elétrons do eletrodo significativamente maior do que aquelas sem puncta, mesmo que ambos os tipos contivessem quantidades similares de CymA. Isso indica que a agregação, e não apenas a abundância da proteína, é o que permite uma transferência extracelular de elétrons eficiente.
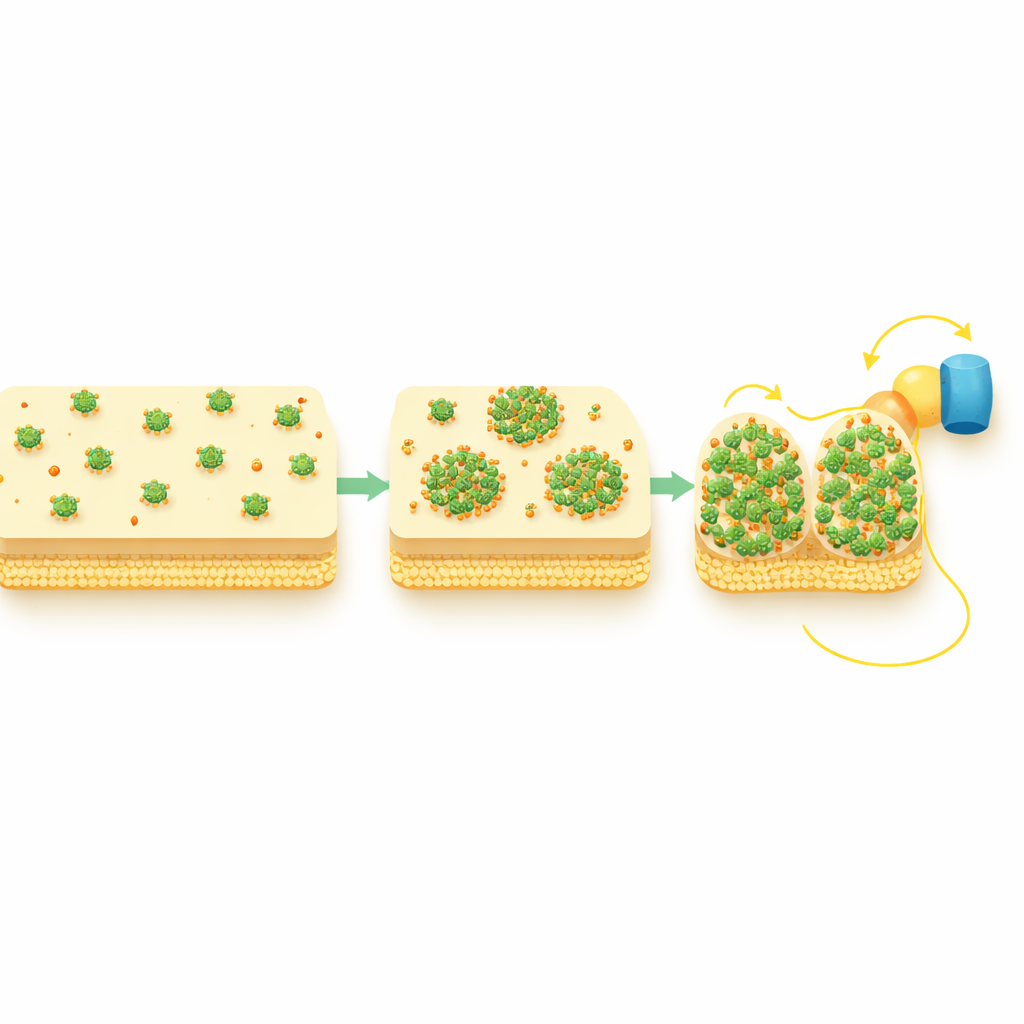
Construindo caminhos mais curtos através do envelope celular
O estudo também acompanhou duas proteínas shuttle periplásmicas, STC e FccA, que trocam elétrons diretamente com a CymA e os passam em direção à membrana externa. Em condições ricas em oxigênio, esses shuttles se distribuíam de maneira uniforme, mas durante a transferência extracelular de elétrons ativa eles também adotaram padrões pontuais e se sobrepuseram espacialmente aos aglomerados de CymA. Testes genéticos mostraram que a CymA se reorganiza primeiro e então atrai esses parceiros, não o contrário. Em outras palavras, os puncta de CymA atuam como pontos centrais que reúnem os shuttles a jusante em junções compactas e de alto tráfego, encurtando e fortalecendo efetivamente a via de elétrons do interior da célula até sua superfície.
Condensados com comportamento líquido impulsionados pela química da membrana
Ao rastrear moléculas individuais de CymA, os pesquisadores descobriram que proteínas dentro dos puncta permaneciam móveis e podiam entrar e sair dos aglomerados, e que os próprios aglomerados podiam aparecer e desaparecer dependendo das condições de crescimento. Esses são sinais característicos de “condensados biomoleculares”, gotículas com comportamento líquido formadas por coleções de proteínas e outras moléculas, em vez de complexos rígidos ou agregados danificados. Medidas de uma pequena molécula de membrana chamada menaquinona, que transporta elétrons dentro da membrana interna, mostraram que seus níveis aumentam em conjunto com o aparecimento dos puncta de CymA. Os autores propõem que regiões da membrana enriquecidas em menaquinona atuam como andaimes que recrutam CymA para domínios semelhantes a condensados, especialmente próximos aos polos celulares.
Por que isso importa para a natureza e para a tecnologia
No geral, o estudo mostra que Shewanella não depende apenas de quais proteínas produz para controlar a transferência extracelular de elétrons; depende também de quando e onde essas proteínas se reúnem em aglomerados dinâmicos. Os condensados de CymA, provavelmente organizados pela química local da membrana, atraem proteínas parceiras para formar “pontos quentes” elétricos temporários que aumentam o fluxo de elétrons através do envelope celular. Para um leitor leigo, isso significa que até as bactérias usam uma espécie de circuitaria auto-montada, reorganizando suas partes internas sob demanda para se conectar a rochas, metais ou eletrodos. Entender e, eventualmente, controlar esse tipo de auto-organização proteica pode ajudar cientistas a projetar células a combustível microbianas melhores, fábricas bioeletroquímicas mais eficientes e novas estratégias para limpar contaminações por metais e poluentes.
Citação: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Palavras-chave: transferência extracelular de elétrons, Shewanella, bioeletricidade bacteriana, condensados biomoleculares, células a combustível microbianas