Clear Sky Science · it
Organizzazione spazio-temporale delle proteine di membrana controlla il trasferimento elettronico extracellulare batterico
Come i batteri spostano l’elettricità fuori dalle loro cellule
Alcuni batteri possono letteralmente “respirare” minerali o elettrodi invece dell’ossigeno, muovendo minuscole cariche elettriche dentro e fuori dalle loro cellule. Questo trucco elettrico alimenta la loro sopravvivenza in ambienti poveri di ossigeno e sostiene tecnologie come le celle a combustibile microbiche e i bioreattori per il trattamento degli inquinanti. Lo studio descritto qui pone una domanda apparentemente semplice: come si dispongono nello spazio e nel tempo le proteine chiave in una cellula microbica affinché questo flusso di elettroni a lunga distanza funzioni davvero?
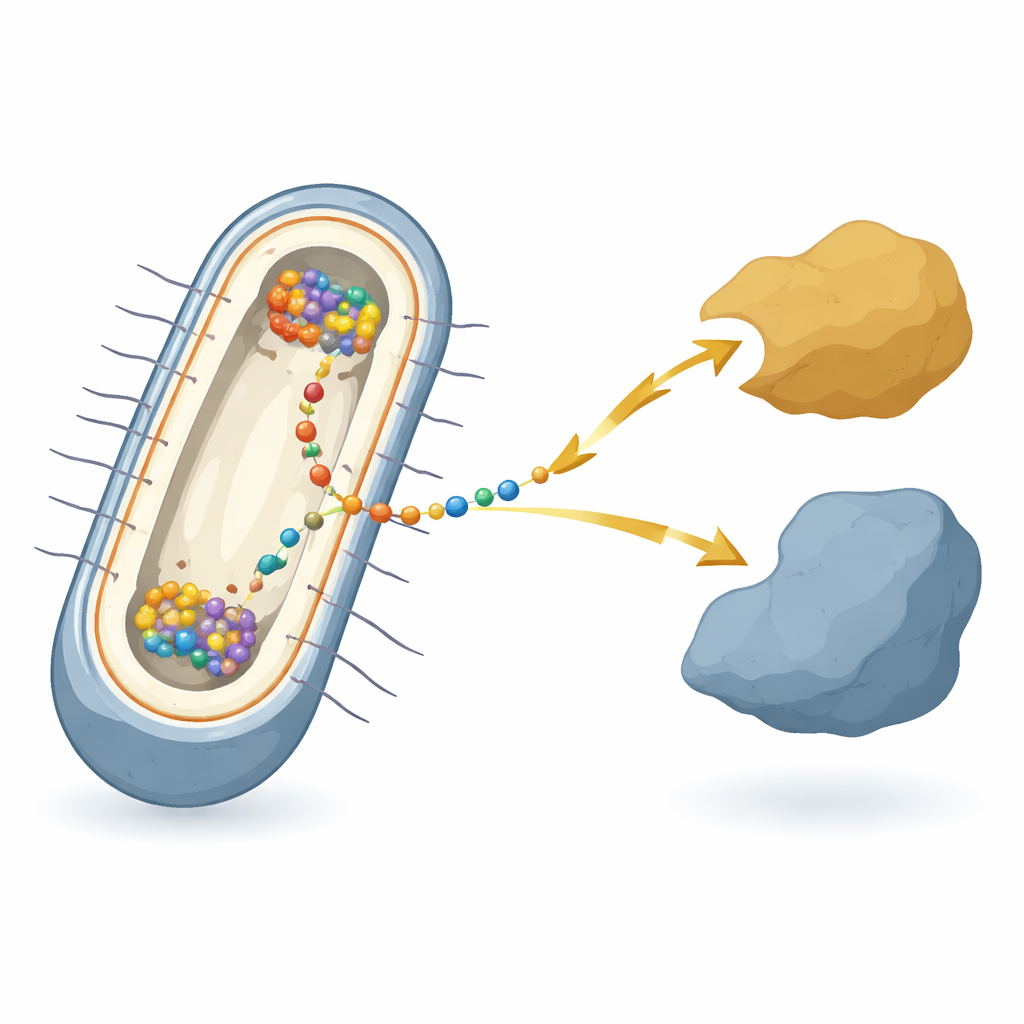
Un microbo che vive di ruggine e fili
Il lavoro si concentra sul batterio Shewanella oneidensis, una specie modello famosa per il “trasferimento elettronico extracellulare” — cedere o ricevere elettroni da metalli, minerali o elettrodi esterni alla cellula. In questi batteri gli elettroni devono attraversare due membrane e lo spazio intermembrana, passando attraverso una staffetta di molte proteine differenti. Al centro di questa staffetta, nella membrana interna, c’è una proteina hub chiamata CymA. CymA comunica da un lato con il metabolismo interno della cellula e dall’altro con proteine shuttle nello spazio periplasmico. Nonostante decenni di studi sulle singole parti, non era chiaro come tutti questi componenti fossero coordinati all’interno di ogni cellula vivente quando il batterio effettua questa respirazione elettrica.
Le proteine si auto-organizzano in punti luminosi
Usando microscopia a fluorescenza avanzata in grado di seguire singole proteine in singole cellule, i ricercatori hanno marcato CymA con indicatori luminosi e osservato il suo comportamento in diverse condizioni di crescita. Quando i batteri crescevano con ossigeno, uno stato in cui CymA è inattiva, la proteina era distribuita in modo uniforme nella membrana interna. Ma quando le cellule sono state costrette a fare affidamento sul trasferimento elettronico extracellulare in assenza di ossigeno, CymA si è riunita inaspettatamente in distinti punti luminosi, o “puncta”, spesso vicino ai poli cellulari. Questa riorganizzazione avveniva sia quando gli elettroni uscivano dalla cellula verso i minerali sia quando entravano nella cellula da ferro metallico o elettrodi. È importante notare che la quantità totale di CymA non cambiava molto; ciò che cambiava era la sua disposizione spaziale.
Cluster dinamici favoriscono un flusso elettronico più intenso
Osservando molte cellule nel tempo, il team ha scoperto che solo una frazione delle cellule formava cluster di CymA in un dato momento e che i tempi variavano da cellula a cellula. Nelle singole cellule, tuttavia, la transizione da una distribuzione uniforme ai puncta era sorprendentemente rapida una volta avviata, suggerendo una riorganizzazione interna improvvisa dopo un ritardo variabile. Per verificare se questi puncta avessero un effetto sulle prestazioni elettriche, i ricercatori hanno combinato elettrodi attivati dalla luce con la microscopia e misurato minuscole foto-correnti da singole cellule. Le cellule che avevano formato puncta di CymA mostravano un assorbimento di elettroni dall’elettrodo significativamente più elevato rispetto a quelle senza puncta, anche se entrambi i tipi contenevano quantità simili di CymA. Questo indica che è il clustering, non la semplice abbondanza proteica, a rendere efficiente il trasferimento elettronico extracellulare.
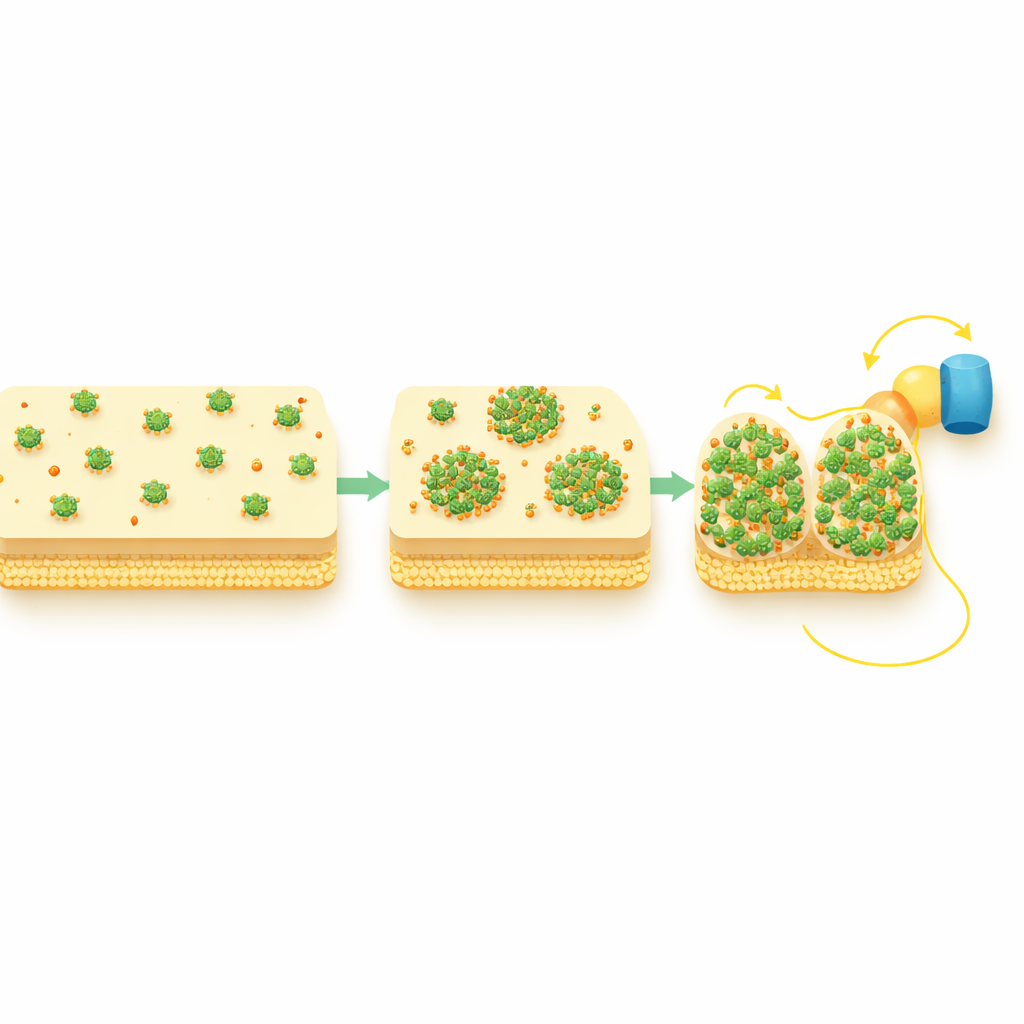
Costruire percorsi più corti attraverso l’involucro cellulare
Lo studio ha seguito anche due proteine shuttle periplasmiche, STC e FccA, che scambiano elettroni direttamente con CymA e li trasferiscono verso la membrana esterna. In condizioni ricche di ossigeno questi shuttle erano distribuiti uniformemente, ma durante il trasferimento elettronico extracellulare attivo hanno adottato anch’essi pattern puntiformi e si sono sovrapposti spazialmente ai cluster di CymA. Test genetici hanno mostrato che CymA si riorganizza per prima e poi richiama questi partner, non il contrario. In altre parole, i puncta di CymA funzionano come hub che raccolgono gli shuttle a valle in giunzioni compatte ad alto traffico, accorciando e rafforzando efficacemente il percorso elettronico dall’interno della cellula alla sua superficie.
Condensati di tipo liquido guidati dalla chimica della membrana
Tracciando singole molecole di CymA, i ricercatori hanno scoperto che le proteine all’interno dei puncta restavano mobili e potevano entrare e uscire dai cluster, e che gli stessi cluster potevano apparire e scomparire a seconda delle condizioni di crescita. Questi sono segni distintivi dei “condensati biomolecolari”, goccioline di tipo liquido formate da collezioni di proteine e altre molecole piuttosto che da complessi rigidi o aggregati danneggiati. Misurazioni di una piccola molecola di membrana chiamata menaquinone, che trasporta elettroni all’interno della membrana interna, hanno mostrato che i suoi livelli aumentano in concomitanza con l’apparizione dei puncta di CymA. Gli autori propongono che regioni di membrana arricchite di menaquinone agiscano come impalcature che reclutano CymA in domini simili a condensati, specialmente vicino ai poli cellulari.
Perché questo è importante per la natura e la tecnologia
Complessivamente, lo studio mostra che Shewanella non si affida solo a quali proteine produce per controllare il trasferimento elettronico extracellulare; dipende anche da quando e dove queste proteine si raccolgono in cluster dinamici. I condensati di CymA, verosimilmente organizzati dalla chimica locale della membrana, richiamano le proteine partner per formare temporanee “zone elettriche calde” che potenziano il flusso di elettroni attraverso l’involucro cellulare. Per un lettore non specialista, questo significa che anche i batteri usano una sorta di circuiteria auto-assemblata, riordinando le loro parti interne su richiesta per collegarsi a rocce, metalli o elettrodi. Capire e alla fine indirizzare questo tipo di auto-organizzazione proteica potrebbe aiutare gli scienziati a progettare celle a combustibile microbiche più efficienti, impianti bioelettrochimici migliori e nuove strategie per bonificare metalli e inquinanti.
Citazione: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Parole chiave: trasferimento elettronico extracellulare, Shewanella, bioelettricità batterica, condensati biomolecolari, celle a combustibile microbiche