Clear Sky Science · sv
Spatiotemporal organisation av membranprotein styr bakteriell extracellulär elektronöverföring
Hur bakterier förflyttar elektricitet utanför sina celler
Vissa bakterier kan bokstavligen andas mineraler eller elektroder istället för syre och därigenom flytta små elektriska laddningar in och ut ur sina celler. Denna elektriska förmåga håller dem vid liv i syrefattiga miljöer och driver tekniker som mikrobiella bränsleceller och bioreaktorer som renar föroreningar. Studien som beskrivs här ställer en bedrägligt enkel fråga: hur organiserar sig de centrala proteinerna i en mikrobiell cell i tid och rum så att denna långdistans elektronflöde faktiskt fungerar?
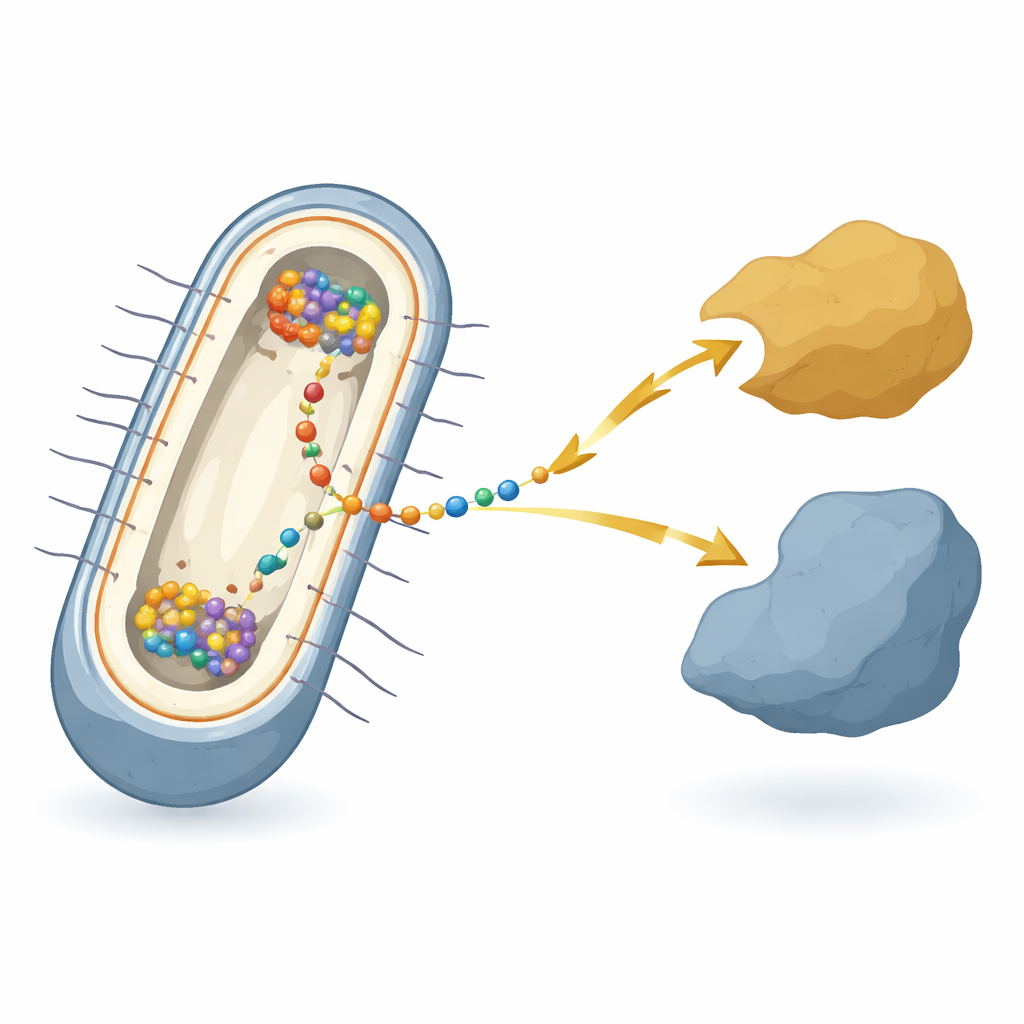
En mikroorganism som lever på rost och ledningar
Arbetet fokuserar på bakterien Shewanella oneidensis, en modellart känd för ”extracellulär elektronöverföring” — att överföra elektroner till eller från metaller, mineraler eller elektroder utanför cellen. I dessa bakterier måste elektronerna korsa två membran och ett mellanrum däremellan, och de passerar genom en relay av många olika proteiner. I centrum av denna relay, i det inre membranet, sitter ett navprotein som kallas CymA. CymA kommunicerar med cellens inre metabolism på ena sidan och med transportproteiner i utrymmet mellan membranen på andra sidan. Trots årtionden av arbete med de enskilda delarna har det varit oklart hur alla dessa komponenter samordnas inne i varje levande cell när bakterien verkligen utför denna elektriska respiration.
Proteiner självorganiserar till ljusa punkter
Med hjälp av avancerad fluorescensmikroskopi som kan följa enskilda proteiner i enskilda celler märkte forskarna CymA med lysande markörer och följde dess beteende under olika odlingsförhållanden. När bakterierna växte med syre, ett tillstånd där CymA är inaktivt, spreds proteinet jämnt runt det inre membranet. Men när cellerna tvingades förlita sig på extracellulär elektronöverföring under syrefria förhållanden samlades CymA oväntat i distinkta ljusa fläckar, eller ”punkta”, ofta nära cellpolerna. Denna omorganisation skedde oavsett om elektroner flödade ut ur cellen till mineraler eller in i cellen från järn eller elektroder. Viktigt är att den totala mängden CymA inte förändrades mycket; det som förändrades var dess rumsliga fördelning.
Dynamiska kluster möjliggör starkare elektronflöde
Genom att studera många celler över tid fann teamet att endast en delmängd av cellerna bildade CymA-kluster vid en given tidpunkt, och att tidpunkten varierade från cell till cell. I enskilda celler var övergången från en jämn fördelning till punkta förvånansvärt snabb när den väl satte igång, vilket tyder på en plötslig intern omorganisation efter en variabel fördröjning. För att testa om dessa punkta verkligen påverkar den elektriska prestationen kombinerade forskarna ljusaktiverade elektroder med mikroskopi och mätte små fotoströmmar från individuella celler. Celler som hade bildat CymA-punkta visade avsevärt starkare elektronupptag från elektroden än de utan punkta, även om båda typerna innehöll liknande mängder CymA. Detta indikerar att klustring — inte endast proteinnivå — möjliggör effektiv extracellulär elektronöverföring.
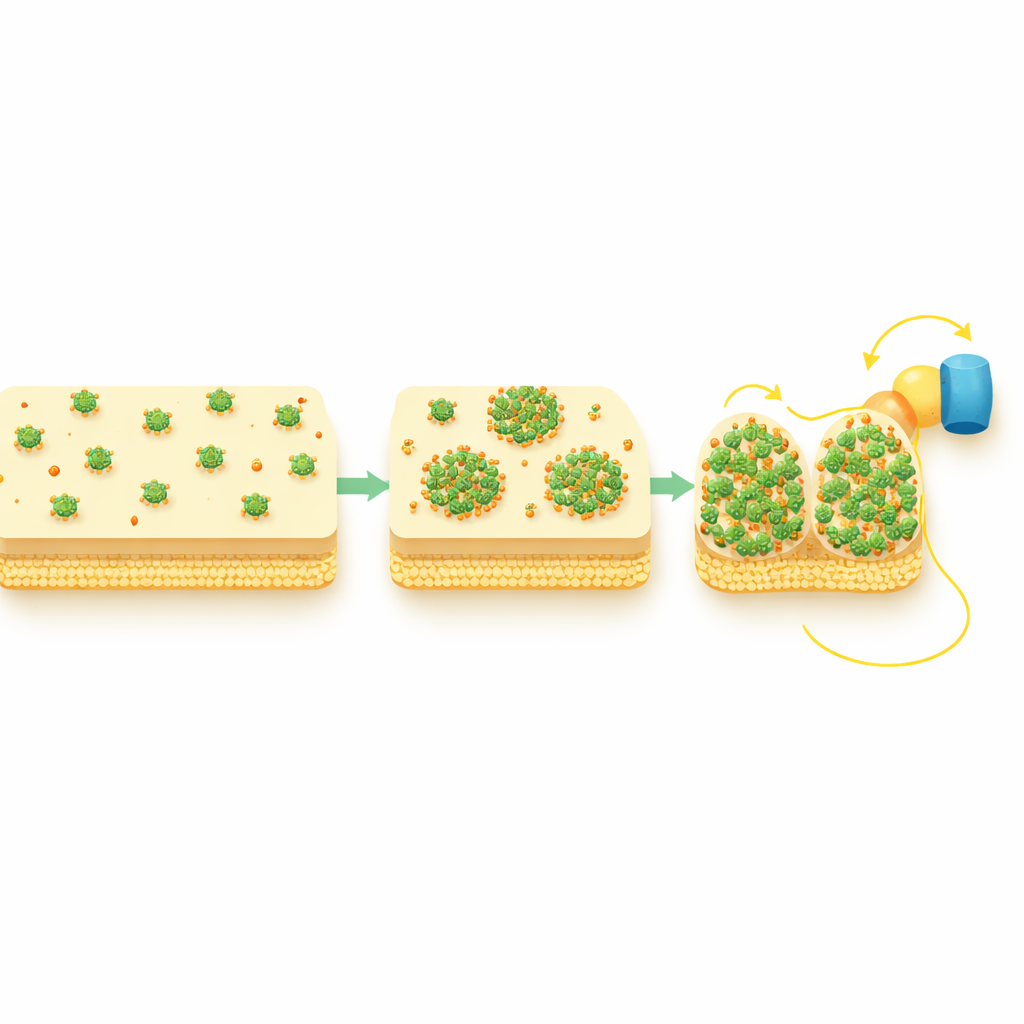
Bygga kortare vägar över cellemembranet
Studien följde också två periplasmatiska transportproteiner, STC och FccA, som direkt utbyter elektroner med CymA och för dem vidare mot det yttre membranet. Under syresatta förhållanden var dessa transportörer jämnt fördelade, men under aktiv extracellulär elektronöverföring antar de också punktvisa mönster och överlappar rumsligt med CymA-kluster. Genetiska tester visade att CymA omorganiserar först och därefter drar till sig dessa partners, inte tvärtom. Med andra ord fungerar CymA-punkta som nav som samlar de nedströms transporterna i kompakta, högtrafikerade knutpunkter och förkortar och förstärker därigenom elektronvägen från cellens inre till dess yta.
Vätskeliknande kondensat drivna av membrankemi
Genom att spåra enskilda CymA-molekyler upptäckte forskarna att proteiner inom punkta förblev rörliga och kunde röra sig in och ut ur klustren, och att klustren själva kunde dyka upp och försvinna beroende på odlingsförhållanden. Detta är kännetecken för ”biomolekylära kondensat”, vätskeliknande droppar bildade av samlingar av proteiner och andra molekyler snarare än av styva komplex eller skadade aggregat. Mätningar av en liten membranmolekyl kallad menakinon, som transporterar elektroner i det inre membranet, visade att dess nivåer ökar i takt med att CymA-punkta uppträder. Författarna föreslår att membranområden som är berikade på menakinon fungerar som ställningar som rekryterar CymA till kondensatlika domäner, särskilt nära cellpolerna.
Varför detta spelar roll för natur och teknik
Sammanfattningsvis visar studien att Shewanella inte enbart förlitar sig på vilka proteiner den producerar för att kontrollera extracellulär elektronöverföring; den är också beroende av när och var dessa proteiner samlas i dynamiska kluster. CymA-kondensat, sannolikt organiserade av lokal membrankemi, drar till sig partnerproteiner för att bilda temporära ”elektriska hetpunkter” som ökar elektronflödet över cellemembranet. För en lekmannaläsare innebär detta att även bakterier använder en form av självmonterad kretsdesign, där de omarrangerar sina inre delar på begäran för att koppla in sig mot berg, metaller eller elektroder. Att förstå och så småningom styra denna typ av proteinernas självorganisation kan hjälpa forskare att utforma bättre mikrobiella bränsleceller, mer effektiva bioelektrokemiska fabriker och nya strategier för att sanera metall- och föroreningsproblem.
Citering: Park, Y., Yan, T., Zhao, Z. et al. Spatiotemporal organization of membrane protein controls bacterial extracellular electron transfer. Nat Commun 17, 2855 (2026). https://doi.org/10.1038/s41467-026-69655-y
Nyckelord: extracellulär elektronöverföring, Shewanella, bakteriell bioelektricitet, biomolekylära kondensat, mikrobiella bränsleceller