Clear Sky Science · zh
簇聚与构象开关驱动哺乳动物受体酪氨酸激酶 ROS1 的激活
为什么这对健康与癌症重要
许多癌症劫持了健康细胞用于生长与发育的相同通讯系统。其中一个系统以一种名为 ROS1 的表面蛋白为中心,该蛋白帮助控制组织发育,但在被误用时也能驱动肿瘤。直到现在,科学家们仍不清楚天然因子如何激活 ROS1,或如何用现代药物将其关闭。本研究既揭示了长期寻找的 ROS1 触发因子,又提供了其工作机制的详细图景,为针对依赖该分子的癌症开辟了新治疗路径。
一个长期神秘的细胞“天线”
ROS1 属于一大类被称为受体酪氨酸激酶的细胞“天线”。这类蛋白穿越细胞膜:外部区域感知信号,而内部区域传递指令,告诉细胞生长、分裂或分化。ROS1 在该家族中较为特殊,具有最大且最复杂的外部结构之一,几十年来没人知道它识别的天然信号是什么。然而,ROS1 在多种肿瘤中出现,要么以已知的、可作为药物靶点的异常基因融合形式存在,要么以全长蛋白在脑、肺、口腔及部分乳腺癌中高表达。由于现有药物主要针对内部的酶活性位点,研究者希望理解外部结构能够激发出更具选择性和持久性的抗体疗法。
找到并证明缺失的信号
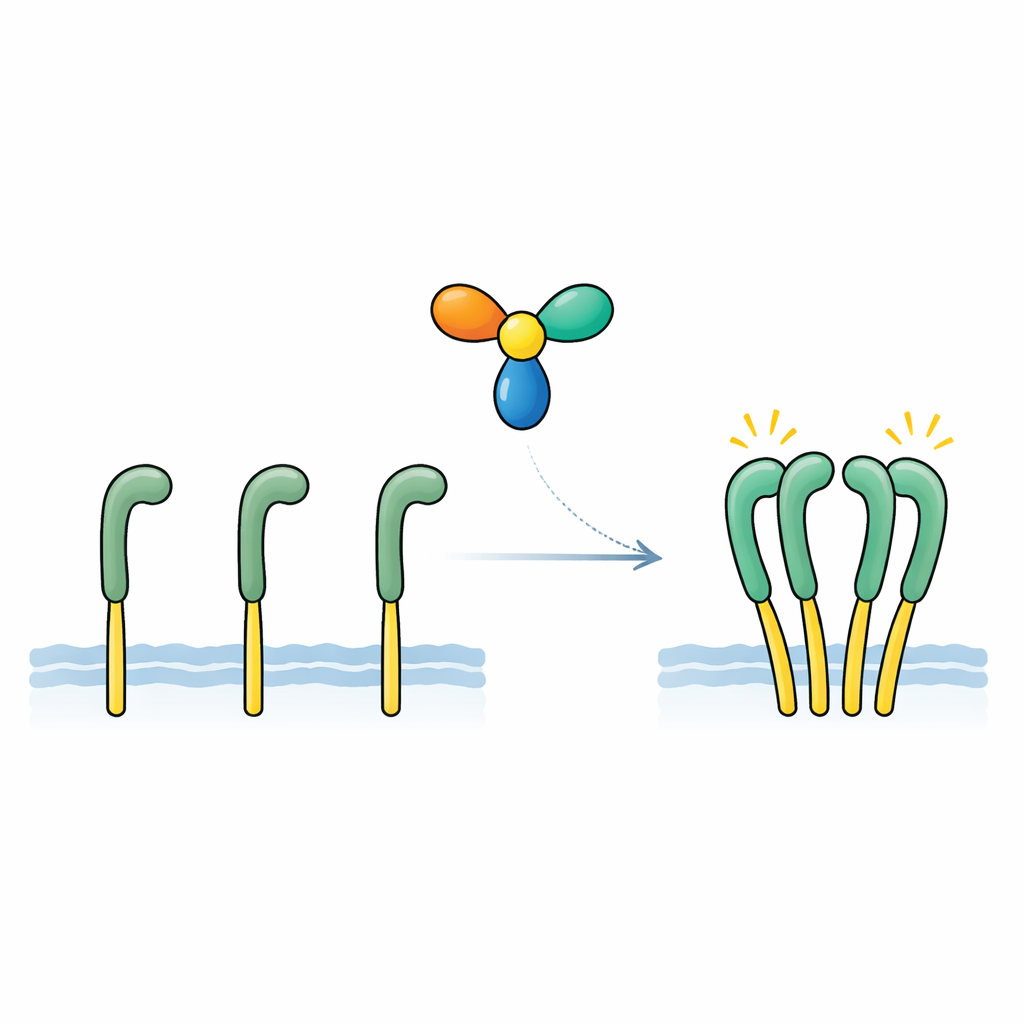
团队把注意力集中在一种名为 NELL2 的分泌蛋白上,该蛋白先前与神经发育以及 ROS1 在雄性生育中的作用有关。通过灵敏的结合测定,他们证明 NELL2 能直接且紧密地附着在 ROS1 的外部区域,其亲和力可与经典生长因子与受体相媲美。在携带基于 ROS1 的测试受体的工程细胞中,加入 NELL2 会强烈增强受体内侧的化学“开启”标记,并激活下游信号通路。被迫形成单体的改造版 NELL2 虽然仍能结合 ROS1,但不再能激活它。这揭示了两个关键点:NELL2 是 ROS1 的真正激活信号,且其形成多单元复合体的能力对将受体切换到活性状态至关重要。
解锁活性的构象变化
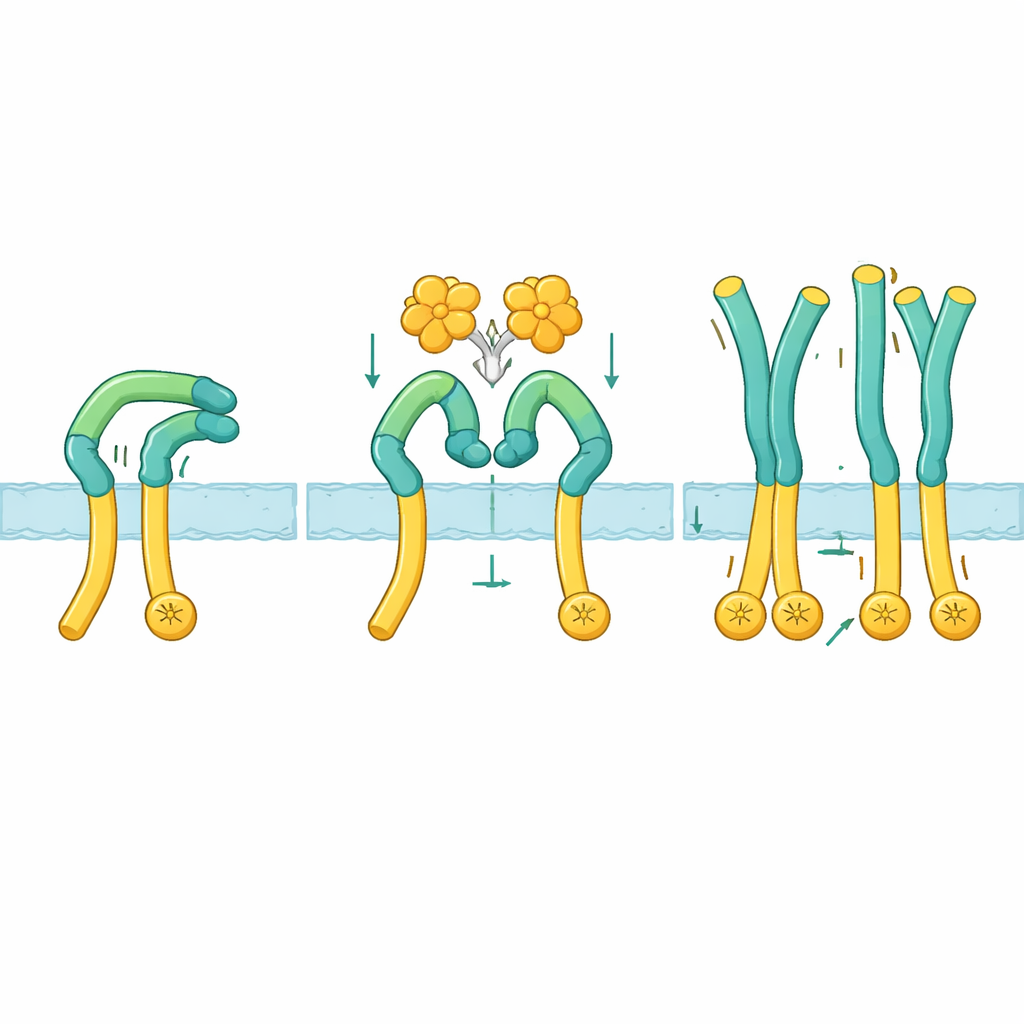
为了观察这一激活过程的实际机制,研究者使用冷冻电镜可视化了独立的 ROS1 外部结构以及与 NELL2 结合时的复合体。在静息状态下,ROS1 自身折叠回去:上部的“臂”弯下并夹在通向细胞膜的长“腿”上。这个弯曲构象使下部保持刚性,并似乎使内部酶端相互之间太远而无法相互作用。当 NELL2 结合时,它抓牢了 ROS1 臂部上跨越多个结构域的三个不同位点。这种结合不仅使多个 ROS1 分子聚集在一起,还将臂从腿上拽开,并将其旋转约130度,变为更直立的姿态。一旦这个夹持被释放,腿段变得柔性,靠近膜的区域以及因此内部酶部分就能彼此接近并相互激活。
把结构学见解转化为药物候选者
基于这些接近原子级别的形态图谱,作者随后使用抗体展示文库筛选出能黏附 ROS1 外部区域的人工抗体。他们发现了两类不同的抗体。一种抗体精确结合在 NELL2 首次停靠的位置,物理阻断配体并阻止激活。第二类抗体楔入臂与 ROS1 中央枢纽之间的裂缝,稳定原本弯曲、被夹持的构象。这两类抗体都能有效关闭细胞中 ROS1 驱动的信号传导,尽管从原理上它们的两个臂可能会将受体聚集在一起。这表明简单的聚集并不足以激活:激活绝对依赖于 NELL2 所诱导的构象变化,使腿段自由并允许内部酶相互接近。
这对未来癌症疗法意味着什么
这项工作揭示了 ROS1 受双重安全机制控制:受体必须由多单元信号拉拢在一起,同时还必须经历释放内部制动的重大构象变化。NELL2 同时提供了这两种功能,而新发现的抗体则选择性地干扰初始的抓握或解锁动作。对于非专业读者,结论是科学家们终于找到了 ROS1 的天然开关,并已几乎逐个原子地绘制出它如何将关闭状态转为开启状态的过程。这些见解为下一代生物制剂药物奠定了基础,未来有望在不干扰其他细胞开关的情况下,特异性地在肿瘤中沉默 ROS1。
引用: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
关键词: ROS1 受体, 受体酪氨酸激酶, 癌症信号传导, NELL2 配体, 治疗性抗体