Clear Sky Science · fr
Le regroupement et un commutateur conformationnel induisent l’activation de la tyrosine kinase réceptrice ROS1 chez les mammifères
Pourquoi c’est important pour la santé et le cancer
De nombreux cancers détournent les mêmes systèmes de communication que les cellules saines utilisent pour croître et se développer. L’un de ces systèmes repose sur une protéine de surface nommée ROS1, qui aide à contrôler le développement tissulaire mais peut aussi provoquer des tumeurs lorsqu’elle est mal utilisée. Jusqu’ici, les chercheurs ignoraient quel signal naturel active ROS1, ou comment l’inhiber avec des médicaments modernes. Cette étude révèle à la fois le longuement recherché déclencheur de ROS1 et une description détaillée de son fonctionnement, ouvrant de nouvelles pistes pour traiter les cancers qui dépendent de cette molécule.
Une antenne cellulaire longtemps mystérieuse
ROS1 appartient à une grande famille d’« antennes » cellulaires connues sous le nom de tyrosine kinases réceptrices. Ces protéines traversent la membrane cellulaire : une portion externe détecte les signaux, tandis qu’une portion interne relaie des messages indiquant à la cellule de croître, de se diviser ou de se spécialiser. ROS1 est atypique au sein de cette famille. Il possède l’une des régions externes les plus larges et les plus élaborées, et pendant des décennies personne n’a su quel signal naturel il reconnaissait. Pourtant ROS1 apparaît dans de nombreuses tumeurs, soit sous forme de fusions géniques anormales déjà ciblées par des médicaments, soit sous forme de protéine pleine longueur présente à de forts niveaux dans certains cancers du cerveau, du poumon, de la cavité buccale et du sein. Comme les traitements actuels ciblent principalement la portion enzymatique interne, les chercheurs espéraient que comprendre la région externe pourrait inspirer des thérapies par anticorps plus sélectives et durables.
Identifier et prouver le signal manquant
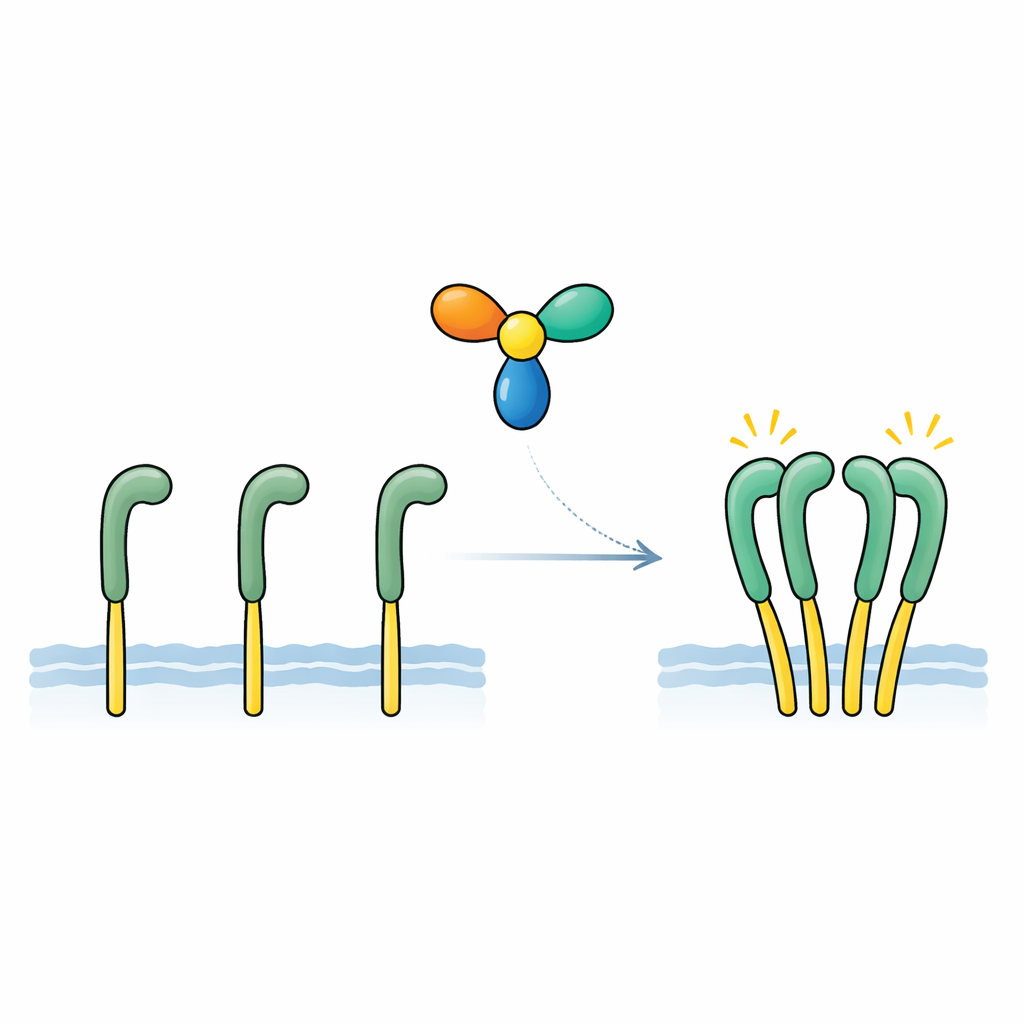
L’équipe s’est concentrée sur une protéine sécrétée appelée NELL2, précédemment associée au développement nerveux et au rôle de ROS1 dans la fertilité masculine. À l’aide de mesures de liaison sensibles, ils ont montré que NELL2 se fixe directement et fortement à la portion externe de ROS1, avec une affinité comparable à celle des facteurs de croissance classiques et de leurs récepteurs. Dans des cellules modifiées portant un récepteur-test basé sur ROS1, l’ajout de NELL2 augmentait fortement les marques chimiques « activatrices » sur la face interne du récepteur et activait les voies de signalisation en aval. Une version modifiée de NELL2, contrainte en forme monomérique, pouvait toujours se lier à ROS1 mais ne l’activait plus. Cela a révélé deux points clés : NELL2 est un signal activateur authentique pour ROS1, et sa capacité à former un complexe multi‑unités est essentielle pour commuter le récepteur vers un état actif.
Un changement de forme qui débloque l’activité
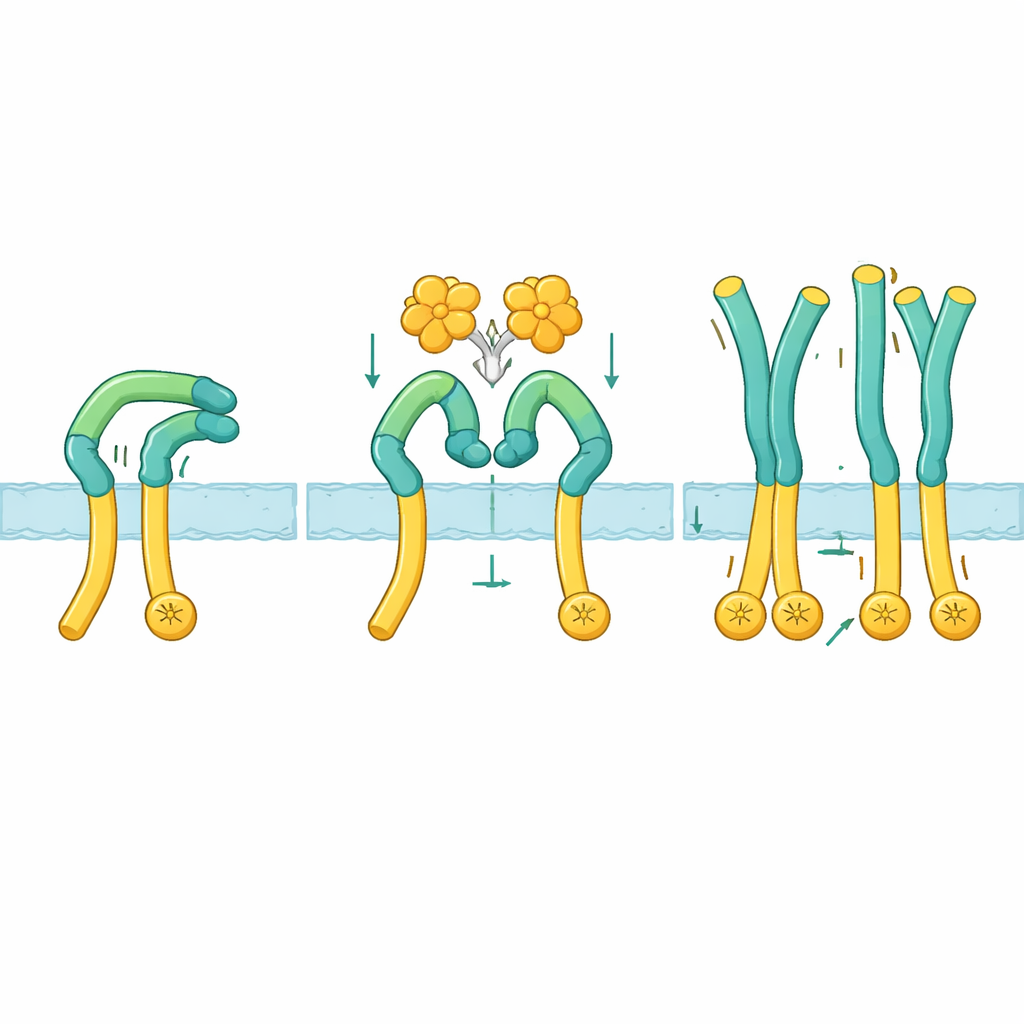
Pour comprendre comment cette activation fonctionne réellement, les chercheurs ont utilisé la cryo‑microscopie électronique pour visualiser la région externe de ROS1 seule et en complexe avec NELL2. À l’état au repos, ROS1 se replie sur lui‑même : une portion « bras » supérieure se courbe vers le bas et s’appuie contre une longue « jambe » qui mène vers la membrane cellulaire. Cette posture repliée maintient la partie inférieure rigide et semble maintenir les extrémités enzymatiques internes trop éloignées pour communiquer. Lorsque NELL2 se lie, il saisit trois endroits différents répartis sur plusieurs domaines du bras de ROS1. Cette liaison non seulement regroupe plusieurs molécules de ROS1, mais elle écarte aussi le bras de la jambe et le fait pivoter d’environ 130 degrés vers une position plus dressée. Une fois ce verrou relâché, le segment de la jambe devient flexible, permettant aux régions proches de la membrane, et donc aux parties enzymatiques internes, de se rapprocher suffisamment pour s’activer mutuellement.
Transformer l’information structurale en candidats médicaments
Dotés de cartes quasi atomiques de ces conformations, les auteurs ont ensuite utilisé des bibliothèques d’affichage d’anticorps pour identifier des anticorps de laboratoire qui se fixent à la région externe de ROS1. Ils ont découvert deux types distincts. Un anticorps se lie précisément à l’endroit où NELL2 s’amarre en premier, bloquant physiquement le ligand et empêchant l’activation. Un second anticorps s’insère dans la fente entre le bras et le noyau central de ROS1, stabilisant la conformation repliée et verrouillée d’origine. Les deux anticorps inhibent puissamment la signalisation induite par ROS1 dans les cellules, bien que, en principe, leurs deux bras pourraient rapprocher les récepteurs. Cela montre que le simple regroupement n’est pas suffisant : l’activation nécessite absolument le changement de conformation induit par NELL2 qui libère la jambe et permet aux enzymes internes de se rencontrer.
Ce que cela signifie pour les futures thérapies contre le cancer
Ce travail révèle que ROS1 est contrôlé par un système de sécurité en deux étapes : les récepteurs doivent être rapprochés par un signal multi‑unités et doivent aussi subir un important changement de forme qui libère un frein interne. NELL2 assure ces deux fonctions, tandis que les anticorps nouvellement découverts interfèrent sélectivement soit avec l’accrochage initial, soit avec le mouvement de déverrouillage. Pour les lecteurs non spécialistes, la conclusion est que les scientifiques ont enfin identifié un commutateur naturel pour ROS1 et ont cartographié, presque atome par atome, comment il transforme un état « éteint » en un état « allumé ». Ces connaissances jettent les bases de médicaments biologiques de nouvelle génération qui pourraient spécifiquement faire taire ROS1 dans les tumeurs, tout en laissant intacts d’autres interrupteurs cellulaires.
Citation: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Mots-clés: récepteur ROS1, tyrosine kinase réceptrice, signalisation du cancer, ligand NELL2, anticorps thérapeutiques