Clear Sky Science · tr
Kümelenme ve konformasyonel bir anahtar, memeli reseptör tirozin kinazı ROS1’in aktivasyonunu tetikliyor
Sağlık ve kanser açısından neden önemli
Birçok kanser, sağlıklı hücrelerin büyüme ve gelişme için kullandığı aynı iletişim sistemlerini ele geçirir. Bu sistemlerden biri, doku gelişimini kontrol etmeye yardımcı olan ancak kötüye kullanıldığında tümörleri tetikleyebilen yüzey proteini ROS1 etrafında döner. Bugüne dek bilim insanları ROS1’i doğal olarak neyin açtığını ya da modern ilaçlarla nasıl kapatılacağını bilmiyordu. Bu çalışma hem uzun süredir aranan ROS1 tetikleyicisini hem de onun nasıl çalıştığına dair ayrıntılı bir resmi ortaya koyarak, bu moleküre bağımlı kanserleri tedavi etmek için yeni yollar açıyor.
Uzun zamandır gizemli bir hücresel anten
ROS1, reseptör tirozin kinazlar olarak bilinen büyük bir hücre “anten” ailesine aittir. Bu proteinler hücre zarını geçer: dış kısmı sinyalleri algılar, iç kısmı ise hücreye büyüme, bölünme veya farklılaşma talimatı veren mesajları iletir. ROS1 bu aile içinde sıra dışıdır. En dış bölgelerinden biri en büyük ve en karmaşık olanlardandır ve on yıllarca hangi doğal sinyali tanıdığı bilinmemiştir. Buna karşın ROS1 birçok tümörde görülür; ya halihazırda ilaç hedefi olan anormal gen füzyonları şeklinde ya da beyin, akciğer, ağız ve bazı meme kanserlerinde yüksek düzeyde bulunan tam boy proteine olarak. Mevcut ilaçlar ağırlıklı olarak içteki enzim bölümünü hedeflediğinden, araştırmacılar dış bölümün anlaşılmasının daha seçici ve dayanıklı antikor terapilerine ilham verebileceğini umuyorlardı.
Eksik sinyali bulmak ve kanıtlamak
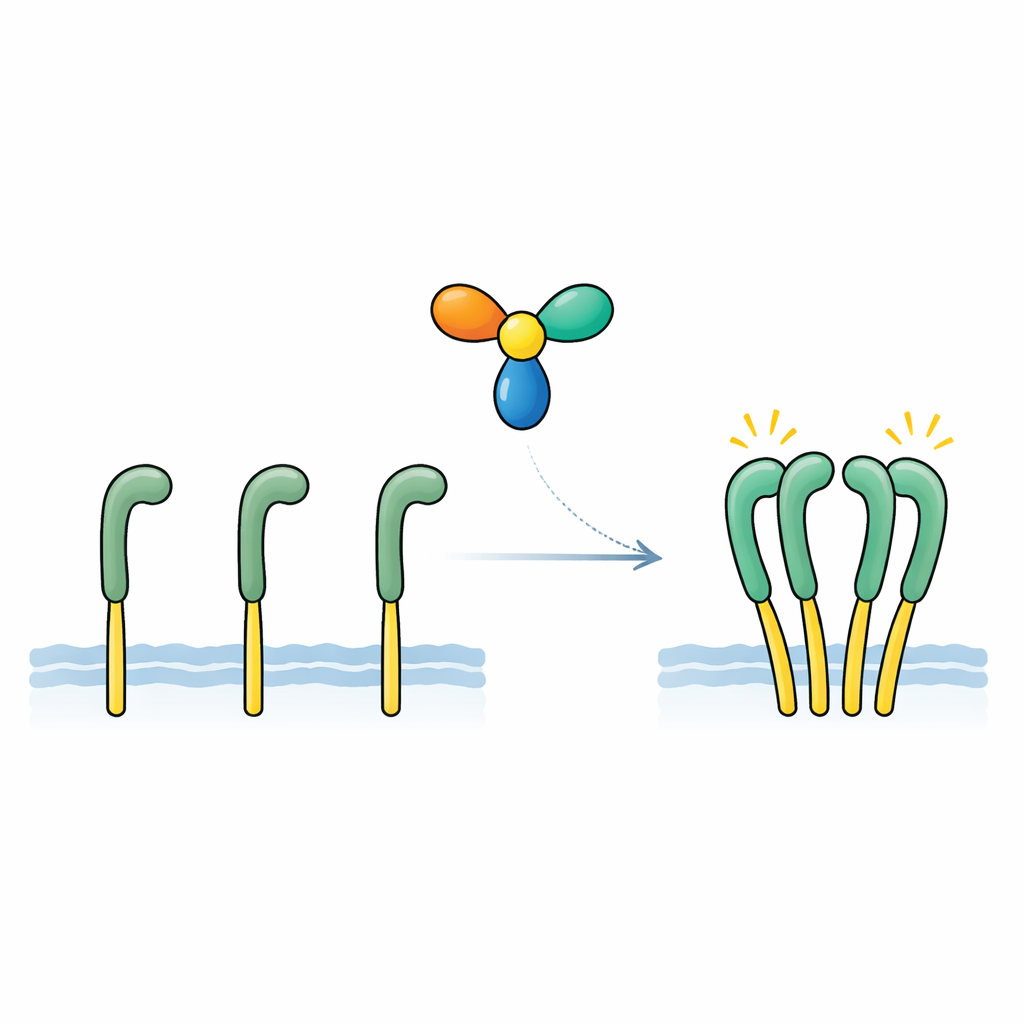
Araştırma ekibi, daha önce sinir gelişimi ve ROS1’in erkek fertliliğindeki rolüyle ilişkilendirilmiş salgılanan bir protein olan NELL2’ye odaklandı. Hassas bağlanma ölçümleri kullanarak NELL2’nin ROS1’in dış bölümüne doğrudan ve sıkı bağlandığını, bağlanma afinitesinin klasik büyüme faktörleri ile onların reseptörlerine benzer olduğunu gösterdiler. ROS1 tabanlı bir test reseptörü taşıyan mühendislenmiş hücrelere NELL2 eklendiğinde, reseptörün iç yüzündeki kimyasal “açık” işaretler güçlü şekilde arttı ve aşağı akış sinyal yolları aktifleşti. Tek birim halinde zorlanmış modifiye edilmiş bir NELL2 sürümü hâlâ ROS1’e bağlanabiliyordu ama artık onu aktifleştiremiyordu. Bu, iki önemli noktayı ortaya koydu: NELL2 gerçek bir ROS1 aktivasyon sinyalidir ve çok birimli kompleks oluşturma yeteneği, reseptörü aktif duruma geçirmek için esastır.
Aktiviteyi açan şekil değişimi
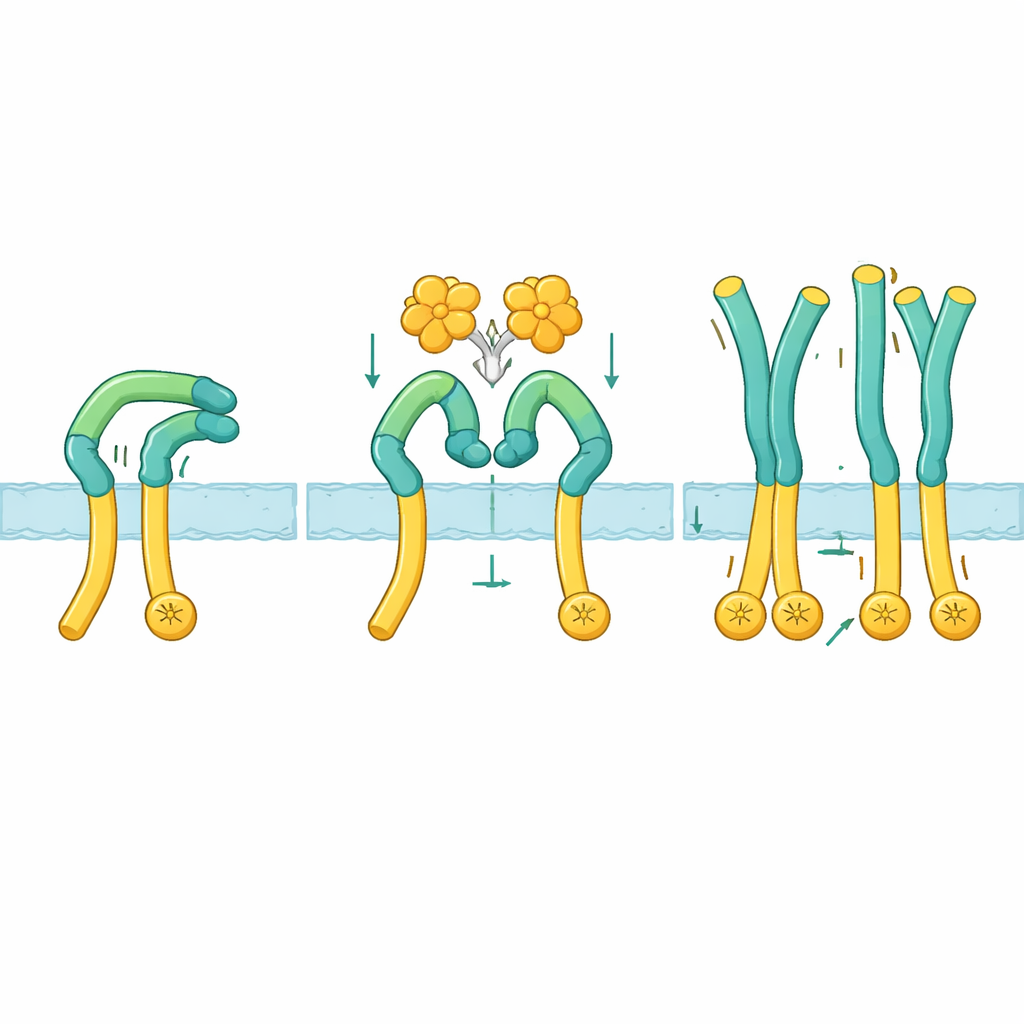
Bu aktivasyonun gerçekte nasıl işlediğini görmek için araştırmacılar ROS1’in dış bölgesini tek başına ve NELL2 ile kompleks halinde görselleştirmek üzere kriyo-elektron mikroskopisi kullandılar. Dinlenme halinde ROS1 kendine doğru katlanır: üst “kol” bölümü aşağı doğru bükülür ve hücre zarına doğru giden uzun bir “bacak” ile kavrama yapar. Bu bükülmüş duruş, alt kısmı rijit tutar ve içteki enzim uçlarını birbirleriyle iletişim kuramayacak kadar uzakta tutuyor gibi görünür. NELL2 bağlandığında, ROS1 kolu üzerindeki birkaç domain boyunca üç farklı noktayı kavrar. Bu bağlanma sadece birden çok ROS1 molekülünü kümelendirmekle kalmaz, aynı zamanda kolu bacaktan ayırır ve yaklaşık 130 derece döndürerek daha dik bir pozisyona getirir. Bu kelepçe serbest bırakıldığında bacak segmenti esnek hale gelir; bu da zar yakınındaki bölgelerin ve dolayısıyla içteki enzim parçalarının birbirine yaklaşarak birbirlerini aktifleştirmesine olanak tanır.
Yapısal bulguyu ilaç adaylarına dönüştürme
Bu şekillerin atom düzeyindeki haritalarıyla donanmış olarak, yazarlar ROS1’in dış bölgesine yapışan laboratuvarda üretilmiş antikorları bulmak için antikor-görüntüleme kütüphanelerini kullandılar. İki farklı tip keşfettiler. Bir antikor, NELL2’nin ilk bağlandığı noktaya tam olarak tutunuyor, ligandı fiziksel olarak engelliyor ve aktivasyonu önlüyor. İkinci bir antikor ise kol ile ROS1’in merkezsel gövdesi arasındaki yarığa girerek orijinal bükülmüş, kelepçelenmiş konformasyonu stabilize ediyor. Her iki antikor da hücrelerde ROS1 kaynaklı sinyalleşmeyi güçlü biçimde kapattı; ilginç olan, teoride her iki antikorun iki kolu reseptörleri bir araya getirebilecekken bunu yapmalarına rağmen aktivasyonu engellemiş olmalarıdır. Bu, basit kümelenmenin yeterli olmadığını gösterir: aktivasyon, bacağı serbest bırakıp iç enzimlerin bir araya gelmesine izin veren NELL2 kaynaklı şekil değişimini kesinlikle gerektirir.
Geleceğin kanser terapileri için ne anlama geliyor
Bu çalışma, ROS1’in iki aşamalı bir güvenlik sistemiyle kontrol edildiğini ortaya koyuyor: reseptörlerin çok birimli bir sinyal tarafından bir araya çekilmesi ve içteki frenin serbest bırakılması için büyük bir şekil değişikliğinden geçmesi gerekir. NELL2 her iki işlevi de sağlar; yeni keşfedilen antikorlar ise ya ilk kavrayışı ya da kilidi açan hareketi seçici olarak engeller. Uzman olmayan okuyucular için çıkarım şudur: bilim insanları sonunda ROS1 için doğal bir anahtar tanımladı ve kapalı durumdan açık duruma geçişin nasıl olduğunu neredeyse atom atom haritaladılar. Bu bulgular, diğer hücresel anahtarları bozmadan tümörlerdeki ROS1’i özgün biçimde susturabilecek yeni nesil biyolojik ilaçların geliştirilmesi için zemin hazırlar.
Atıf: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Anahtar kelimeler: ROS1 reseptörü, reseptör tirozin kinaz, kanser sinyalleşmesi, NELL2 ligandı, terapötik antikorlar