Clear Sky Science · pl
Grupowanie i przełączenie konformacyjne napędzają aktywację receptorowej kinazy tyrozynowej ROS1 u ssaków
Dlaczego to ma znaczenie dla zdrowia i onkologii
Wiele nowotworów przejmuje te same systemy komunikacji, których zdrowe komórki używają do wzrostu i rozwoju. Jednym z takich systemów jest białko powierzchniowe o nazwie ROS1, które pomaga kontrolować rozwój tkanek, ale może też napędzać guzy, gdy zostanie wykorzystane w niewłaściwy sposób. Do tej pory naukowcy nie wiedzieli, co naturalnie włącza ROS1 ani jak skutecznie go wyłączyć za pomocą współczesnych leków. To badanie ujawnia zarówno długo poszukiwany czynnik uruchamiający ROS1, jak i szczegółowy obraz jego działania, otwierając nowe drogi leczenia nowotworów zależnych od tego białka.
Długo zagadkowa antena komórkowa
ROS1 należy do dużej rodziny komórkowych „anten” znanych jako receptorowe kinazy tyrozynowe. Białka te przechodzą przez błonę komórkową: zewnętrzna część odbiera sygnały, a wewnętrzna przekazuje komunikaty, które mówią komórce, by rosła, dzieliła się lub różnicowała. ROS1 jest w tej rodzinie nietypowy. Ma jedną z największych i najbardziej rozbudowanych części zewnętrznych i przez dekady nikt nie znał naturalnego sygnału, który rozpoznaje. Tymczasem ROS1 pojawia się w wielu nowotworach — jako nieprawidłowe fuzyjne geny będące już celami leków lub jako pełnej długości białko występujące w podwyższonych ilościach w raku mózgu, płuca, jamy ustnej i niektórych typach raka piersi. Ponieważ istniejące leki głównie celują w wewnętrzną, enzymatyczną część, badacze liczyli, że poznanie zewnętrznej domeny zainspiruje terapie przeciwciałowe, które będą bardziej selektywne i trwałe.
Odnalezienie i potwierdzenie brakującego sygnału
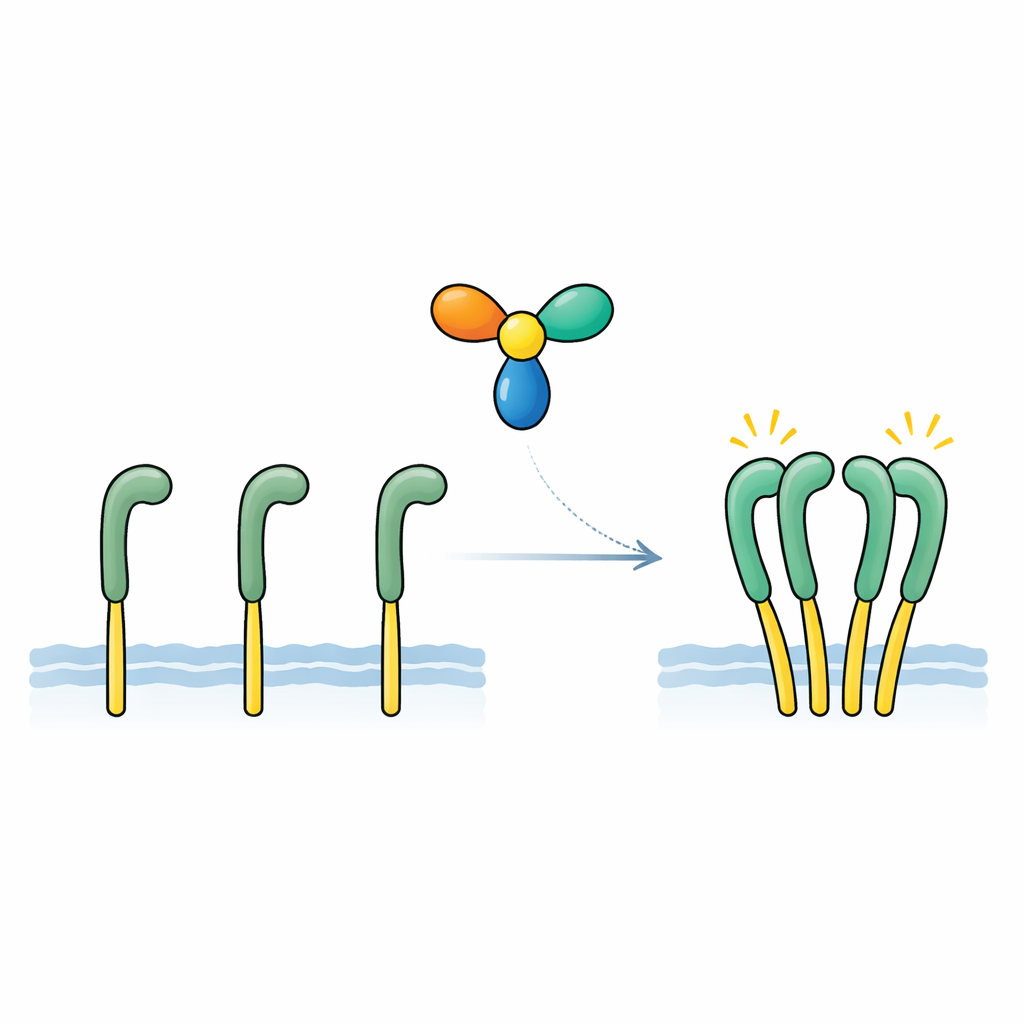
Zespół skupił się na wydzielanym białku o nazwie NELL2, wcześniej powiązanym z rozwojem nerwów i rolą ROS1 w męskiej płodności. Przy użyciu czułych pomiarów wiązania wykazali, że NELL2 przyłącza się bezpośrednio i silnie do zewnętrznej części ROS1, z powinowactwem podobnym do klasycznych czynników wzrostu i ich receptorów. W komórkach inżynieryjnych niosących receptor testowy oparty na ROS1, dodanie NELL2 silnie zwiększało chemiczne znaczniki „włączenia” po wewnętrznej stronie receptora i aktywowało szlaki sygnałowe poniżej. Zmodyfikowana wersja NELL2 przymuszona do jednoczynnikowej formy nadal mogła wiązać ROS1, ale przestała go aktywować. To ujawniło dwie kluczowe kwestie: NELL2 jest rzeczywistym, aktywującym sygnałem dla ROS1, a jej zdolność do tworzenia kompleksu wielojednostkowego jest niezbędna do przełączenia receptora w stan aktywny.
Zmiana kształtu uwalniająca aktywność
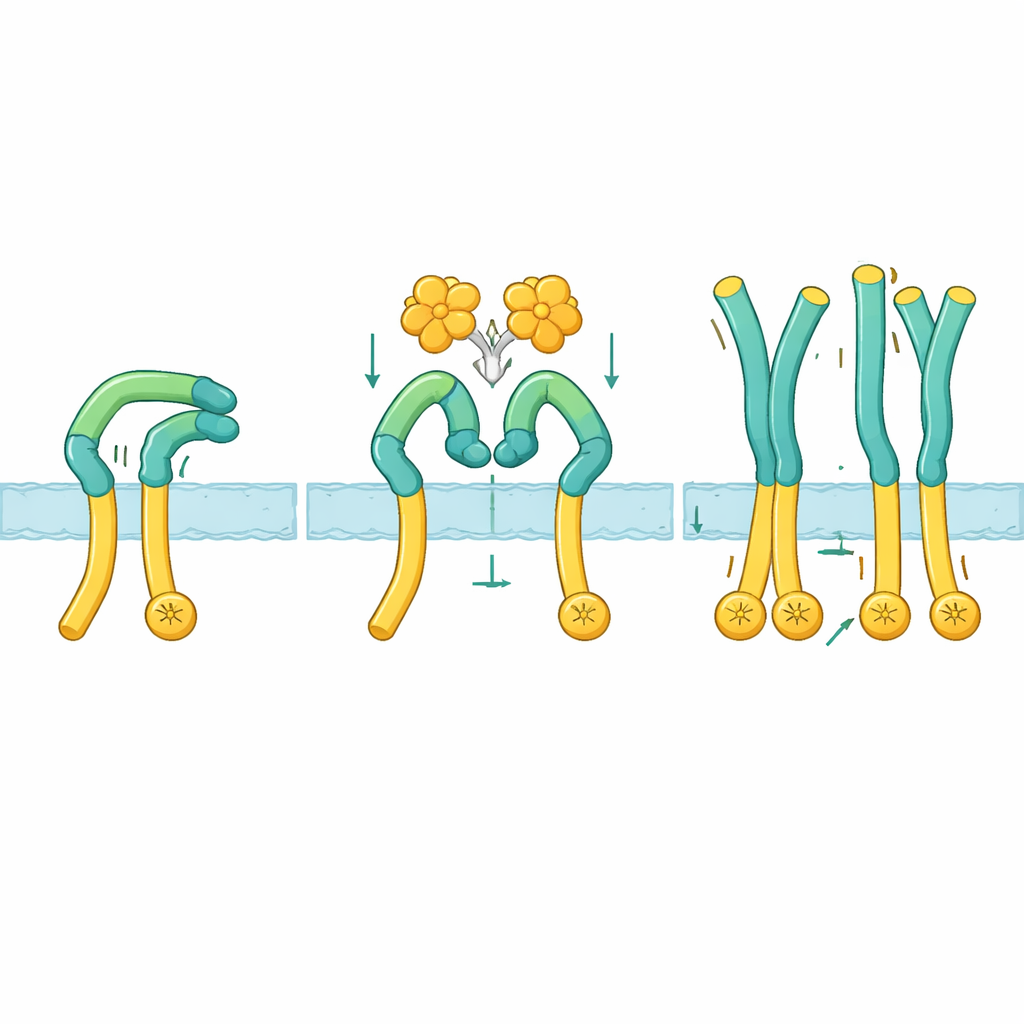
Aby zobaczyć, jak ta aktywacja działa w praktyce, badacze użyli kriomikroskopii elektronowej do zobrazowania samej zewnętrznej domeny ROS1 oraz kompleksu z NELL2. W stanie spoczynkowym ROS1 składa się jakby z powrotem na siebie: górna „ramię” zgina się w dół i zaciska na długiej „nodze” prowadzącej w kierunku błony komórkowej. Taka zgięta pozycja sztywnie utrzymuje dolną część i wydaje się zbyt mocno rozdzielać wewnętrzne końce enzymatyczne, uniemożliwiając ich komunikację. Gdy NELL2 wiąże się, obejmuje trzy różne miejsca na kilku domenach ramienia ROS1. To wiązanie nie tylko grupuje wiele cząsteczek ROS1 razem, ale też odciąga ramię od nogi i obraca je o około 130 stopni do bardziej pionowej pozycji. Gdy zacisk zostaje zwolniony, segment nogi staje się elastyczny, pozwalając obszarom przybliżonym do błony, a więc i wewnętrznym częściom enzymatycznym, zbliżyć się na tyle, by się nawzajem aktywować.
Zamiana wglądu strukturalnego na kandydatów leków
Posiadając mapy na poziomie atomowym tych kształtów, autorzy użyli bibliotek ekspresji przeciwciał, by odnaleźć laboratoryjnie wytworzone przeciwciała wiążące zewnętrzną część ROS1. Odkryli dwa odrębne typy. Jedno przeciwciało wiąże się precyzyjnie tam, gdzie NELL2 najpierw dokuje, fizycznie blokując ligand i zapobiegając aktywacji. Drugie przeciwciało klinuje się w szczelinie między ramieniem a centralnym rdzeniem ROS1, stabilizując pierwotną zgiętą, zaciskającą konformację. Oba przeciwciała silnie wygaszają sygnalizację napędzaną przez ROS1 w komórkach, mimo że teoretycznie ich dwa ramiona mogłyby ściągać receptory razem. Pokazuje to, że samo grupowanie nie wystarcza: aktywacja absolutnie wymaga zmiany kształtu wywołanej przez NELL2, która uwalnia nogę i pozwala wewnętrznym enzymom się spotkać.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Praca ta ujawnia, że ROS1 jest kontrolowany przez dwustopniowy system bezpieczeństwa: receptory muszą zostać zbliżone przez sygnał wielojednostkowy i jednocześnie muszą przejść znaczną zmianę konformacyjną, która zwalnia wewnętrzny hamulec. NELL2 zapewnia obie funkcje, podczas gdy nowo odkryte przeciwciała selektywnie ingerują albo w początkowy chwyt, albo w ruch „odblokowujący”. Dla czytelników bez specjalistycznego przygotowania kluczowy wniosek jest taki, że naukowcy wreszcie zidentyfikowali naturalny przełącznik dla ROS1 i odwzorowali, niemal atom po atomie, jak zamienia on stan wyłączony w włączony. Te spostrzeżenia tworzą podstawę dla leków biologicznych nowej generacji, które mogłyby specyficznie uciszyć ROS1 w guzach, nie zaburzając innych komórkowych przełączników.
Cytowanie: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Słowa kluczowe: receptor ROS1, receptorowa kinaza tyrozynowa, sygnalizacja nowotworowa, ligand NELL2, przeciwciała terapeutyczne