Clear Sky Science · sv
Klustring och en konformationsväxling driver aktivering av den däggdjurska receptor-tyrosinkinasen ROS1
Varför detta är viktigt för hälsa och cancer
Många cancerformer kapar samma kommunikationssystem som friska celler använder för att växa och utvecklas. Ett sådant system kretsar kring ett ytmolekyl kallat ROS1, som hjälper till att reglera vävnadsutveckling men som också kan driva tumörer när det missbrukas. Fram till nu visste forskare inte vad som naturligt slår på ROS1, eller hur man kan stänga av det med moderna läkemedel. Denna studie avslöjar både den länge eftersökta utlösaren för ROS1 och en detaljerad bild av hur den fungerar, vilket öppnar nya vägar för behandling av cancerformer som är beroende av detta protein.
En länge gåtfull cellantenn
ROS1 tillhör en stor familj av cellens "antenner" som kallas receptor-tyrosinkinaser. Dessa proteiner sträcker sig genom cellmembranet: en yttre del känner av signaler, medan en inre del förmedlar budskap som säger åt cellen att växa, dela sig eller specialisera sig. ROS1 är ovanlig inom denna familj. Den har en av de största och mest invecklade yttre regionerna, och i årtionden visste ingen vilken naturlig signal den kände igen. Ändå förekommer ROS1 i många tumörer, antingen som onormala genfusioner som redan är läkemedelsmål, eller som fullängdsprotein funnet i höga nivåer i hjärn-, lunga-, mun- och vissa bröstcancer. Eftersom befintliga läkemedel främst riktar sig mot den inre enzymdelen hoppades forskarna att förståelsen av den yttre delen kunde inspirera antikroppsbehandlingar som är mer selektiva och långvariga.
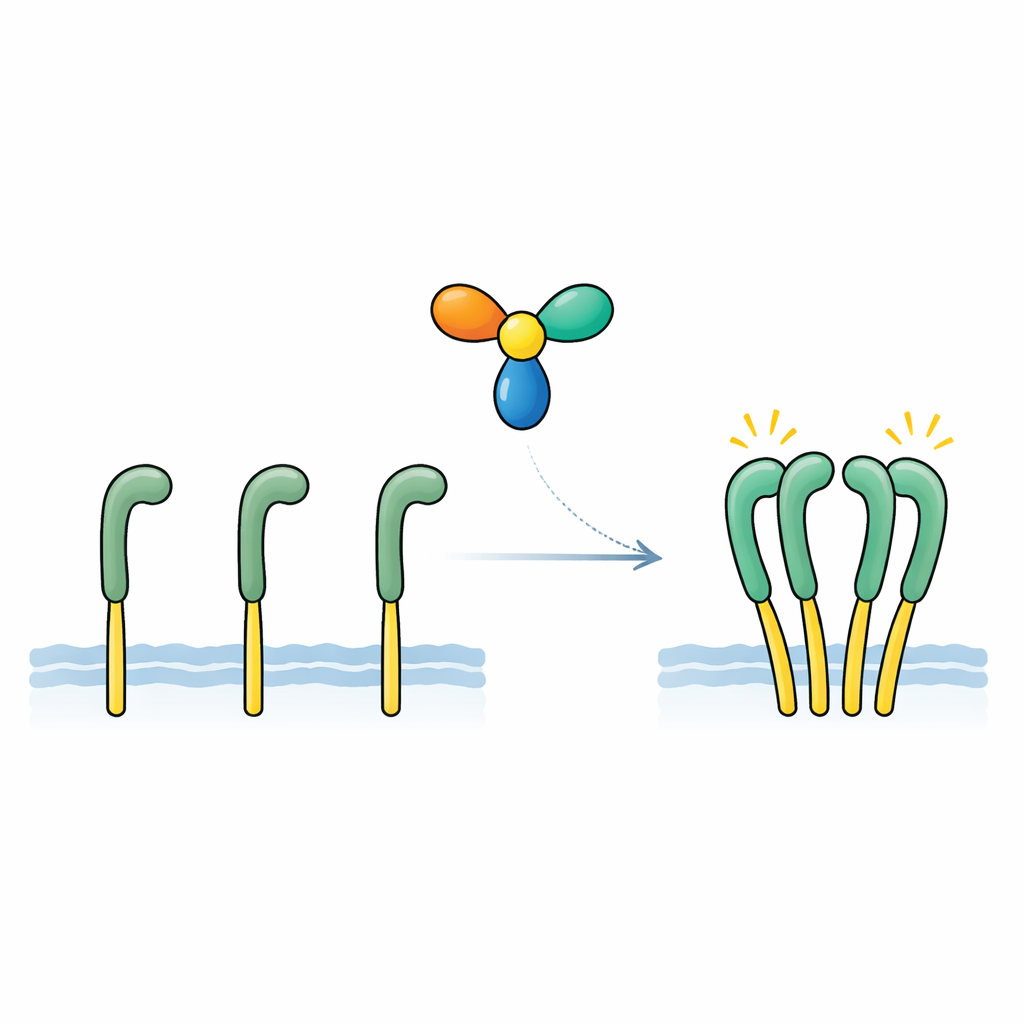
Att hitta och bevisa den saknade signalen
Forskargruppen fokuserade på ett utsöndrat protein kallat NELL2, tidigare kopplat till nervutveckling och till ROS1:s roll i manlig fertilitet. Med känsliga bindningsmätningar visade de att NELL2 fäster direkt och tätt vid ROS1:s yttre del, med en affinitet som liknar klassiska tillväxtfaktorer och deras receptorer. I konstruerade celler med en ROS1-baserad testreceptor gav tillsatt NELL2 en kraftig ökning av de kemiska "på"-märkena på receptorernas insida och aktiverade nedströms signalvägar. En modifierad version av NELL2 som hade tvingats till en enhetsform kunde fortfarande binda ROS1 men aktiverade det inte längre. Detta avslöjade två viktiga punkter: NELL2 är en äkta aktiverande signal för ROS1, och dess förmåga att bilda ett mångenhetskomplex är avgörande för att slå över receptorn till ett aktivt tillstånd.
En formförändring som frigör aktivitet
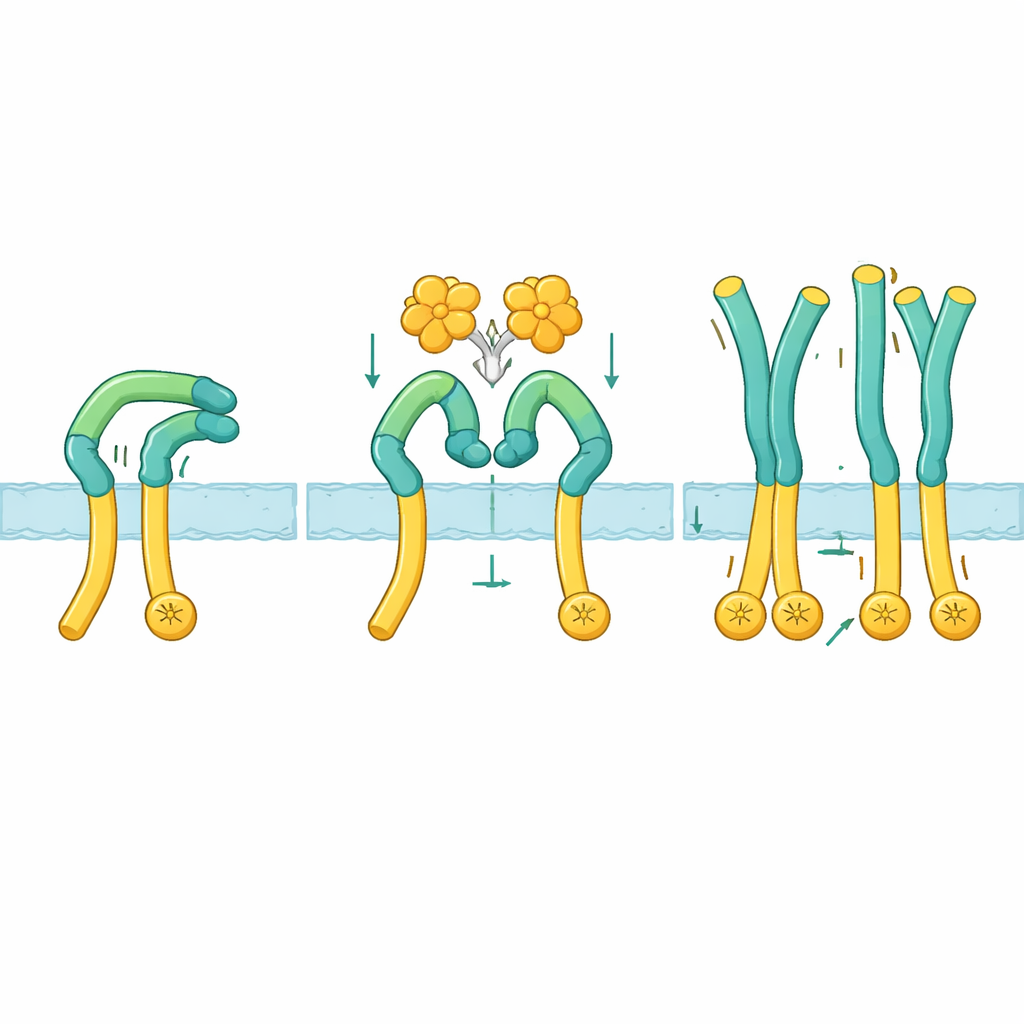
För att se hur denna aktivering faktiskt fungerar använde forskarna kryo-elektronmikroskopi för att visualisera ROS1:s yttre region ensam och i komplex med NELL2. I vilotillståndet viker ROS1 tillbaka över sig själv: en övre "arm" böjer sig ned och klämmer mot ett långt "ben" som leder mot cellmembranet. Denna böjda hållning håller den nedre delen styv och verkar hålla de inre enzymändarna för långt ifrån varandra för att kommunicera. När NELL2 binder, greppar den tre olika platser över flera domäner på ROS1-armen. Denna bindning klustrar inte bara flera ROS1-molekyler tillsammans, utan bryter också armens grepp om benet och roterar den med ungefär 130 grader till en mer upprätt position. När detta klämmande frigörs blir bensegmentet flexibelt, vilket tillåter de membran-nära regionerna och därmed de inre enzymdelarna att röra sig tillräckligt nära för att aktivera varandra.
Att omvandla strukturell insikt till läkemedelskandidater
Utrustade med atomnivåkartor över dessa former använde författarna sedan antikroppsdisplaybibliotek för att hitta laboratorietillverkade antikroppar som fäster vid ROS1:s yttre region. De hittade två distinkta typer. En antikropp binder exakt där NELL2 först lägger an, blockerar fysiskt liganden och förhindrar aktivering. En andra antikropp kilas in i språnget mellan armen och ROS1:s centrala nav och stabiliserar den ursprungliga böjda, klämda konformationen. Båda antikropparna slår kraftfullt ned ROS1-driven signalering i celler, även om deras två armar i princip skulle kunna föra receptorer samman. Detta visar att enkel klustring inte räcker: aktivering kräver nödvändigtvis den NELL2-inducerade formförändringen som frigör benet och låter de inre enzymerna mötas.
Vad detta betyder för framtida cancerterapier
Arbetet visar att ROS1 styrs av ett tvåstegs-säkerhetssystem: receptorer måste dras ihop av en mångenhetssignal och måste också genomgå en omfattande formförändring som frigör en intern broms. NELL2 tillhandahåller båda funktionerna, medan de nyligen upptäckta antikropparna selektivt stör antingen det initiala greppet eller upplåsningsrörelsen. För icke-experter är huvudpoängen att forskarna äntligen har identifierat en naturlig strömbrytare för ROS1 och nästan atom för atom kartlagt hur den förvandlar ett av-stadium till ett på-stadium. Dessa insikter lägger grunden för nästa generation biologiska läkemedel som skulle kunna tystna ROS1 specifikt i tumörer, samtidigt som andra cellulära switchar lämnas orörda.
Citering: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Nyckelord: ROS1-receptor, receptor-tyrosinkinas, cancersignalering, NELL2-ligand, terapeutiska antikroppar