Clear Sky Science · es
Agrupamiento y un cambio conformacional impulsan la activación de la tirosina quinasa receptora ROS1 en mamíferos
Por qué esto importa para la salud y el cáncer
Muchos cánceres secuestran los mismos sistemas de comunicación que las células sanas utilizan para crecer y desarrollarse. Uno de esos sistemas gira en torno a una proteína de superficie denominada ROS1, que ayuda a controlar el desarrollo tisular pero que, cuando se utiliza incorrectamente, también puede impulsar tumores. Hasta ahora, los científicos no sabían qué activa naturalmente a ROS1 ni cómo desactivarlo con fármacos modernos. Este estudio descubre tanto el activador largamente buscado de ROS1 como una imagen detallada de su funcionamiento, abriendo nuevas vías para tratar los cánceres que dependen de esta molécula.
Una antena celular largamente misteriosa
ROS1 pertenece a una gran familia de “antenas” celulares conocidas como receptores tirosina quinasa. Estas proteínas atraviesan la membrana celular: una porción exterior detecta señales, mientras que una porción interior transmite mensajes que indican a la célula que crezca, se divida o se especialice. ROS1 es inusual dentro de esta familia. Tiene una de las regiones extracelulares más grandes y complejas, y durante décadas nadie supo qué señal natural reconocía. Aun así, ROS1 aparece en muchos tumores, ya sea como fusiones génicas anómalas que son dianas farmacológicas conocidas, o como proteína de longitud completa presente a niveles altos en cánceres de cerebro, pulmón, cavidad oral y algunos de mama. Dado que los fármacos existentes actúan principalmente sobre la porción enzimática interna, los investigadores esperaban que entender la porción exterior pudiera inspirar terapias con anticuerpos más selectivas y duraderas.
Encontrar y demostrar la señal faltante
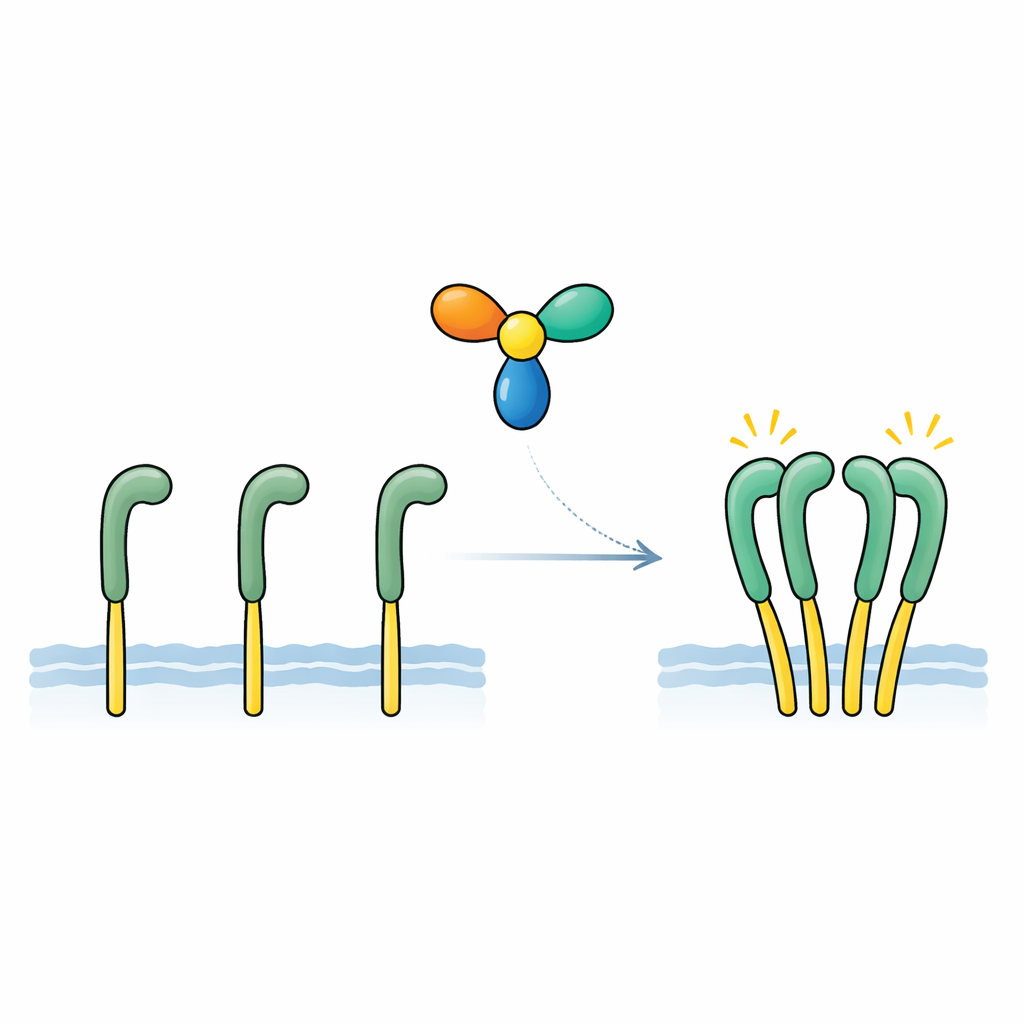
El equipo se centró en una proteína secretada llamada NELL2, previamente vinculada al desarrollo nervioso y al papel de ROS1 en la fertilidad masculina. Mediante medidas de unión sensibles, mostraron que NELL2 se adhiere directa y fuertemente a la porción extracelular de ROS1, con una afinidad similar a la de factores de crecimiento clásicos y sus receptores. En células diseñadas con un receptor de prueba basado en ROS1, la adición de NELL2 aumentó marcadamente las marcas químicas de “encendido” en la cara interna del receptor y activó vías de señalización aguas abajo. Una versión modificada de NELL2 forzada a una forma monomérica todavía podía unirse a ROS1 pero dejó de activarlo. Esto reveló dos puntos clave: NELL2 es una señal activadora genuina de ROS1 y su capacidad para formar un complejo multímérico es esencial para conmutar el receptor a un estado activo.
Un cambio de forma que desbloquea la actividad
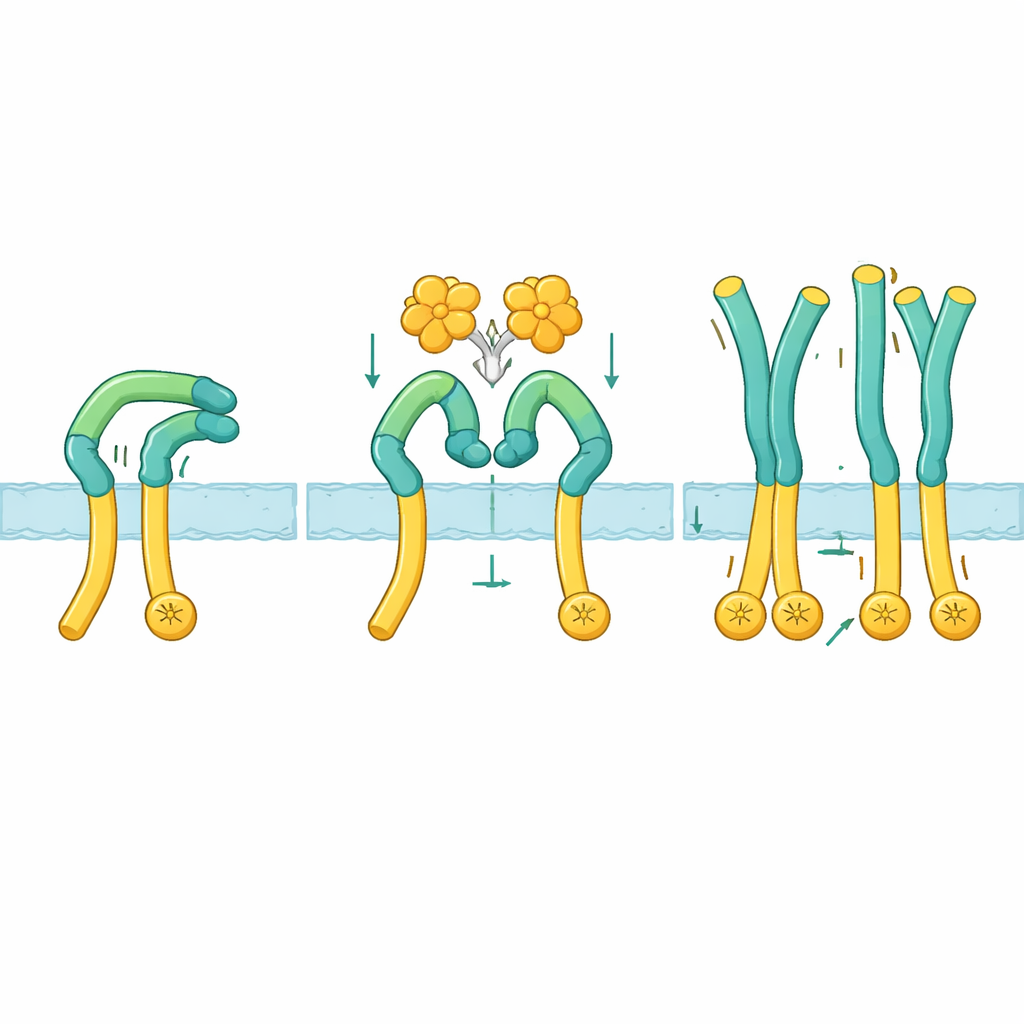
Para ver cómo funciona realmente esta activación, los investigadores usaron criomicroscopía electrónica para visualizar la región exterior de ROS1 sola y en complejo con NELL2. En el estado inactivo, ROS1 se pliega sobre sí mismo: una porción superior en forma de “brazo” se inclina hacia abajo y se cierra contra una larga “pierna” que conduce hacia la membrana celular. Esta postura doblada mantiene la parte inferior rígida y parece mantener los extremos enzimáticos internos demasiado separados para comunicarse. Cuando NELL2 se une, se agarra a tres puntos diferentes a través de varios dominios en el brazo de ROS1. Esta unión no solo agrupa múltiples moléculas de ROS1, sino que también separa el brazo de la pierna y lo rota aproximadamente 130 grados hacia una postura más erguida. Una vez que se libera esta abrazadera, el segmento de la pierna se vuelve flexible, permitiendo que las regiones próximas a la membrana, y por tanto las partes enzimáticas internas, se acerquen lo suficiente para activarse mutuamente.
Convertir la información estructural en candidatos a fármacos
Con mapas a nivel atómico de estas conformaciones, los autores emplearon bibliotecas de visualización de anticuerpos para encontrar anticuerpos fabricados en laboratorio que se adhieren a la región extracelular de ROS1. Descubrieron dos tipos distintos. Un anticuerpo se une precisamente donde NELL2 se acopla inicialmente, bloqueando físicamente al ligando e impidiendo la activación. Un segundo anticuerpo se interpone en la hendidura entre el brazo y el núcleo central de ROS1, estabilizando la conformación original doblada y cerrada. Ambos anticuerpos inhibieron de forma potente la señalización impulsada por ROS1 en células, aunque, en principio, sus dos brazos podrían juntar receptores. Esto demuestra que el simple agrupamiento no es suficiente: la activación requiere absolutamente el cambio conformacional inducido por NELL2 que libera la pierna y permite que las enzimas internas se encuentren.
Qué implica esto para futuras terapias contra el cáncer
Este trabajo revela que ROS1 está controlado por un sistema de seguridad en dos pasos: los receptores deben ser reunidos por una señal multicomponente y además deben sufrir un cambio de forma mayor que libere un freno interno. NELL2 proporciona ambas funciones, mientras que los anticuerpos recién descritos interfieren selectivamente con el agarre inicial o con el movimiento de desbloqueo. Para lectores no expertos, la conclusión es que los científicos han identificado finalmente un interruptor natural para ROS1 y han cartografiado, casi átomo por átomo, cómo convierte un estado apagado en uno encendido. Estos conocimientos sientan las bases para fármacos biológicos de nueva generación que podrían silenciar específicamente a ROS1 en tumores, dejando intactos otros interruptores celulares.
Cita: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Palabras clave: receptor ROS1, receptor tirosina quinasa, señalización en el cáncer, ligando NELL2, anticuerpos terapéuticos