Clear Sky Science · nl
Clustering en een conformationele schakelaar drijven de activatie van de zoogdier receptor-tyrosinekinase ROS1
Waarom dit belangrijk is voor gezondheid en kanker
Veel kankers kapen dezelfde communicatiepaden die gezonde cellen gebruiken om te groeien en zich te ontwikkelen. Een van die systemen draait om een oppervlakteeiwit genaamd ROS1, dat helpt weefselontwikkeling te reguleren maar ook tumoren kan stimuleren wanneer het verkeerd wordt gebruikt. Tot nu toe wisten wetenschappers niet wat ROS1 op natuurlijke wijze inschakelt, of hoe het met moderne medicijnen uit te zetten. Deze studie onthult zowel de langgezochte trigger voor ROS1 als een gedetailleerd beeld van hoe het werkt, en opent daarmee nieuwe wegen voor de behandeling van kankers die afhankelijk zijn van dit molecuul.
Een lang mysterieus celantennetje
ROS1 behoort tot een grote familie van cellulaire “antennes” die receptor-tyrosinekinasen worden genoemd. Deze eiwitten steken door het celmembraan: een buitenste deel detecteert signalen, terwijl een binnenste deel berichten doorgeeft die de cel vertellen te groeien, zich te delen of te specialiseren. ROS1 is ongewoon binnen deze familie. Het heeft een van de grootste en meest uitgebreide buitenste regio’s, en decennialang wist niemand welk natuurlijk signaal het herkent. Toch duikt ROS1 op in veel tumoren, hetzij als abnormale genfusies die reeds medicijndoelen zijn, hetzij als het volledige eiwit dat in hoge mate voorkomt bij hersen-, long-, mond- en sommige borstkankers. Omdat bestaande medicijnen vooral het binnenste enzymgedeelte raken, hoopten onderzoekers dat inzicht in het buitenste gedeelte antistoftherapieën zou kunnen inspireren die selectiever en duurzamer zijn.
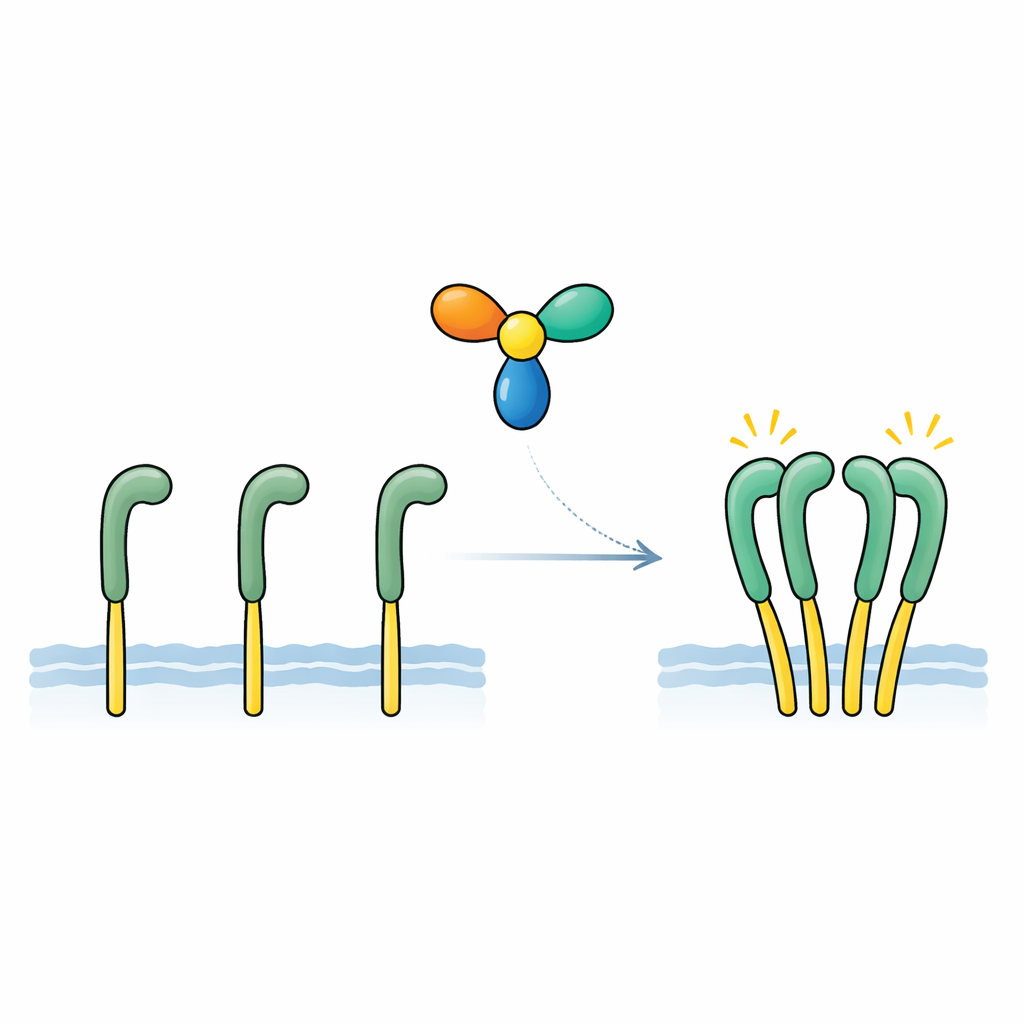
Het ontbrekende signaal vinden en bewijzen
Het team richtte zich op een uitgescheiden eiwit genaamd NELL2, eerder gekoppeld aan zenuwontwikkeling en aan de rol van ROS1 in mannelijke vruchtbaarheid. Met gevoelige bindingsmetingen toonden ze aan dat NELL2 direct en strak bindt aan het buitenste deel van ROS1, met een affiniteit vergelijkbaar met klassieke groeifactoren en hun receptoren. In gemodificeerde cellen met een op ROS1 gebaseerd testreceptor versterkte toevoeging van NELL2 sterk de chemische "aan"-kenmerken aan de binnenzijde van de receptor en activeerde downstream signaalroutes. Een gewijzigde versie van NELL2 die tot een eenheid was geforceerd kon wel ROS1 binden maar schakelde het niet meer aan. Dit onthulde twee belangrijke punten: NELL2 is een echte activerende signaalgever voor ROS1, en het vermogen van NELL2 om een meer-eenheidcomplex te vormen is essentieel om de receptor in een actieve toestand te zetten.
Een vormverandering die activiteit ontgrendelt
Om te zien hoe deze activatie precies werkt, gebruikten de onderzoekers cryo-elektronenmicroscopie om ROS1’s buitenste regio alleen en in complex met NELL2 te visualiseren. In de rusttoestand vouwt ROS1 zich naar achteren: een hoger gelegen "arm"-gedeelte buigt naar beneden en klemt zich tegen een lange "poot" die richting het celmembraan loopt. Deze gebogen houding houdt het onderste deel star en lijkt te voorkomen dat de binnenste enzymuiteinden dicht genoeg bij elkaar komen om te communiceren. Wanneer NELL2 bindt, grijpt het drie verschillende plekken aan over meerdere domeinen op de ROS1-arm. Deze binding clustert niet alleen meerdere ROS1-moleculen samen, maar wrikt ook de arm weg van de poot en roteert deze met ongeveer 130 graden naar een meer rechtopstaande positie. Zodra deze klem is losgelaten, wordt het pootsegment flexibel, waardoor de membraan-naastgelegen regio’s en daarmee de binnenste enzymdelen dicht genoeg kunnen bewegen om elkaar te activeren.
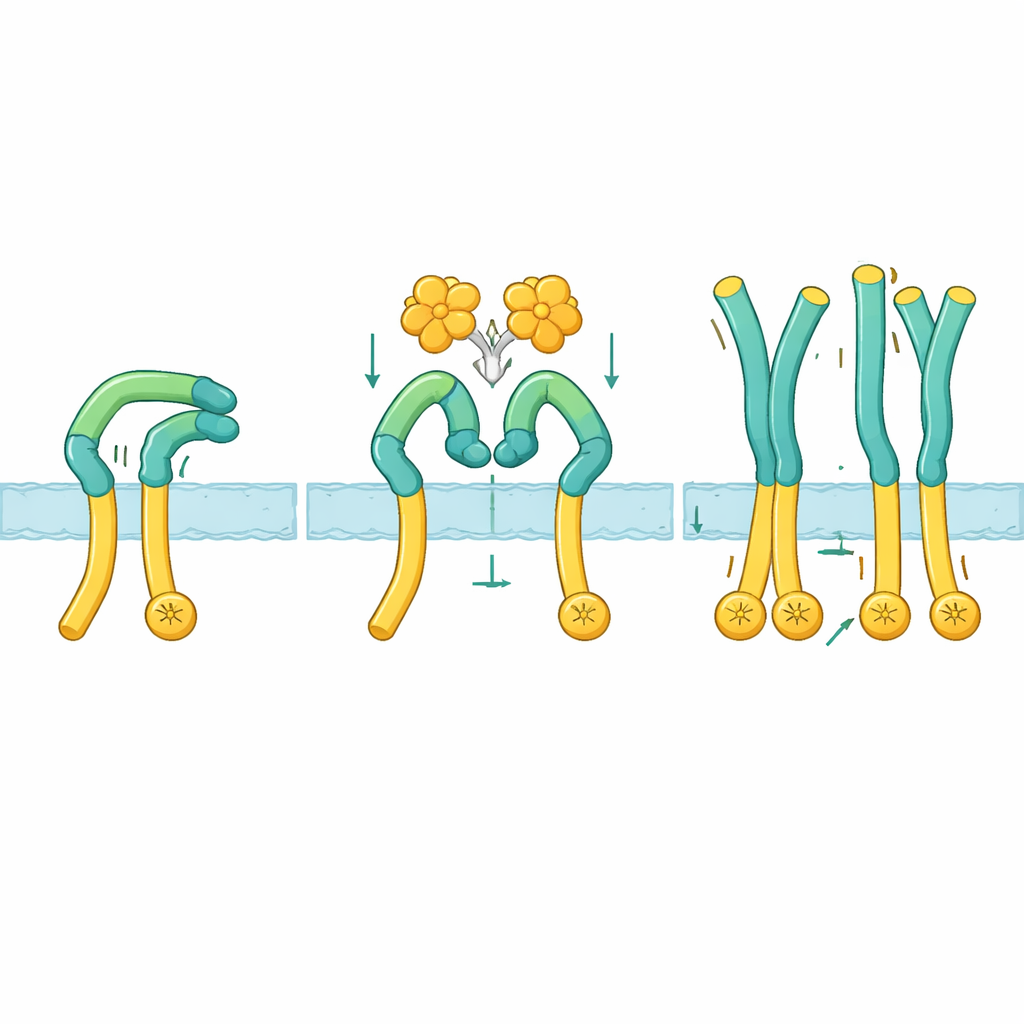
Structureel inzicht omzetten in medicijnkandidaten
Gewapend met atomaire kaarten van deze vormen, gebruikten de auteurs vervolgens antilichaam-displaybibliotheken om in het laboratorium gemaakte antilichamen te vinden die zich aan ROS1’s buitenste regio hechten. Ze ontdekten twee verschillende typen. Eén antilichaam bindt precies waar NELL2 eerst aanhecht en blokkeert fysiek het ligand en voorkomt activatie. Een tweede antilichaam klemt zich in de spleet tussen de arm en de centrale hub van ROS1 en stabiliseert de oorspronkelijke gebogen, geklemde conformatie. Beide antilichamen schakelden ROS1-gedreven signaaloverdracht in cellen krachtig uit, ook al zouden hun twee armen in principe receptoren bij elkaar kunnen brengen. Dit toont aan dat simpele clustering onvoldoende is: activatie vereist absoluut de door NELL2 geïnduceerde vormverandering die de poot bevrijdt en de binnenste enzymen elkaar laat ontmoeten.
Wat dit betekent voor toekomstige kankertherapieën
Dit werk laat zien dat ROS1 wordt gecontroleerd door een tweestapsveiligheidssysteem: receptoren moeten door een meer-eenheidssignaal bij elkaar worden getrokken en moeten bovendien een grote vormverandering ondergaan die een interne rem loslaat. NELL2 biedt beide functies, terwijl de nieuw ontdekte antilichamen selectief ingrijpen op óf de initiële greep óf de ontgrendelingsbeweging. Voor niet-experts is de kernboodschap dat wetenschappers eindelijk een natuurlijke schakelaar voor ROS1 hebben geïdentificeerd en bijna atoomgewijs in kaart hebben gebracht hoe het een uit- naar een aan-toestand omzet. Deze inzichten vormen de basis voor volgende generatie biologische geneesmiddelen die ROS1 specifiek in tumoren kunnen stilleggen, terwijl andere cellulaire schakelaars ongemoeid blijven.
Bronvermelding: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Trefwoorden: ROS1-receptor, receptor-tyrosinekinase, kankersignalering, NELL2-ligand, therapeutische antilichamen