Clear Sky Science · ru
Кластеризация и конформационный переключатель запускают активацию тирозинкиназного рецептора ROS1 у млекопитающих
Почему это важно для здоровья и онкологии
Многие раки захватывают те же системы коммуникации, которые используют здоровые клетки для роста и развития. Одна из таких систем основана на белке на поверхности клетки под названием ROS1, который помогает контролировать развитие тканей, но при нарушениях может запускать опухолевый рост. До сих пор ученым было неизвестно, что естественным образом включает ROS1 и как эффективно его выключить современными препаратами. Это исследование раскрывает как давно разыскиваемый триггер ROS1, так и подробную картину его работы, открывая новые пути лечения опухолей, зависящих от этого белка.
Долгое время таинственная клеточная «антенна»
ROS1 принадлежит большой семье клеточных «антенн», известных как рецепторные тирозинкиназы. Эти белки пронизывают клеточную мембрану: внешняя часть улавливает сигналы, а внутренняя передает сообщения, заставляющие клетку расти, делиться или дифференцироваться. ROS1 выделяется в этой семье: у него одна из самых больших и сложных внешних областей, и десятилетиями никто не знал, какой естественный сигнал она распознает. Между тем ROS1 встречается во многих опухолях — либо в виде аномальных генетических фузий, уже являющихся мишенями для лекарств, либо в виде полноразмерного белка, обнаруживаемого в повышенных уровнях при раке мозга, легких, полости рта и в некоторых случаях при раке молочной железы. Поскольку существующие препараты в основном нацелены на внутреннюю ферментативную часть, исследователи надеялись, что понимание внешней области поможет разработать антительным препараты, которые будут более селективны и долговечны.
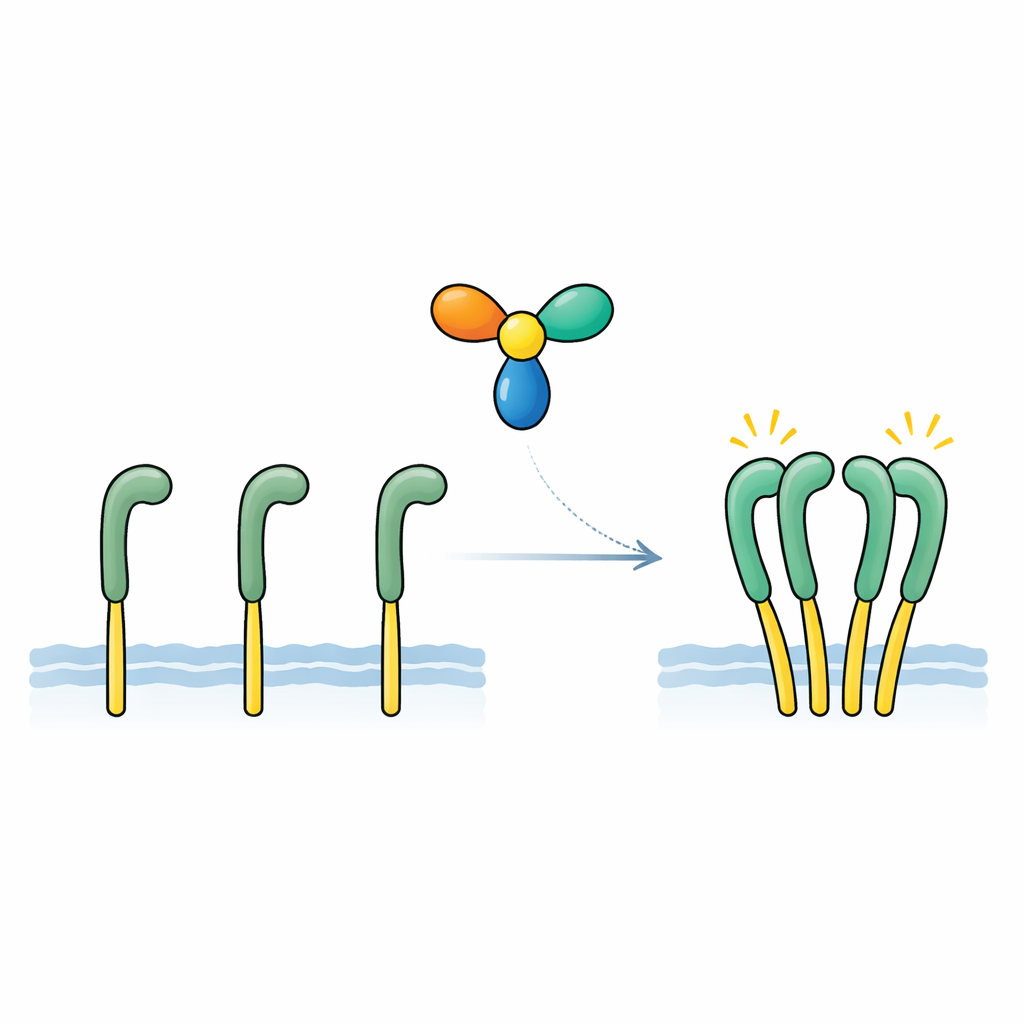
Нахождение и доказательство недостающего сигнала
Команда сосредоточилась на секретируемом белке NELL2, ранее связанном с развитием нервной системы и ролью ROS1 в мужской фертильности. С помощью чувствительных измерений связывания они показали, что NELL2 напрямую и прочно присоединяется к внешней части ROS1, с афинностью, сопоставимой с классическими факторами роста и их рецепторами. В инженерных клетках с тестовым рецептором на основе ROS1 добавление NELL2 сильно усиливало фосфорилирование «включающих» меток на внутренней стороне рецептора и активировало внизпотоковые сигнальные пути. Модифицированная версия NELL2, принудительно существовавшая в одиночной форме, по-прежнему могла связываться с ROS1, но уже не активировала его. Это подчеркнуло два ключевых момента: NELL2 является истинным активирующим сигналом для ROS1, и способность NELL2 образовывать многоединичный комплекс необходима для переключения рецептора в активное состояние.
Изменение формы, которое освобождает активность
Чтобы понять, как именно происходит активация, исследователи использовали крио–электронную микроскопию для визуализации внешней области ROS1 в одиночном состоянии и в комплексе с NELL2. В состоянии покоя ROS1 складывается назад: верхняя «рука» сгибается вниз и прижимается к длинной «ноге», ведущей к мембране. Эта согнутая поза удерживает нижнюю часть жесткой и, по-видимому, не дает внутренним ферментативным участкам приблизиться друг к другу для взаимодействия. При связывании NELL2 захватывает три разные точки на нескольких доменах «руки» ROS1. Такое связывание не только стягивает несколько молекул ROS1 вместе, но и отщелкивает руку от ноги, поворачивая её примерно на 130 градусов в более вертикальное положение. Как только этот зажим отпускался, сегмент ноги становился гибким, позволяя прилегающим к мембране областям и, следовательно, внутренним ферментативным частям сближаться достаточно для взаимной активации.
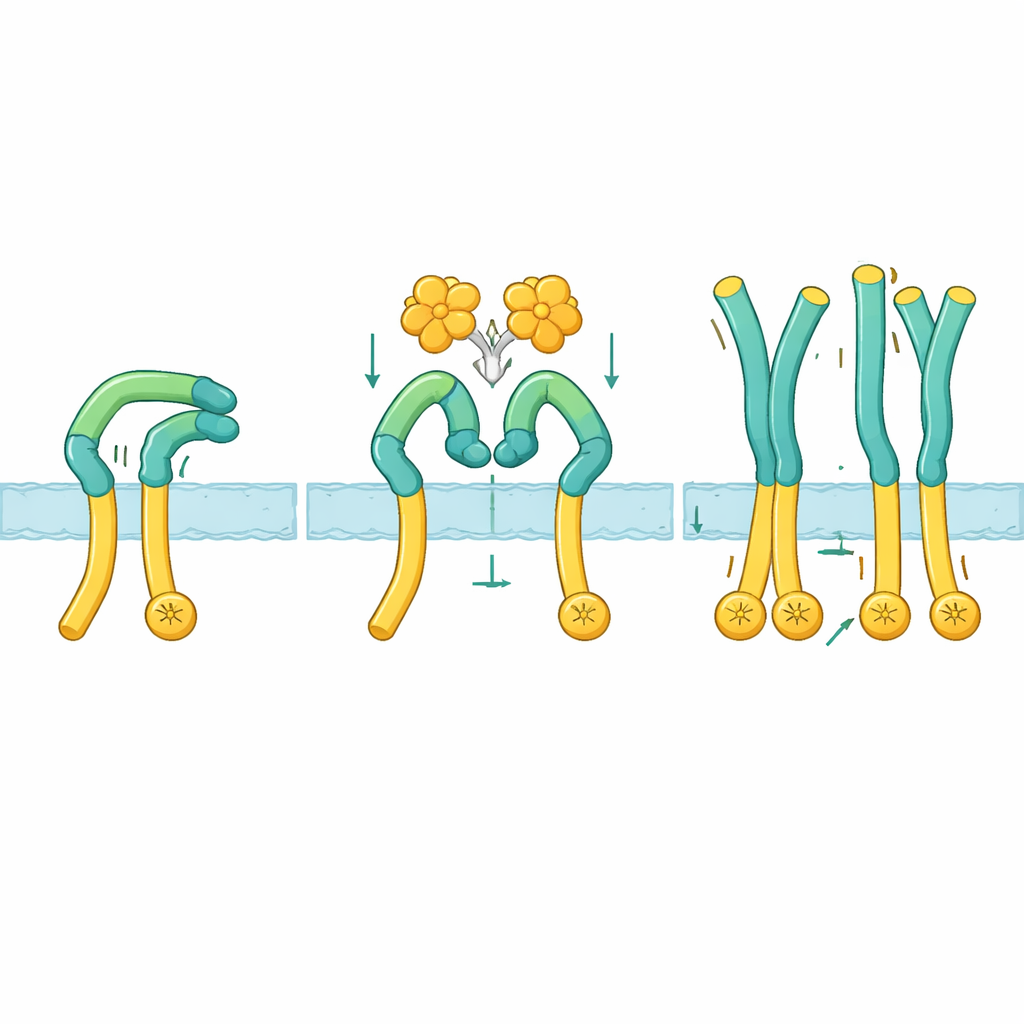
От структурного понимания к кандидатам в препараты
Имея атомные карты этих конформаций, авторы затем использовали библиотеки отображаемых антител, чтобы найти лабораторные антитела, связывающиеся с внешней частью ROS1. Они обнаружили два разных типа. Одно антитело связывается точно там, где первоначально докируется NELL2, физически блокируя лиганд и предотвращая активацию. Второе антитело вклинивается в щель между рукой и центральным узлом ROS1, стабилизируя исходную согнутую, зажатую конформацию. Оба антитела мощно отключали ROS1‑опосредованные сигналы в клетках, хотя формально их двуцепочечные структуры тоже могли бы способствовать сближению рецепторов. Это показывает: простая кластеризация недостаточна — активация обязательно требует индуцированного NELL2 изменения формы, которое освобождает «ногу» и позволяет внутренним ферментам встретиться.
Что это означает для будущих противораковых терапий
Эта работа показывает, что ROS1 контролируется двухступенчатой системой безопасности: рецепторы должны быть стянуты вместе многоединичным сигналом и одновременно подвергнуться крупной конформационной перестройке, снимающей внутренний тормоз. NELL2 обеспечивает обе функции, а недавно обнаруженные антитела выборочно вмешиваются либо в начальный захват, либо в движение, размыкающее конструкцию. Для неспециалистов вывод таков: ученые наконец идентифицировали естественный выключатель ROS1 и почти послойно отобразили, как он переводит рецептор из выключенного состояния в включенное. Эти знания закладывают основу для препаратов следующего поколения на биологической основе, которые смогут избирательно подавлять ROS1 в опухолях, не затрагивая другие клеточные переключатели.
Цитирование: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Ключевые слова: рецептор ROS1, тирозинкиназный рецептор, сигналы при раке, лиганд NELL2, терапевтические антитела