Clear Sky Science · pt
Agrupamento e uma mudança conformacional acionam a tirosina quinase receptora mamífera ROS1
Por que isso importa para a saúde e o câncer
Muitos cânceres se apropriam dos mesmos sistemas de comunicação que células saudáveis usam para crescer e se desenvolver. Um desses sistemas gira em torno de uma proteína de superfície chamada ROS1, que ajuda a controlar o desenvolvimento dos tecidos, mas também pode impulsionar tumores quando é usada de forma inadequada. Até agora, os cientistas não sabiam o que naturalmente ativa o ROS1, nem como desligá‑lo com drogas modernas. Este estudo revela tanto o gatilho há muito procurado para o ROS1 quanto um retrato detalhado de seu funcionamento, abrindo novos caminhos para tratar cânceres que dependem dessa molécula.
Uma antena celular há muito misteriosa
ROS1 pertence a uma grande família de “antenas” celulares conhecidas como tirosina quinases receptoras. Essas proteínas atravessam a membrana celular: uma porção externa percebe sinais, enquanto uma porção interna transmite mensagens que dizem à célula para crescer, dividir‑se ou se especializar. O ROS1 é incomum nessa família. Tem uma das regiões externas mais longas e elaboradas, e durante décadas ninguém sabia qual sinal natural ele reconhecia. Ainda assim, o ROS1 aparece em muitos tumores, seja como fusões gênicas anormais que já são alvos de fármacos, seja como proteína de comprimento total encontrada em altos níveis em cânceres de cérebro, pulmão, boca e alguns de mama. Como as drogas existentes atingem principalmente a porção enzimática interna, os pesquisadores esperavam que entender a porção externa pudesse inspirar terapias com anticorpos mais seletivas e duradouras.
Encontrando e comprovando o sinal ausente
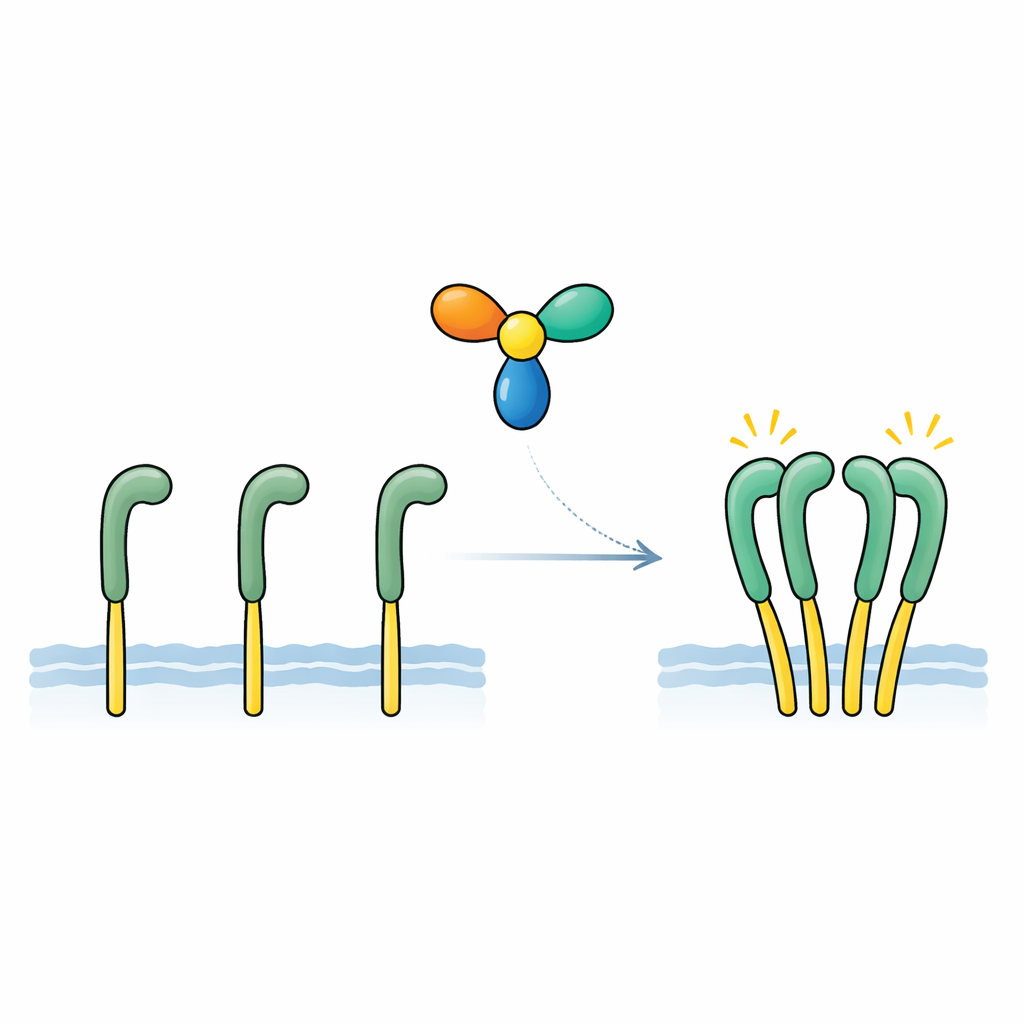
A equipe concentrou‑se em uma proteína secretada chamada NELL2, previamente ligada ao desenvolvimento nervoso e ao papel do ROS1 na fertilidade masculina. Usando medições de afinidade sensíveis, demonstraram que a NELL2 se liga direta e fortemente à porção externa do ROS1, com uma afinidade semelhante à de fatores de crescimento clássicos e seus receptores. Em células engenheiradas carregando um receptor de teste baseado no ROS1, a adição de NELL2 aumentou fortemente as marcas químicas de “ligado” no lado interno do receptor e ativou vias de sinalização a jusante. Uma versão modificada da NELL2, forçada a existir em forma monomérica, ainda podia se ligar ao ROS1, mas não o ativava. Isso revelou dois pontos-chave: NELL2 é um sinal ativador genuíno para o ROS1, e sua capacidade de formar um complexo multimérico é essencial para alternar o receptor para um estado ativo.
Uma mudança de forma que destrava a atividade
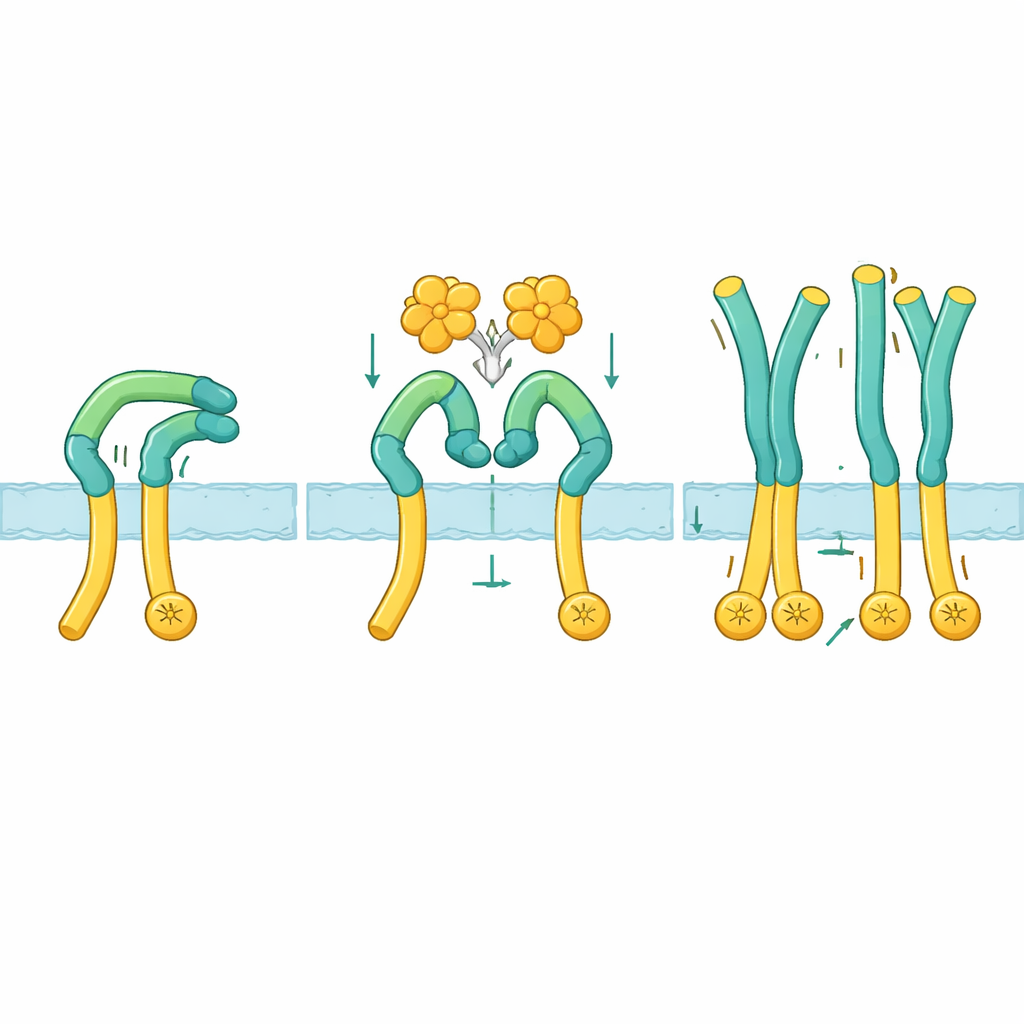
Para ver como essa ativação realmente funciona, os pesquisadores usaram crio–microscopia eletrônica para visualizar a região externa do ROS1 sozinha e em complexo com a NELL2. No estado de repouso, o ROS1 se dobra sobre si mesmo: uma porção superior em forma de “braço” dobra‑se para baixo e trava contra uma longa “perna” que conduz em direção à membrana celular. Essa posição dobrada mantém a parte inferior rígida e parece manter as extremidades enzimáticas internas muito afastadas para se comunicarem. Quando a NELL2 se liga, ela envolve três pontos diferentes através de vários domínios no braço do ROS1. Essa ligação não apenas agrupa múltiplas moléculas de ROS1, como também afasta o braço da perna e o rota em cerca de 130 graus para uma posição mais ereta. Uma vez que essa trava é liberada, o segmento da perna torna‑se flexível, permitindo que as regiões próximas à membrana, e portanto as partes enzimáticas internas, se aproximem o suficiente para se ativarem mutuamente.
Transformando insight estrutural em candidatos a fármaco
Munidos de mapas em nível atômico dessas conformações, os autores então utilizaram bibliotecas de exibição de anticorpos para encontrar anticorpos artificiais que se ligam à região externa do ROS1. Eles descobriram dois tipos distintos. Um anticorpo liga‑se precisamente ao local onde a NELL2 inicialmente se ancora, bloqueando fisicamente o ligante e prevenindo a ativação. Um segundo anticorpo se aloja na fenda entre o braço e o núcleo central do ROS1, estabilizando a conformação dobrada e travada original. Ambos os anticorpos bloquearam com potência a sinalização dirigida pelo ROS1 em células, mesmo que, em princípio, seus dois braços pudessem agrupar receptores. Isso mostra que o simples agrupamento não é suficiente: a ativação requer necessariamente a mudança conformacional induzida pela NELL2 que libera a perna e permite o encontro das enzimas internas.
O que isso significa para futuras terapias contra o câncer
Este trabalho revela que o ROS1 é controlado por um sistema de segurança em dois passos: os receptores devem ser reunidos por um sinal multimérico e também devem sofrer uma grande mudança de forma que libere um freio interno. A NELL2 fornece ambas as funções, enquanto os anticorpos recém‑descobertos interferem seletivamente tanto na aderência inicial quanto no movimento de destravamento. Para leitores não especialistas, a conclusão é que os cientistas finalmente identificaram um interruptor natural para o ROS1 e mapearam, quase átomo por átomo, como ele transforma um estado desligado em um estado ligado. Esses insights constituem a base para fármacos biológicos de próxima geração que poderiam silenciar especificamente o ROS1 em tumores, preservando outros interruptores celulares intactos.
Citação: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Palavras-chave: receptor ROS1, tirosina quinase receptora, sinalização do câncer, ligante NELL2, anticorpos terapêuticos