Clear Sky Science · it
Clustering e un interruttore conformazionale guidano l’attivazione della tirosina chinasi recettoriale ROS1 nei mammiferi
Perché questo è importante per la salute e il cancro
Molti tumori dirottano gli stessi sistemi di comunicazione che le cellule sane utilizzano per crescere e svilupparsi. Uno di questi sistemi ruota intorno a una proteina di superficie chiamata ROS1, che contribuisce a controllare lo sviluppo dei tessuti ma può anche promuovere i tumori se usata in modo anomalo. Fino a oggi, gli scienziati non sapevano quale segnale naturale attivasse ROS1 né come spegnerlo con farmaci moderni. Questo studio rivela sia il tanto cercato innesco di ROS1 sia una descrizione dettagliata del suo funzionamento, aprendo nuove strade per trattare i tumori che dipendono da questa molecola.
Un’antenna cellulare a lungo misteriosa
ROS1 appartiene a una vasta famiglia di “antenne” cellulari note come recettori tirosina chinasi. Queste proteine attraversano la membrana cellulare: una porzione esterna percepisce i segnali, mentre una porzione interna trasmette messaggi che dicono alla cellula di crescere, dividersi o specializzarsi. ROS1 è insolito all’interno di questa famiglia. Ha una delle regioni esterne più grandi e complesse e per decenni nessuno sapeva quale segnale naturale riconoscesse. Eppure ROS1 compare in molti tumori, sia come fusioni geniche anomale già bersagliate da farmaci, sia come proteina a lunghezza intera presente a livelli elevati in tumori cerebrali, polmonari, orali e in alcuni tumori della mammella. Poiché i farmaci esistenti colpiscono principalmente la porzione enzimatica interna, i ricercatori speravano che comprendere la porzione esterna potesse ispirare terapie a base di anticorpi più selettive e durature.
Trovare e dimostrare il segnale mancante
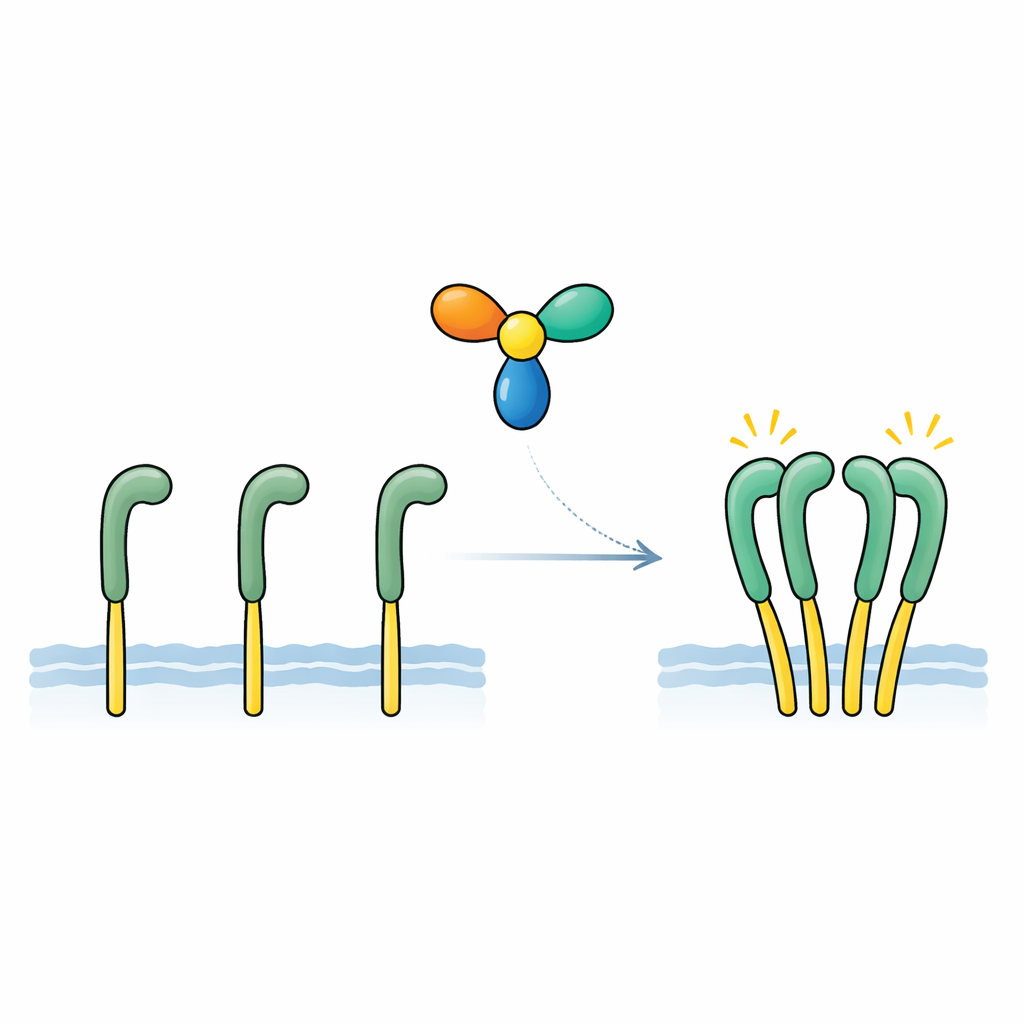
Il gruppo si è concentrato su una proteina secreta chiamata NELL2, precedentemente collegata allo sviluppo nervoso e al ruolo di ROS1 nella fertilità maschile. Usando misure di legame sensibili, hanno mostrato che NELL2 si lega direttamente e con grande affinità alla porzione esterna di ROS1, con un’attrazione simile a quella dei fattori di crescita classici per i loro recettori. In cellule ingegnerizzate che portavano un recettore di prova basato su ROS1, l’aggiunta di NELL2 aumentava fortemente i segni chimici di “accensione” sul lato interno del recettore e attivava le vie di segnalazione a valle. Una versione modificata di NELL2, costretta a rimanere in forma monomerica, poteva ancora legare ROS1 ma non lo attivava più. Questo ha rivelato due punti chiave: NELL2 è un autentico segnale attivante per ROS1 e la sua capacità di formare un complesso multiunità è essenziale per commutare il recettore in uno stato attivo.
Un cambio di forma che sblocca l’attività
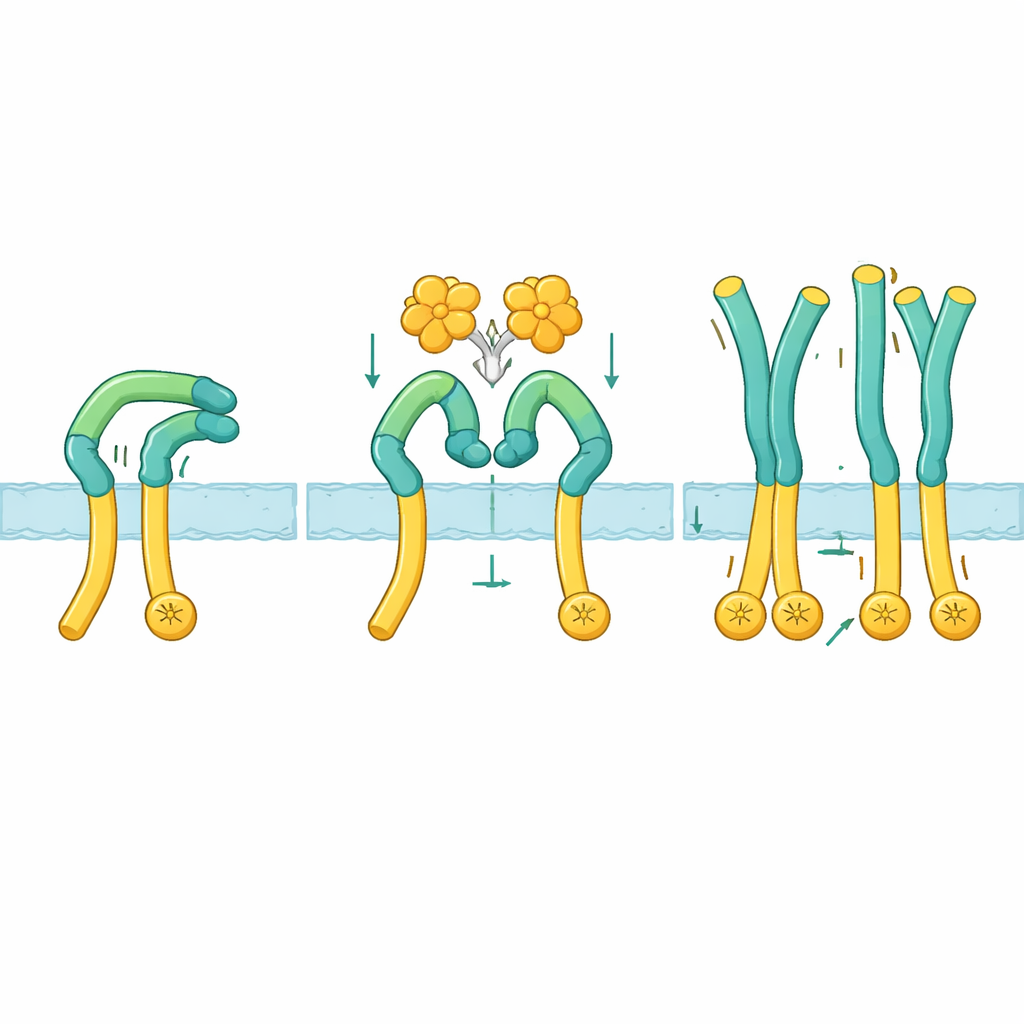
Per capire come avviene concretamente questa attivazione, i ricercatori hanno usato la crio–microscopia elettronica per visualizzare la regione esterna di ROS1 da sola e in complesso con NELL2. Nello stato di riposo, ROS1 si ripiega su sé stesso: una porzione superiore a “braccio” si piega verso il basso e si blocca contro una lunga “gamba” che porta verso la membrana cellulare. Questa posa piegata mantiene la parte inferiore rigida e sembra mantenere le estremità enzimatiche interne troppo distanti per comunicare. Quando NELL2 si lega, si ancora a tre punti diversi distribuiti su diversi domini del braccio di ROS1. Questo legame non solo raggruppa più molecole di ROS1, ma stacca anche il braccio dalla gamba e lo ruota di circa 130 gradi in una posizione più eretta. Una volta rilasciata questa pinza, il segmento a gamba diventa flessibile, permettendo alle regioni prossimali alla membrana, e quindi alle parti enzimatiche interne, di avvicinarsi a sufficienza per attivarsi a vicenda.
Trasformare l’intuizione strutturale in candidati farmaceutici
Con mappe a livello atomico di queste conformazioni, gli autori hanno poi utilizzato librerie di anticorpi esposti per trovare anticorpi prodotti in laboratorio che si legano alla regione esterna di ROS1. Hanno individuato due tipi distinti. Un anticorpo si lega precisamente nel punto in cui NELL2 si aggancia inizialmente, bloccando fisicamente il ligando e impedendo l’attivazione. Un secondo anticorpo si infila nella fenditura tra il braccio e il fulcro centrale di ROS1, stabilizzando la conformazione piegata e bloccata originale. Entrambi gli anticorpi spengono potentemente la segnalazione guidata da ROS1 nelle cellule, anche se, in teoria, i loro due siti di legame potrebbero riunire i recettori. Questo dimostra che il semplice clustering non è sufficiente: l’attivazione richiede assolutamente il cambiamento di forma indotto da NELL2 che libera la gamba e permette agli enzimi interni di incontrarsi.
Cosa significa per le future terapie anticancro
Questo lavoro rivela che ROS1 è controllato da un sistema di sicurezza a due passi: i recettori devono essere avvicinati da un segnale multiunità e devono anche subire un importante cambiamento di forma che rilascia un freno interno. NELL2 fornisce entrambe le funzioni, mentre i nuovi anticorpi scoperti interferiscono selettivamente sia con la presa iniziale sia con il movimento di sblocco. Per i lettori non esperti, la conclusione è che gli scienziati hanno finalmente identificato un interruttore naturale per ROS1 e hanno mappato, quasi atomo per atomo, come esso converta uno stato spento in uno stato acceso. Queste intuizioni gettano le basi per farmaci biologici di nuova generazione che potrebbero silenziare specificamente ROS1 nei tumori, lasciando indisturbati altri interruttori cellulari.
Citazione: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Parole chiave: recettore ROS1, tirosina chinasi recettoriale, segnalazione nel cancro, ligando NELL2, anticorpi terapeutici