Clear Sky Science · ar
التجميع ومفتاح طوري يقودان تنشيط كيناز التيروزين المستقبلِي الثديي ROS1
لماذا يهم هذا للصحة والسرطان
تستولي العديد من السرطانات على أنظمة الاتصال نفسها التي تستخدمها الخلايا السليمة للنمو والتطور. أحد هذه الأنظمة يدور حول بروتين سطحي يسمى ROS1، الذي يساعد في التحكم بتطور الأنسجة ولكنه قد يسبب أيضاً الأورام عند إساءة استخدامه. حتى الآن، لم يعرف العلماء ما الذي يشغّل ROS1 طبيعياً، أو كيف يمكن إيقافه بعقاقير حديثة. تكشف هذه الدراسة عن الزناد الذي طال البحث عنه لتنشيط ROS1 كما تقدم صورة مفصلة لكيفية عمله، فاتحة طرقاً جديدة لعلاج السرطانات التي تعتمد على هذه الجزيئة.
هوائي خلوي ظل غامضاً طويلاً
ينتمي ROS1 إلى عائلة واسعة من «الهوائيات» الخلوية المعروفة بمستقبلات كيناز التيروزين. تمتد هذه البروتينات عبر غشاء الخلية: جزء خارجي يستشعر الإشارات، بينما ينقل جزء داخلي الرسائل التي تأمر الخلية بالنمو أو الانقسام أو التمايز. يتميز ROS1 داخل هذه العائلة بكونه يحتوي على واحدة من أكبر وأعقد المناطق الخارجية، وعلى مدى عقود لم يعرف أحد الإشارة الطبيعية التي يتعرف عليها. مع ذلك يظهر ROS1 في العديد من الأورام، إما كاندماجات جينية شاذة تُستهدف بالفعل بأدوية، أو كبروتين كامل الطول موجود بمستويات مرتفعة في سرطانات الدماغ والرئة والفم وبعض سرطانات الثدي. وبما أن الأدوية الحالية تستهدف أساساً الجزء الإنزيمي الداخلي، فقد أمل الباحثون أن فهم الجزء الخارجي قد يلهم علاجات بالأجسام المضادة تكون أكثر انتقائية وديمومة.
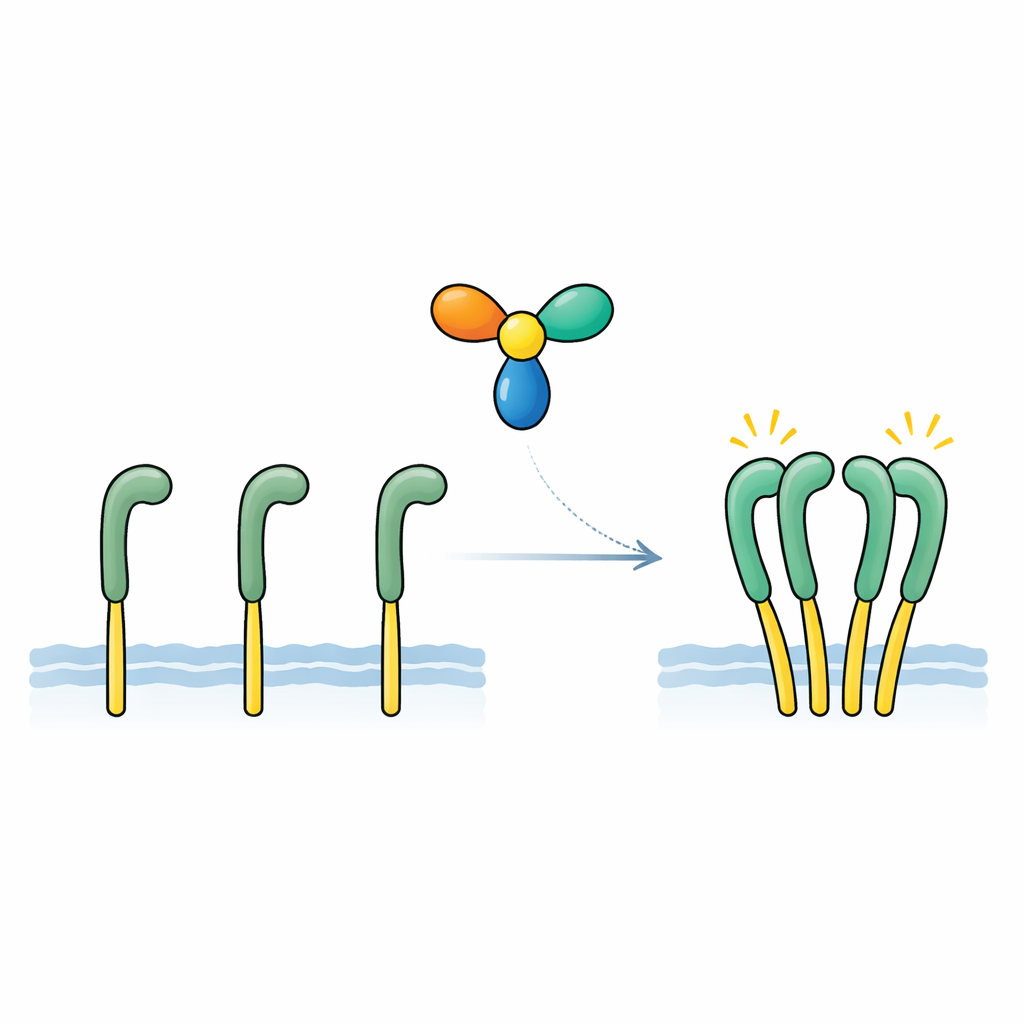
اكتشاف وإثبات الإشارة المفقودة
ركز الفريق على بروتين مُفرَز يسمى NELL2، مرتبط سابقاً بتطور الأعصاب وبدور ROS1 في الخصوبة لدى الذكور. باستخدام قياسات ربط حساسة، أظهروا أن NELL2 يرتبط مباشرة وبقوة بالجزء الخارجي من ROS1، بارتباطية تشبه تلك الخاصة بعوامل النمو ومستقبلاتها الكلاسيكية. في خلايا مُهندَسة تحمل مستقبل اختبار مبني على ROS1، أدى إضافة NELL2 إلى تعزيز كبير على العلامات الكيميائية المؤشرة للوضع «التشغيلي» على الجانب الداخلي من المستقبل وتنشيط مسارات الإشارة اللاحقة. نسخة معدلة من NELL2 مُكرهَة لتتواجد كوحدة أحادية لا تزال قادرة على الارتباط بـROS1 لكنها لم تعد تشغّله. يكشف هذا عن نقطتين أساسيتين: NELL2 هي إشارة منشِّطة حقيقية لـROS1، وقدرة NELL2 على تشكيل مجمعات متعددة الوحدات ضرورية لتحويل المستقبل إلى حالة نشطة.
تحول شكلي يطلق النشاط
لمعرفة كيف يعمل هذا التنشيط فعلياً، استخدم الباحثون المجهر الإلكتروني بالتجميد لتصوير المنطقة الخارجية من ROS1 بمفردها ومركبة مع NELL2. في الحالة الراحة، يطوي ROS1 على نفسه: جزء علوي شبيه «بالذراع» ينحني لأسفل ويثبّت نفسه على «ساق» طويلة تتجه نحو غشاء الخلية. هذا الوضع المنحني يجعل الجزء السفلي صلباً ويبدو أنه يبقي أطراف الإنزيم الداخلي متباعدة جداً بحيث لا تتواصل. عندما يرتبط NELL2، يمسك بثلاثة مواقع مختلفة عبر عدة مجالات على الذراع. هذا الارتباط لا يجمع عدة جزيئات ROS1 معاً فحسب، بل يفك أيضاً الذراع عن الساق ويديرها بحوالي 130 درجة إلى وضع أكثر اعتدالاً. بمجرد إطلاق هذا المشبك، تصبح قطعة الساق مرنة، مما يسمح للمناطق القريبة من الغشاء، وبالتالي لأجزاء الإنزيم الداخلية، بالتحرك لتقترب من بعضها بما يكفي لتنشيط بعضها البعض.
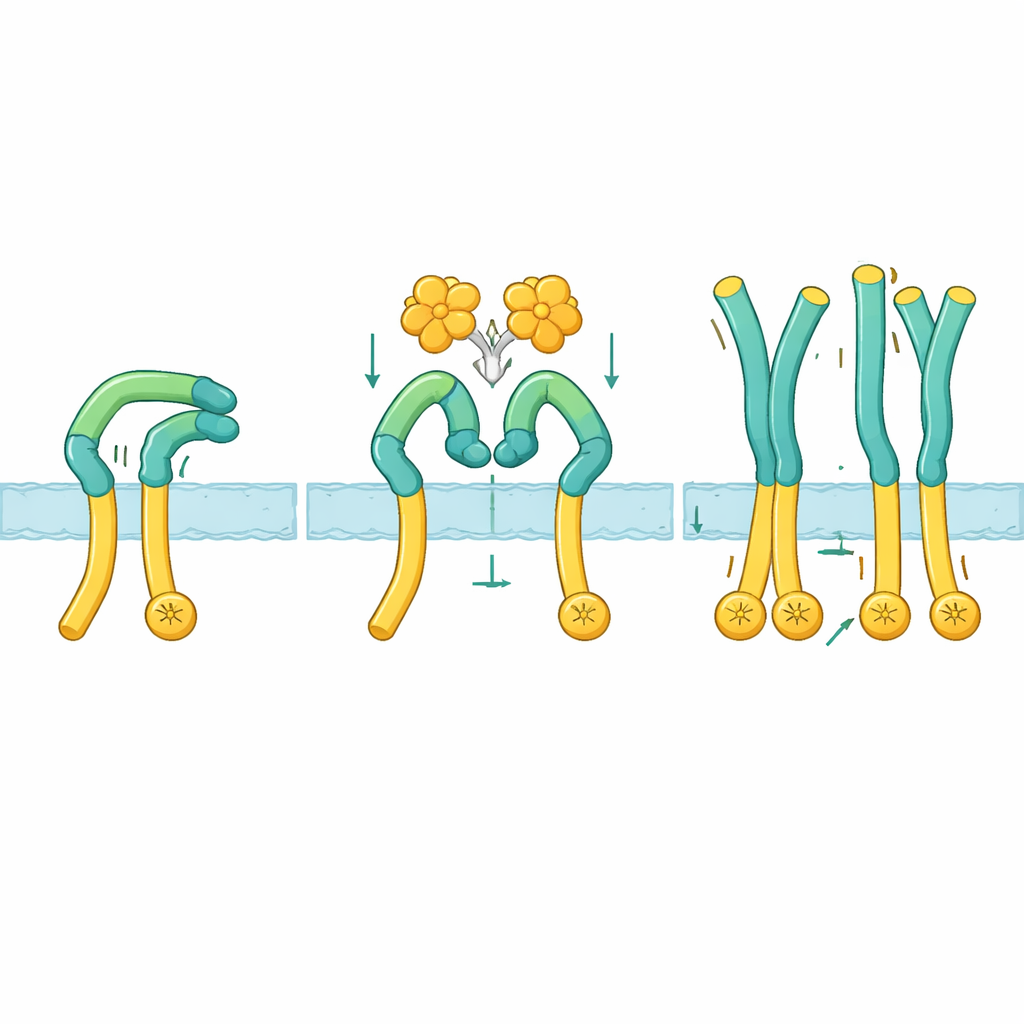
تحويل البصيرة البنيوية إلى مرشحات دوائية
مسلحين بخرائط على مستوى الذرات لهذه الأشكال، استخدم المؤلفون مكتبات عرض الأجسام المضادة للعثور على أجسام مضادة مصنّعة تلتصق بالمنطقة الخارجية من ROS1. اكتشفوا نوعين مميزين. يلتصق أحدهما تماماً بالموقع الذي يرسو فيه NELL2 أولاً، مانعاً الفيزيائياً الليغاند ومنعاً للتنشيط. يلسع جسم مضاد ثانٍ الفجوة بين الذراع والمحور المركزي لـROS1، مثبتاً الوضع المنحني الأصلي والمشبك. كلا الجسمين المضادين أوقفا بقوة إشارات ROS1 في الخلايا، على الرغم من أنه من الناحية المبدئية يمكن لذراعيهما أن تجمع المستقبلات معاً. هذا يوضح أن التجميع البسيط لا يكفي: التنشيط يتطلب بلا شك التغيير الشكلي المحفز بـNELL2 الذي يحرر الساق ويسمح لأجزاء الإنزيم الداخلية بالالتقاء.
ما الذي يعنيه هذا لعلاجات السرطان المستقبلية
تكشف هذه العمل أن ROS1 مُتحكم به عبر نظام أمان من خطوتين: يجب سحب المستقبلات معاً بواسطة إشارة متعددة الوحدات ويجب أيضاً أن تخضع لتغيير شكلي كبير يفرج عن فرملة داخلية. يوفر NELL2 الوظيفتين معاً، بينما تتدخل الأجسام المضادة المكتشفة حديثاً بشكل انتقائي إما في القبضة الأولية أو في حركة الفتح. للقراء غير المتخصصين، الخلاصة أن العلماء حددوا أخيراً زر التشغيل الطبيعي لـROS1 ورسموا تقريباً ذرة بذرة كيف يحول الحالة المطفأة إلى حالة مُشغَّلة. تؤسس هذه الرؤى قاعدة لتطوير عقاقير حيوية من الجيل التالي قد تسكت ROS1 تحديداً في الأورام مع ترك مفاتيح خلوية أخرى دون اضطراب.
الاستشهاد: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
الكلمات المفتاحية: مستقبل ROS1, كيناز التيروزين المستقبلِي, إشارات السرطان, الليغاند NELL2, أجسام مضادة علاجية