Clear Sky Science · de
Clustering und ein konformationeller Schalter treiben die Aktivierung der Säugetier-Rezeptor-Tyrosinkinase ROS1 voran
Warum das für Gesundheit und Krebs wichtig ist
Viele Krebsarten kapern dieselben Kommunikationssysteme, die gesunde Zellen für Wachstum und Entwicklung nutzen. Eines dieser Systeme dreht sich um ein Oberflächenprotein namens ROS1, das die Gewebeentwicklung mitsteuert, aber bei Fehlsteuerung auch Tumoren antreiben kann. Bislang wussten Wissenschaftler nicht, was ROS1 natürlich aktiviert oder wie man es mit modernen Wirkstoffen ausschaltet. Diese Studie entlarvt sowohl den lange gesuchten Auslöser von ROS1 als auch ein detailliertes Funktionsbild — und öffnet damit neue Wege zur Behandlung von Krebserkrankungen, die von diesem Molekül abhängen.
Eine lange rätselhafte Zellantenne
ROS1 gehört zu einer großen Familie von Zell‑“Antennen”, den Rezeptor‑Tyrosinkinasen. Diese Proteine durchspannen die Zellmembran: ein äußerer Teil nimmt Signale wahr, während ein innerer Teil Botschaften weitergibt, die der Zelle sagen, zu wachsen, sich zu teilen oder sich zu spezialisieren. ROS1 ist innerhalb dieser Familie ungewöhnlich. Es besitzt eine der größten und aufwendigsten Außendomänen, und jahrzehntelang wusste niemand, welches natürliche Signal es erkennt. Dennoch taucht ROS1 in vielen Tumoren auf — entweder als abnorme Genfusionen, die bereits medikamentöse Ziele sind, oder als vollständiges Protein, das in Gehirn-, Lungen-, Mund‑ und einigen Brustkrebserkrankungen in hohen Mengen vorkommt. Da vorhandene Medikamente vorwiegend die innere Enzymdomäne treffen, hofften Forscher, dass das Verständnis der Außendomäne Antikörpertherapien inspirieren könnte, die selektiver und langlebiger sind.
Den fehlenden Signalgeber finden und beweisen
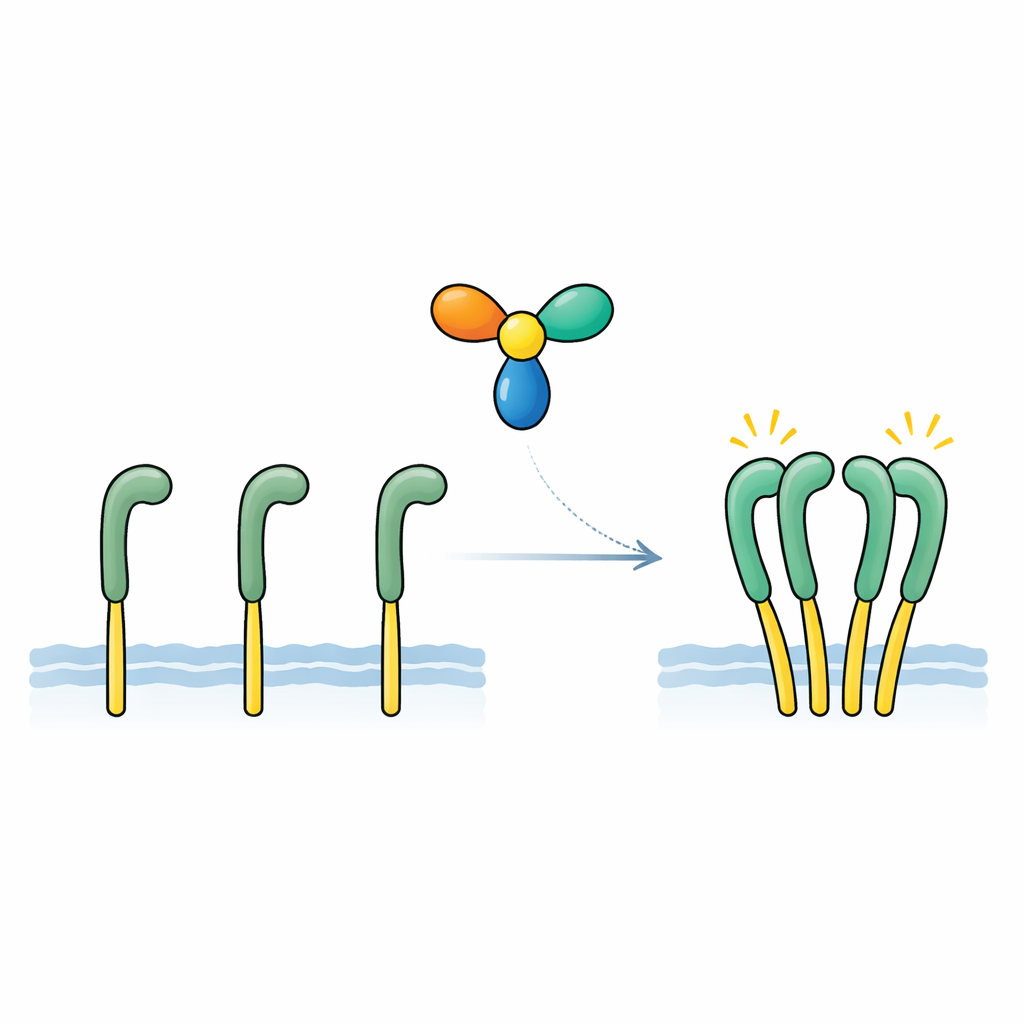
Das Team konzentrierte sich auf ein sekretierbares Protein namens NELL2, das zuvor mit der Nerventwicklung und mit ROS1s Rolle bei der männlichen Fruchtbarkeit in Verbindung gebracht worden war. Mithilfe empfindlicher Bindungsmessungen zeigten sie, dass NELL2 direkt und fest an die Außenseite von ROS1 andockt, mit einer Affinität, die mit klassischen Wachstumsfaktoren und ihren Rezeptoren vergleichbar ist. In konstruierten Zellen, die einen auf ROS1 basierenden Testrezeptor trugen, führte die Zugabe von NELL2 zu starken Zunahmen chemischer „An“-Marken an der Innenseite des Rezeptors und aktivierte nachgeschaltete Signalwege. Eine veränderte Version von NELL2, die in eine einheitliche Einzeleinheit gezwungen worden war, konnte zwar noch an ROS1 binden, schaltete es aber nicht mehr ein. Das ergab zwei zentrale Erkenntnisse: NELL2 ist ein echter Aktivierungssignalgeber für ROS1, und seine Fähigkeit, sich zu einem Mehr‑Einheiten‑Komplex zusammenzubinden, ist für das Umschalten des Rezeptors in den aktiven Zustand unerlässlich.
Ein Formwechsel, der Aktivität freisetzt
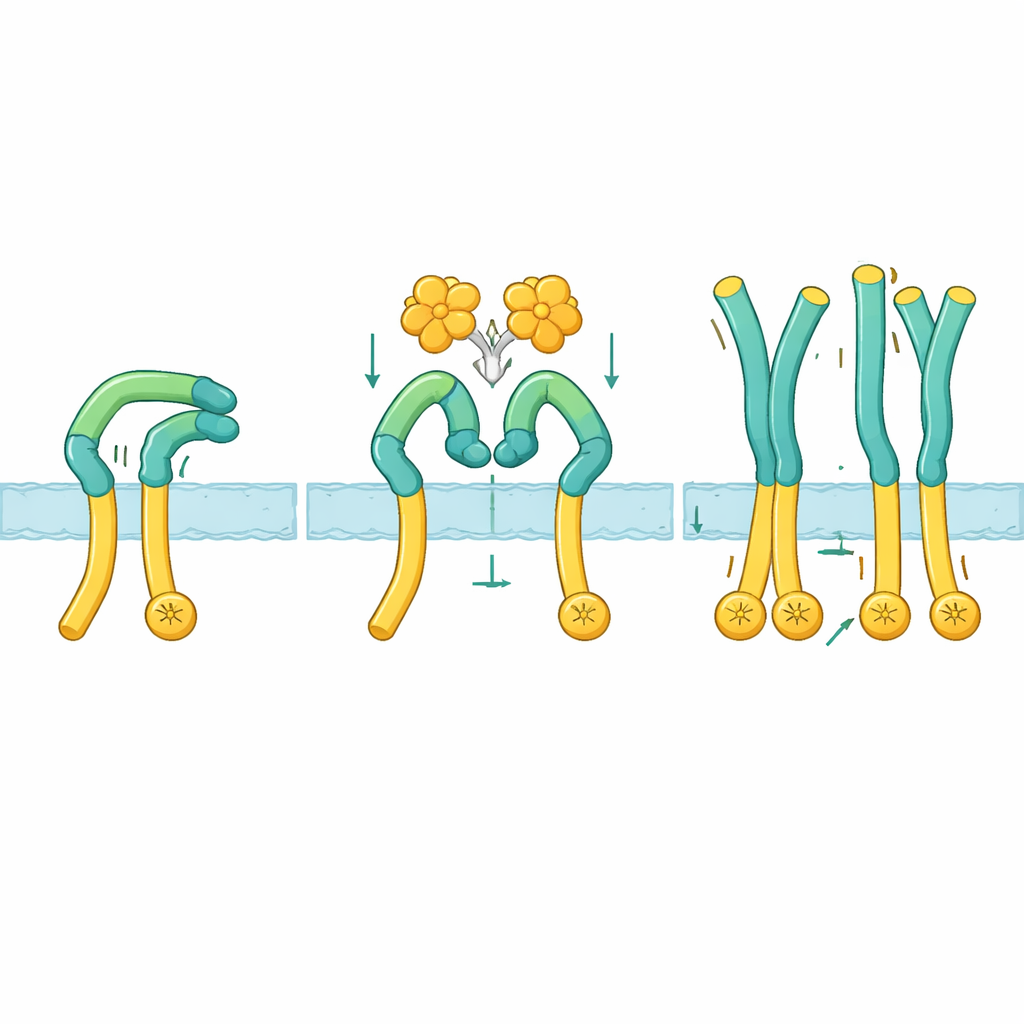
Um zu verstehen, wie diese Aktivierung tatsächlich funktioniert, verwendeten die Forscher Kryo‑Elektronenmikroskopie, um ROS1s Außendomäne allein und im Komplex mit NELL2 sichtbar zu machen. Im Ruhezustand klappt ROS1 auf sich selbst zurück: ein oberer „Arm“-Abschnitt biegt sich nach unten und klemmt gegen ein langes „Bein“, das zur Zellmembran führt. Diese gebogene Haltung hält den unteren Teil starr und scheint die inneren Enzymenden zu weit auseinander zu halten, um zu kommunizieren. Wenn NELL2 bindet, packt es drei verschiedene Stellen über mehrere Domänen des ROS1‑Arms. Diese Bindung führt nicht nur zur Clusterbildung mehrerer ROS1‑Moleküle, sie hebelt den Arm auch vom Bein weg und dreht ihn um etwa 130 Grad in eine aufrechtere Position. Sobald diese Klammer gelöst ist, wird das Bein flexibel, wodurch die membrannäheren Bereiche und damit die inneren Enzymteile dicht genug zusammenrücken können, um sich gegenseitig zu aktivieren.
Strukturelle Einsicht in Wirkstoffkandidaten verwandeln
Mit atomaren Karten dieser Konformationen suchten die Autorinnen und Autoren anschließend in Antikörper‑Bibliotheken nach im Labor erzeugten Antikörpern, die an ROS1s Außenseite haften. Sie fanden zwei verschiedene Typen. Ein Antikörper bindet genau dort, wo NELL2 zunächst andockt, blockiert den Liganden physisch und verhindert so die Aktivierung. Ein zweiter Antikörper verkeilt sich in den Spalt zwischen Arm und zentraler Schaltstelle von ROS1 und stabilisiert die ursprüngliche gebogene, geklemmte Konformation. Beide Antikörper unterdrückten ROS1‑vermittelte Signalwege in Zellen wirkungsvoll, obwohl ihre zwei Arme prinzipiell Rezeptoren zusammenführen könnten. Das zeigt: einfache Clusterbildung genügt nicht — die Aktivierung erfordert zwingend die von NELL2 ausgelöste Formänderung, die das Bein freigibt und den inneren Enzymen erlaubt, sich zu treffen.
Was das für künftige Krebstherapien bedeutet
Diese Arbeit zeigt, dass ROS1 durch ein zweistufiges Sicherheitssystem kontrolliert wird: Rezeptoren müssen durch ein Mehr‑Einheiten‑Signal zusammengezogen werden und zugleich eine große Formänderung durchlaufen, die eine interne Bremse löst. NELL2 erfüllt beide Funktionen, während die neu entdeckten Antikörper gezielt entweder den anfänglichen Griff oder die Entsperrbewegung stören. Für nicht fachkundige Leser lautet die Quintessenz: Wissenschaftler haben endlich einen natürlichen Schalter für ROS1 identifiziert und nahezu atomgenau kartiert, wie er einen Aus‑Zustand in einen Ein‑Zustand verwandelt. Diese Erkenntnisse bilden die Grundlage für die Entwicklung neuer biologischer Therapeutika, die ROS1 in Tumoren gezielt stumm schalten könnten, während andere zelluläre Schalter ungestört bleiben.
Zitation: Li, H., Zhang, J., Li, T. et al. Clustering and a conformational switch drive activation of the mammalian receptor tyrosine kinase ROS1. Nat Commun 17, 3657 (2026). https://doi.org/10.1038/s41467-026-69630-7
Schlüsselwörter: ROS1-Rezeptor, Rezeptor-Tyrosinkinase, Krebs-Signalgebung, NELL2-Ligand, therapeutische Antikörper