Clear Sky Science · zh
直接来自种子:通过从头 MicroED 获得的原子分辨率蛋白质结构
观察生命的最小构件
蛋白质是维持活细胞运行的微小机器,但要真正理解它们的工作原理,科学家需要以极高的清晰度看到它们的原子。本文描述了研究人员如何使用一种强大的电子方法,从直接来自碾碎植物种子的样品出发,在不依赖已有结构模型的情况下确定出原子级的蛋白质结构。他们的成功为研究那些抗拒传统技术、体积小或难以处理的蛋白质树立了新的标杆。
为什么微小晶体是个大问题
几十年来,X 射线晶体学一直是绘制蛋白质原子分辨率结构的主要工具。然而,它要求相对较大且高度有序的晶体——通常尺寸在几十到数百微米。许多重要蛋白天然只形成极小的晶体,远小于此尺寸,因此容易被标准方法漏掉。另一种常用方法——单粒子冷冻电子显微镜,对于较小的蛋白(尤其是接近人类蛋白典型大小的那些)也存在困难。合在一起,这些局限使得生物学中有很大一部分领域在结构上仍未被探索。
用电子代替 X 射线
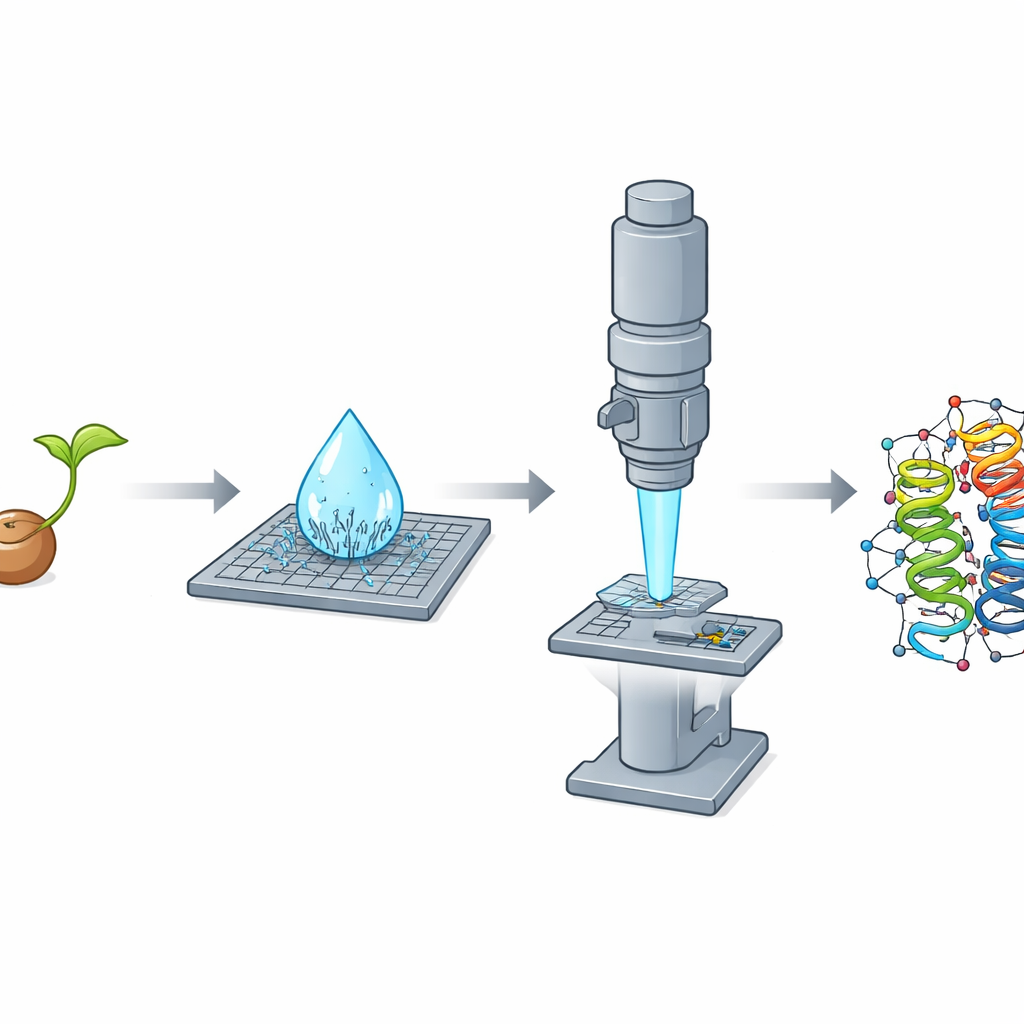
微晶体电子衍射(MicroED)通过使用电子而非 X 射线来解决这个问题。电子与物质的相互作用强得多,使得科学家能够从体积比 X 射线所需小数千倍的晶体中提取详细的结构信息。在这项研究中,团队聚焦于 crambin,这是一种存在于油籽植物 Crambe abyssinica 种子中的微小蛋白。长期以来,crambin 一直是先进晶体学方法的试验对象,早期利用 X 射线和中子束的工作将分辨率推向惊人的高度。然而,使用 MicroED 对 crambin 进行从头完整解析的研究尚未完全实现。
在干燥液滴中的偶然发现
在用一种简单的基于乙醇的程序从碾碎的种子中纯化 crambin 时,研究人员观察到一个引人注目的现象:当微升量的溶液滴在载玻片上干燥时,几秒钟内自发地产生了大量针状纳米晶体。这些细长晶体在 X 射线实验中表现不佳,但对于电子衍射几乎是理想的,因为它们在一个维度上极薄,从而对电子束透明。团队同时也培养出了传统的方块状晶体,这类晶体在 X 射线试验中表现优异,但即使研碎后对于 MicroED 来说仍然太厚。这种明显的反差——针状晶体对 X 射线不利但对电子有利,而方块状晶体则相反——凸显了晶体形状和厚度如何决定哪种方法更适用。
将许多针状晶体合成为一幅清晰图像
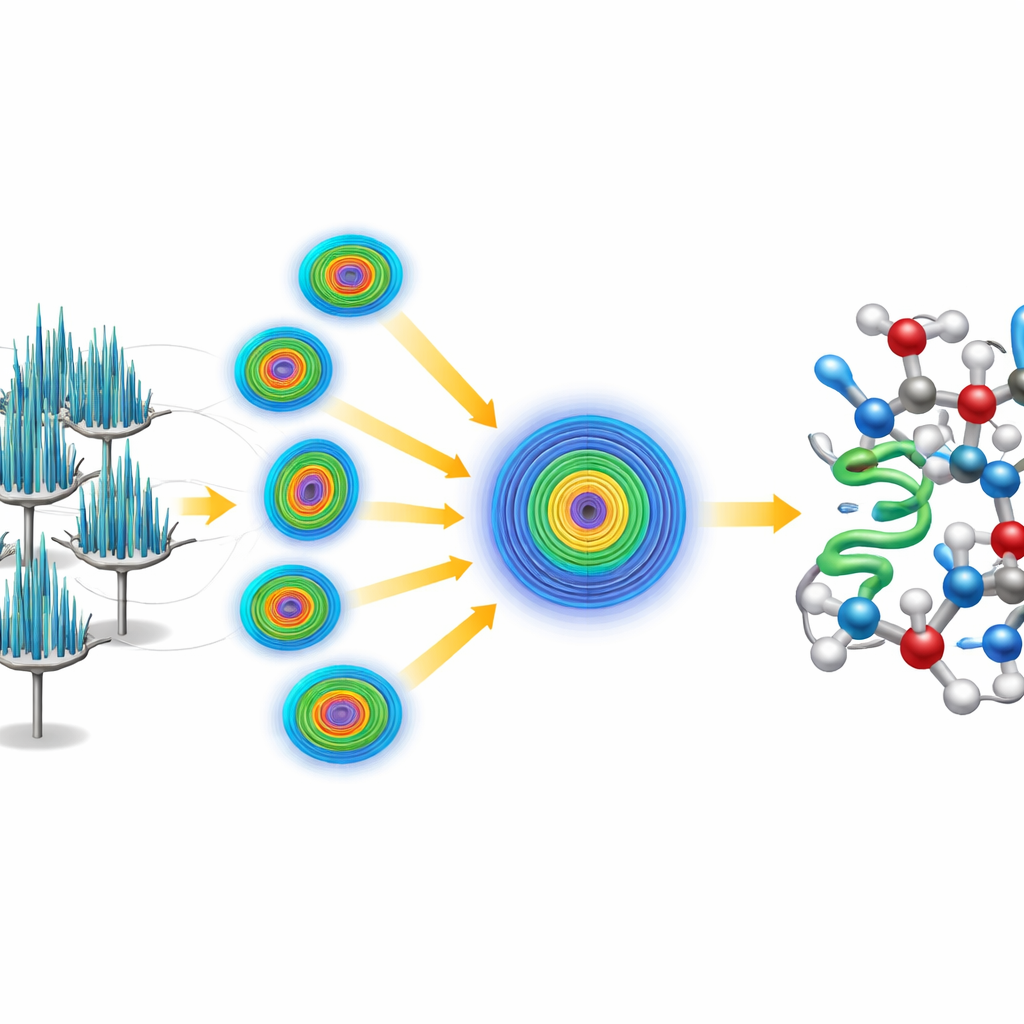
问题是:针状晶体在显微镜网格上往往以相同方向排列,这意味着任何单个晶体提供的都是不完整且具有方向性偏倚的蛋白视图。为了解决这一问题,研究人员采用了串行策略,从 58 个不同晶体收集小片段数据并将其合并为一个大型数据集。因为数据质量强烈依赖于观察方向,他们使用了一种专门的处理步骤,识别并裁剪掉在采样不足方向上弱且噪声大的测量,同时保留晶体衍射最强的方向上的有力信号。该处理产生了一个质量极高的数据集,分辨率优于一埃,细节足以显示单个原子,包括许多氢原子。
从头解决结构
研究团队没有依赖已有的 crambin 模型,而是挑战自己从“ab initio”(从头)求解结构。他们一开始只用一个非常微小、通用的五肽螺旋——本质上是一个短的、理想化的蛋白片段,与已知的 crambin 结构无关。利用已建立的软件,他们定位了这个片段在晶体重复格子中可能的位置,然后应用一种迭代的锐化程序,逐步改善由电子衍射得到的图像。精修后的电镜密度图变得足够清晰,自动化软件能够在无人为干预的情况下追踪完整的 crambin 链,得出一个完整的高分辨率模型。数据细致到研究人员能够区分并定量两种天然存在的 crambin 变体,它们仅在链上的两个位置不同。
这对未来研究意味着什么
这项工作表明,通过精心的数据采集和考虑各向异性的处理,仅使用自发形成的纳米晶体和标准电子显微镜硬件,就可以达到真正的原子分辨率并从头求解蛋白质结构。crambin 现在成为一个公开的基准数据集,其他科学家可以用它来测试新的分析方法、完善电子散射模型,并探索如氢键和电荷分布等现象。对非专业读者而言,关键结论是:强大的电子为本工具正在扩展结构生物学的能力,使得以往被认为过小、过脆或过于非典型而无法以原子细节研究的蛋白质,逐渐变得可视化可研究。}
引用: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
关键词: MicroED, 蛋白质结构, crambin, 电子衍射, 纳米晶体