Clear Sky Science · pl
Bezpośrednio z nasiona: struktura białka w rozdzielczości atomowej metodą ab initio MicroED
Widzieć najmniejsze cegiełki życia
Białka to niewielkie maszyny utrzymujące funkcjonowanie komórek żywych organizmów, ale aby naprawdę zrozumieć ich działanie, naukowcy muszą zobaczyć ich atomy z niezwykłą klarownością. W tym artykule opisano, jak badacze użyli silnej metody opartej na elektronach, aby wyznaczyć strukturę białka na poziomie atomowym, zaczynając bezpośrednio od zgniecionych nasion rośliny, bez polegania na wcześniejszych modelach strukturalnych. Ich sukces stanowi nowe odniesienie do badań nad małymi lub trudnymi białkami, które opierają się tradycyjnym technikom.
Dlaczego maleńkie kryształy są wielkim problemem
Przez dekady krystalografia rentgenowska była głównym narzędziem do mapowania struktur białek w rozdzielczości atomowej. Jednak wymaga ona relatywnie dużych, silnie uporządkowanych kryształów — często o rozmiarach od dziesiątek do setek mikrometrów. Wiele ważnych białek naturalnie tworzy jedynie mikroskopijne kryształy, znacznie mniejsze od tych wymagań, i dlatego umyka standardowym metodom. Inne popularne podejście, krioelektronowa mikroskopia pojedynczych cząstek, ma problemy z mniejszymi białkami, szczególnie tymi zbliżonymi rozmiarami do typowych białek ludzkich. Razem te ograniczenia pozostawiają dużą część biologii strukturalnej niezbadaną.
Użycie elektronów zamiast promieniowania rentgenowskiego
Elektronowa dyfrakcja mikrokrystaliczna, czyli MicroED, rozwiązuje ten problem, używając elektronów zamiast promieniowania rentgenowskiego. Elektrony oddziałują z materią znacznie silniej, co pozwala naukowcom wydobyć szczegółowe informacje strukturalne z kryształów o objętości tysiące razy mniejszej niż te wymagane do badań rentgenowskich. W tym badaniu zespół skoncentrował się na crambinie, niewielkim białku występującym w nasionach rośliny oleistej Crambe abyssinica. Crambin od dawna służył jako pole doświadczalne dla zaawansowanych metod krystalograficznych — wcześniejsze prace z użyciem promieni rentgenowskich i neutronów osiągały zdumiewające rozdzielczości. Niemniej jednak pełne, od podstaw badanie crambinu przy użyciu MicroED nie zostało wcześniej w pełni zrealizowane.
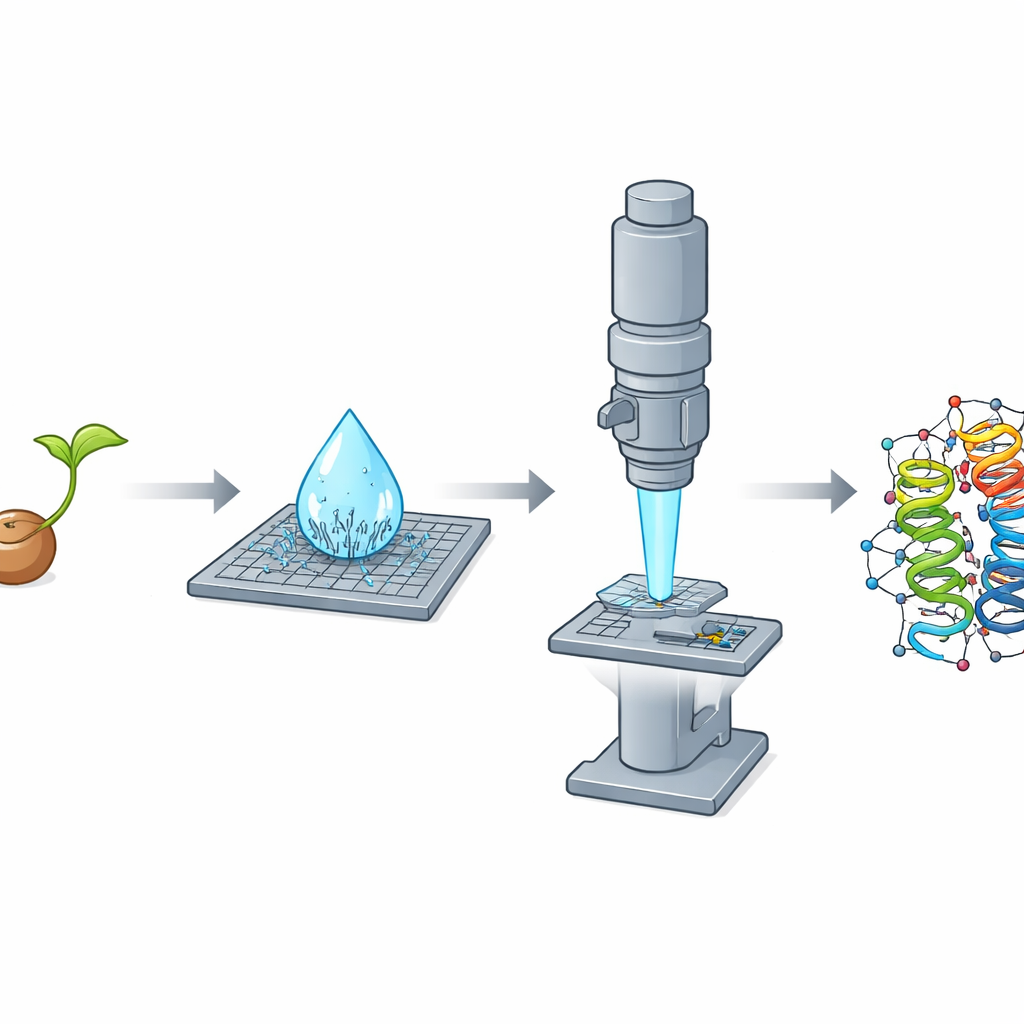
Szczęśliwe odkrycie w wysychającej kropli
Podczas oczyszczania crambinu z rozgniecionych nasion prostą procedurą na bazie etanolu badacze zaobserwowali zaskakujące zjawisko: gdy mikrolitrowa kropla roztworu wysychała na szkielecie, w ciągu sekund spontanicznie powstawał gęsty deszcz igiełkowatych nanokrystalików. Te cienkie płatki okazały się słabo nadające się do badań rentgenowskich, ale niemal idealne do dyfrakcji elektronowej, ponieważ były niezwykle cienkie w jednym wymiarze i przez to przezroczyste dla wiązki elektronów. Zespół także wyhodował tradycyjne, blokowe kryształy świetne do eksperymentów rentgenowskich, lecz zbyt grube do MicroED, nawet po rozkruszeniu. Ten wyraźny odwrót — igły złe dla rentgena, lecz doskonałe dla elektronów; bloki odwrotnie — podkreślił, jak kształt i grubość kryształu mogą decydować o przewadze danej metody.
Łączenie wielu igieł w jeden wyraźny obraz
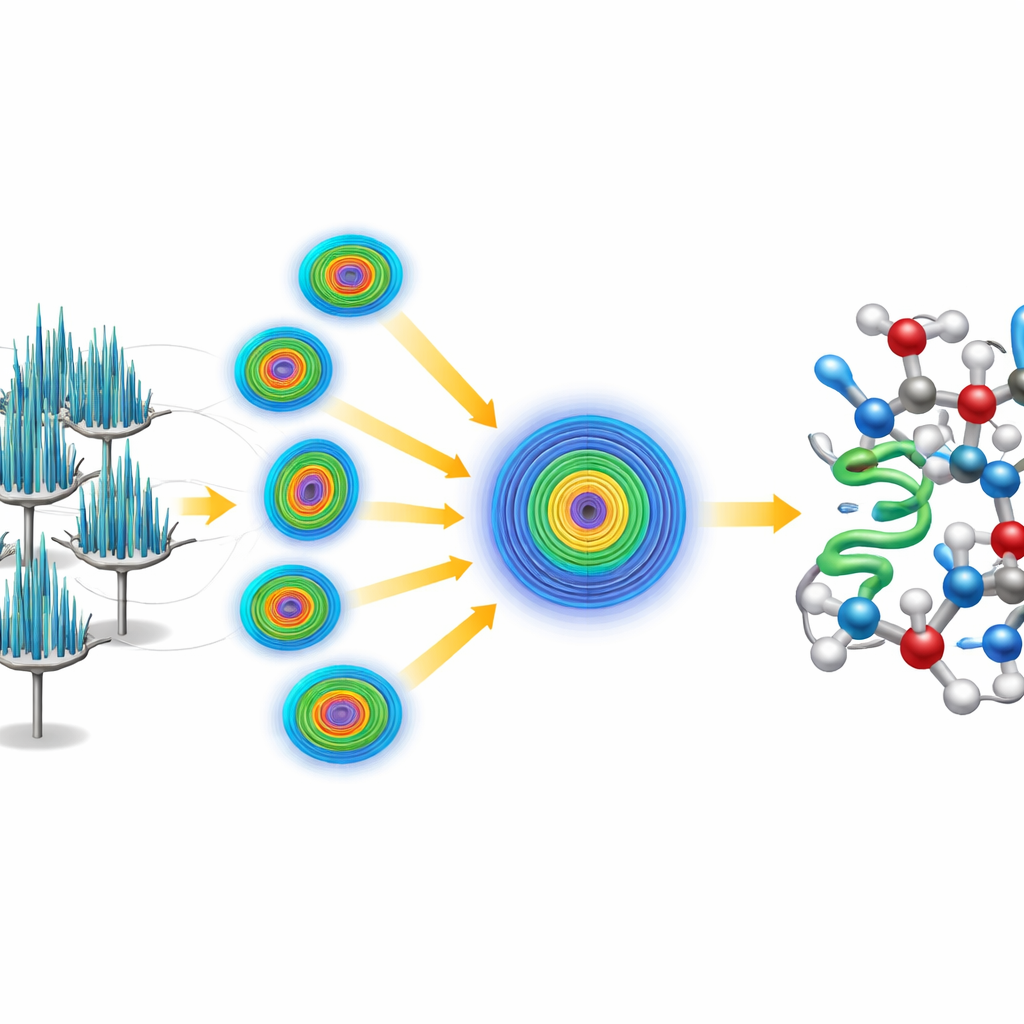
Był jednak haczyk: kryształy w postaci igieł miały tendencję do układania się w tej samej orientacji na siatce mikroskopu, co oznaczało, że pojedynczy kryształ dostarczał niepełnego i kierunkowo zniekształconego obrazu białka. Aby to obejść, badacze zastosowali strategię seryjną, zbierając krótkie porcje danych z 58 różnych kryształów i łącząc je w jeden duży zestaw danych. Ponieważ jakość danych silnie zależała od kierunku oglądu, użyli specjalizowanego kroku przetwarzania, który rozpoznaje i odrzuca słabe, zaszumione pomiary w słabo próbkowanych kierunkach, jednocześnie zachowując silne sygnały tam, gdzie kryształy najlepiej dyfraktowały. Takie podejście dało bardzo wysokiej jakości zbiór danych o rozdzielczości lepszej niż jeden angstrem, wystarczająco bogaty, by uwidocznić pojedyncze atomy, w tym wiele atomów wodoru.
Rozwiązanie struktury od podstaw
Zamiast opierać się na istniejącym modelu crambinu, zespół postawił sobie wyzwanie rozwiązania struktury „ab initio”, czyli od pierwszych zasad. Zaczęli jedynie od niewielkiej, ogólnej, pięcioaminokwasowej helisy — w istocie krótkiego, idealizowanego fragmentu białkowego niezwiązanego z znaną strukturą crambinu. Korzystając z ugruntowanego oprogramowania, zlokalizowali, gdzie ten fragment mógł pasować w powtarzalnym wzorze kryształu, a następnie zastosowali iteracyjną procedurę wyostrzania, która stopniowo polepszała mapę wyprowadzoną z danych elektronowych. Ulepszona mapa stała się na tyle czytelna, że zautomatyzowane oprogramowanie mogło odtworzyć cały łańcuch crambinu bez ingerencji człowieka, uzyskując kompletny model o wysokiej rozdzielczości. Dane były tak szczegółowe, że badacze mogli rozróżnić i ilościowo ocenić dwie naturalnie występujące warianty crambinu różniące się zaledwie w dwóch pozycjach łańcucha.
Co to oznacza dla przyszłych badań
Praca pokazuje, że przy starannym zbieraniu danych i przetwarzaniu uwzględniającym anizotropię możliwe jest osiągnięcie prawdziwej rozdzielczości atomowej i rozwiązanie struktury białka od podstaw używając wyłącznie spontanicznie powstałych nanokrystalików oraz standardowego sprzętu mikroskopu elektronowego. Crambin staje się teraz publicznym zbiorem odniesienia, którego inni naukowcy mogą używać do testowania nowych metod analizy, udoskonalania modeli rozpraszania elektronów oraz badania zjawisk takich jak wiązania wodorowe i rozkład ładunku. Dla czytelnika nietechnicznego kluczowy wniosek jest taki, że potężne, oparte na elektronach narzędzia rozszerzają zasięg biologii strukturalnej, czyniąc coraz bardziej realnym wizualizowanie najmniejszych detali białek, które kiedyś uważano za zbyt małe, zbyt kruche lub zbyt nietypowe, by badać je w szczegółach atomowych.
Cytowanie: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
Słowa kluczowe: MicroED, struktura białka, crambin, dyfrakcja elektronów, nanokrystaliki