Clear Sky Science · he
ישירות מן הזרע: מבנה חלבון ברזולוציה אטומית באמצעות MicroED מאפס
מציגים את אבני הבניין הקטנות ביותר של החיים
חלבונים הם המכונות הזעירות שמחזיקות תאים חיים בפעולה, אך כדי להבין באמת איך הם פועלים, מדענים צריכים לראות את האטומים שלהם בבהירות יוצאת דופן. מאמר זה מתאר כיצד חוקרים השתמשו בשיטה עוצמתית מבוססת אלקטרונים כדי לקבוע מבנה חלבון ברזולוציה אטומית, החל ישירות מזרעים מעוכתים של צמח, מבלי להיעזר במודלים מבניים קודמים. ההצלחה שלהם מציבה רף חדש ללימוד חלבונים קטנים או קשים שמסרבים לשיטות המסורתיות.
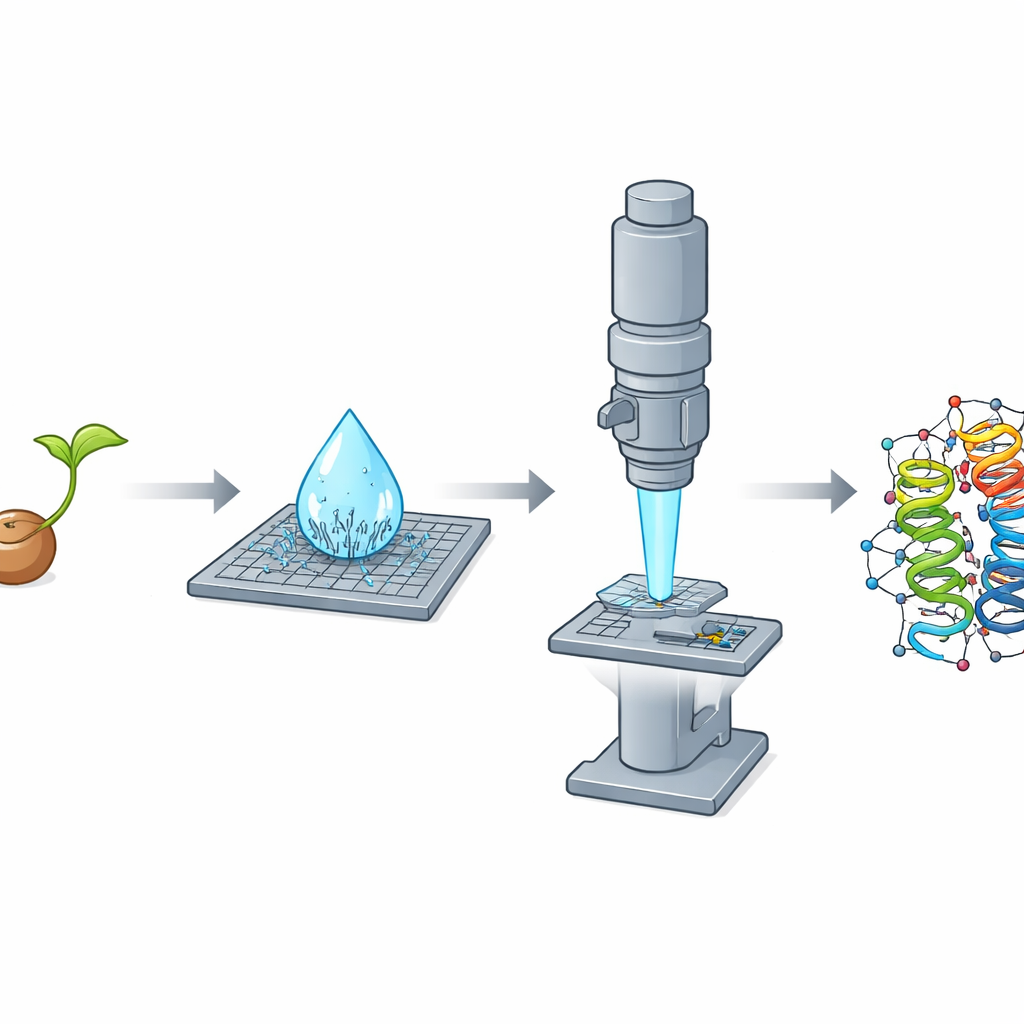
למה גבישים זעירים הם בעיה גדולה
בעשורים רבים, קריסטלוגרפיית קרני רנטגן הייתה הכלי העיקרי למיפוי מבני חלבונים ברזולוציה אטומית. עם זאת, היא דורשת גבישים יחסית גדולים ומאורגנים מאוד—לעתים עשרות עד מאות מיקרומטר. חלבונים חשובים רבים בוחרים ליצור רק גבישים זעירים בהרבה, וכתוצאה מכך נופלים מהצל של השיטות הסטנדרטיות. גישה פופולרית נוספת, קרי-אלקטרון מיקרוסקופיה של חלק בודד, מתקשה עם חלבונים קטנים יותר, ובפרט עם אלה בגודל טיפוסי של חלבוני אדם. יחד, מגבלות אלו משאירות שטח נרחב בביולוגיה ללא חקירה מבנית.
שימוש באלקטרונים במקום קרני רנטגן
דיפרקציית אלקטרונים של מיקרו-גבישים, או MicroED, מתמודדת עם הבעיה באמצעות אלקטרונים במקום קרני רנטגן. אלקטרונים מתקשרים עם החומר בעוצמה הרבה יותר גדולה, ומאפשרים לחוקרים להפיק מידע מבני מפורט מגבישים שנפחם קטן באלפי מונים מהנדרש לעבודה בקרני רנטגן. במחקר זה הקבוצה התמקדו בקרמבין, חלבון זעיר שנמצא בזרעי צמח השמן Crambe abyssinica. קרמבין שימש זמן רב כשטח ניסוי לשיטות קריסטלוגרפיות מתקדמות, כאשר עבודות קודמות באמצעות רנטגן ונויטרונים דחפו את הרזולוציה לרמות מרשימות. יחד עם זאת, חקירה מלאה מאפס של קרמבין באמצעות MicroED לא הושלמה במלואה עד כה.
גילוי נדיב בטיפה שמתייבשת
בעת טיהור קרמבין מזרעים מעוכתים בפרוצדורה פשוטה מבוססת אתנול, החוקרים שימו לב לתצפית מרשימה: כאשר טיפה של מיקרוליטר מהתמיסה התייבשה על שקף, היא ייצרה בתוך שניות שובל צפוף של ננו-גבישים בצורת מחטים. שברי המחטים האלו התגלה כי הם בעלי ביצועים חלשים לעבודה בקרני רנטגן אך כמעט אידיאליים לדיפרקציית אלקטרונים, מאחר שהם היו דקים מאוד בממד אחד ולכן שקופים לקרן האלקטרונים. הקבוצה גם גידלה גבישים מסורתיים בצורת משבצות שהצטיינו בניסויי רנטגן אך היו עבים מדי ל-MicroED, אפילו לאחר עיקור. ההיפוך הברור הזה—מחטים לקויות לקרני רנטגן אך מצוינות לאלקטרונים, ומשבצות להיפך—הדגיש כיצד צורת הגביש ועוביו יכולים לקבוע איזו שיטה תנצח.
שילוב מחטים רבות לתמונה ברורה אחת
ישנה בעייה: גבישי המחט נטו לשכב באותו כיוון על הרשת במיקרוסקופ, מה שאומר שכל גביש בודד סיפק מבט חסר ושל מכוון של החלבון. כדי להתגבר על כך אימצו החוקרים אסטרטגיה סדרתית, איסוף פרוסות קטנות של נתונים מ-58 גבישים שונים ומיזוגם למערך נתונים אחד גדול. מאחר שאיכות הנתונים תלויה בחוזקה בכיוון התצפית, השתמשו בצעד עיבוד מיוחד שמזהה וגוזם מדידות חלשות ורועשות בכיוונים שנותרו מדוללים, תוך שמירה על אותות חזקים היכן שהגבישים התפזרו היטב. טיפול זה הניב מערך נתונים באיכות גבוהה מאוד שהגיע לטוב מ-אחד-אנגסטרם ברזולוציה, עשיר מספיק כדי לגלות אטומים בודדים, כולל מימנים רבים.
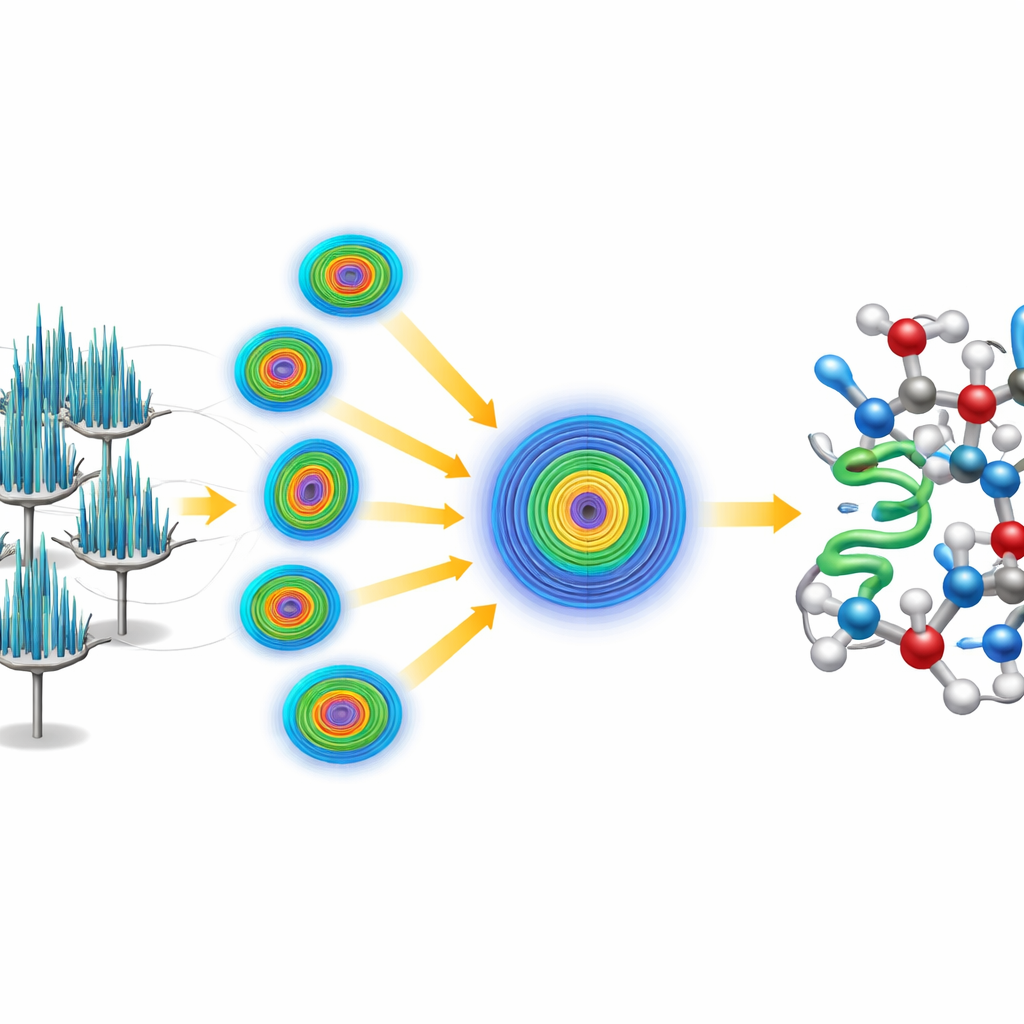
פתרון המבנה מאפס
במקום להישען על מודל קיים של קרמבין, הקבוצה אתגרה את עצמה לפתור את המבנה “ab initio”, או מעקרונות ראשוניים. הם התחילו רק עם הקטע הגלילי הגנרי הקצר של חמש חומצות אמינו—בע Essentially חלק חלבון אידיאליזטי קצר שאינו קשור למבנה הידוע של הקרמבין. באמצעות תוכנה מבוססת הם מצאו היכן קטע זה יכול לשבת באופן סביר בתבנית המחזורית של הגביש, ואז יישמו פרוצדורת החידוד החוזרת שעשתה בהדרגה את המפה הנובעת מהאלקטרונים לברורה יותר. המפה המופרת הפכה ברורה מספיק כדי שתוכנה אוטומטית תעקוב אחרי שרשרת הקרמבין כולה ללא התערבות ידנית, מה שהניב מודל מלא וברזולוציה גבוהה. הנתונים היו כל כך מפורטים שהחוקרים יכלו להבחין ולכמת שתי וריאנטים טבעיים של קרמבין השונים רק בשתי עמדות בשרשרת.
מה משמעות הדבר למחקרים עתידיים
העבודה ממחישה כי, עם איסוף נתונים זהיר ועיבוד המודע לאנסטרופיה (אי-סימטריה בכיווניות), ניתן להגיע לרזולוציה אטומית אמיתית ולפתור מבנה חלבון מאפס באמצעות ננו-גבישים שהתפתחו ספונטנית וחומרה סטנדרטית של מיקרוסקופ אלקטרונים. קרמבין כעת עומד כסטנדרט ציבורי של מערך נתונים שאיתו מדענים אחרים יכולים לבדוק שיטות ניתוח חדשות, לחדד מודלים של פיזור אלקטרונים ולחקור תופעות כגון קשרי מימן והתפלגות מטען. עבור קהל שאינו מומחה, המסקנה המרכזית היא שכלי אלקטרון עוצמתיים חדשים מרחיבים את טווח הביולוגיה המבנית, ובכך הופכים לנגיש יותר ויותר היכולת לדמיין את הפרטים הקטנים ביותר של חלבונים שנחשבו פעם לקטנים מדי, שבריריים מדי או לא שגרתיים כדי לחקור אותם ברזולוציה אטומית.
ציטוט: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
מילות מפתח: MicroED, מבנה חלבון, קרמבין, ביחון אלקטרוני, ננו-גבישים