Clear Sky Science · tr
Tohumdan doğrudan: ab initio MicroED ile atom çözünürlüklü bir protein yapısı
Yaşamın En Küçük Yapıtaşlarını Görmek
Proteinler, canlı hücreleri çalıştıran küçük makineler gibidir; ancak bunların nasıl işlediğini gerçekten anlamak için bilim insanlarının atomlarını olağanüstü bir netlikle görmesi gerekir. Bu makale, araştırmacıların güçlü bir elektron tabanlı yöntem kullanarak öğütülmüş bitki tohumlarından doğrudan, önceki yapısal modellerden bağımsız şekilde atom düzeyinde bir protein yapısını nasıl belirlediklerini anlatıyor. Elde ettikleri başarı, geleneksel tekniklere dirençli, küçük veya zor proteinleri incelemek için yeni bir kıyas noktası sunuyor.
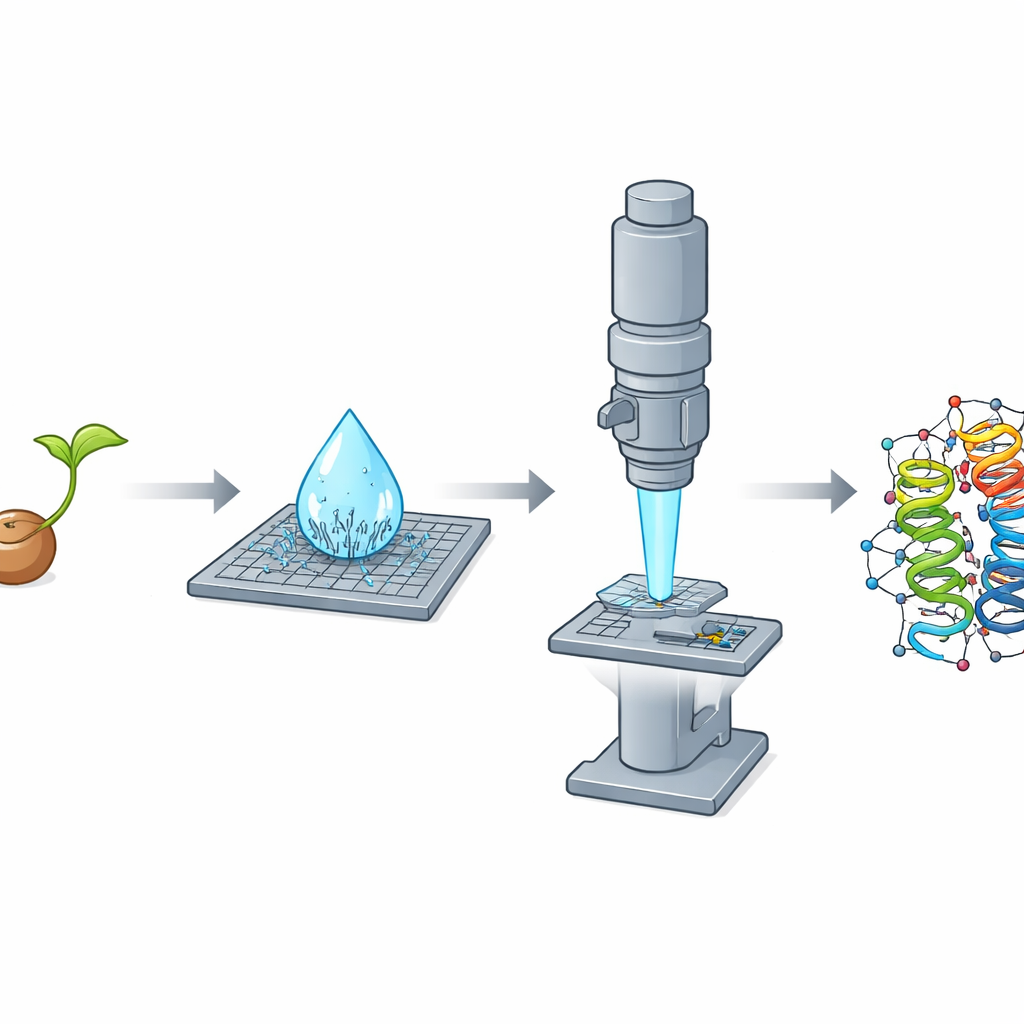
Neden Küçük Kristaller Büyük Bir Sorun Oluşturuyor
On yıllardır atom çözünürlüğünde protein yapılarının haritalanmasında ana araç X-ışını kristalografisidir. Ancak bu yöntem nispeten büyük, yüksek derecede düzenli kristaller—çoğunlukla onlarla yüzlerce mikrometre aralığında—gerektirir. Birçok önemli protein doğal olarak yalnızca çok küçük kristaller oluşturur, bunlar bu boyuttan çok daha küçüktür ve standart yöntemlerin ağından kaçıp gider. Başka popüler bir yaklaşım olan tek parçacıklı kriyo-elektron mikroskobu ise özellikle insan proteinlerinin tipik boyutlarına yakın olan daha küçük proteinlerle zorlanır. Bu sınırlamalar birlikte biyolojinin geniş bir kesimini yapısal olarak keşfedilmemiş bırakıyor.
X-Işınları Yerine Elektron Kullanmak
Microcrystal elektron kırınımı veya MicroED, bu sorunu X-ışınları yerine elektronlar kullanarak çözer. Elektronlar madde ile çok daha güçlü etkileşime girer; bu sayede bilim insanları X-ışını çalışmalarında gereken hacimden binlerce kat daha küçük kristallerden ayrıntılı yapısal bilgi çıkarabilirler. Bu çalışmada ekip, yağlı tohum bitkisi Crambe abyssinica tohumlarında bulunan küçük bir protein olan crambin üzerinde yoğunlaştı. Crambin, gelişmiş kristalografik yöntemlerin test alanı olarak uzun süredir kullanılmış; önceki X-ışını ve nötron çalışmaları olağanüstü çözünürlüklere ulaşmıştır. Buna karşın, MicroED kullanılarak crambin’in sıfırdan tam bir çözümü tam anlamıyla gerçekleştirilmemişti.
Kuruyan Bir Damladaki Şanslı Keşif
Crambin’i öğütülmüş tohumlardan basit bir etanol bazlı prosedürle arıtırken araştırmacılar çarpıcı bir gözlem yaptı: çözeltinin mikrolitre büyüklüğündeki bir damlası lam üzerine kururken birkaç saniye içinde iğne şeklinde yoğun bir nanokristal yağmuru oluşturdu. Bu ince parçalar X-ışını çalışmaları için kötü performans gösterirken elektron kırınımı için neredeyse ideal çıktılar, çünkü bir boyutta son derece incediler ve bu nedenle elektron ışınına karşı saydamdılar. Ekip ayrıca X-ışını deneylerinde mükemmel olan ama MicroED için, ezildikten sonra bile çok kalın kalan geleneksel, blok benzeri kristaller de büyüttü. Bu net terslik—iğnelerin X-ışınları için kötü, elektronlar için mükemmel; blokların ise tam tersi—kristal şekli ve kalınlığının hangi yöntemin üstün geleceğini nasıl belirleyebileceğini vurguladı.
Birçok İğneyi Birleştirip Tek Bir Net Görüntü Elde Etmek
Bir sorun vardı: iğne kristaller mikroskop ızgarası üzerinde genelde aynı yönde yatma eğilimindeydi, bu da tek bir kristalin proteine eksiksiz ve yönsel olarak tarafsız bir görüş vermesini engelliyordu. Bunu aşmak için araştırmacılar seri bir strateji benimsediler; 58 farklı kristalden küçük veri dilimleri topladılar ve bunları tek bir büyük veri kümesinde birleştirdiler. Veri kalitesi izleme yönüne güçlü biçimde bağlı olduğundan, kötü örneklenen yönlerde zayıf, gürültülü ölçümleri tanıyan ve budayan, kristallerin en iyi kırınım verdiği güçlü sinyalleri ise koruyan özel bir işleme adımı kullandılar. Bu işlem, bireysel atomları, birçok hidrojen de dahil olmak üzere açığa çıkaracak kadar zengin, bir ångström’den daha iyi çözünürlüğe ulaşan çok yüksek kaliteli bir veri kümesi üretti.
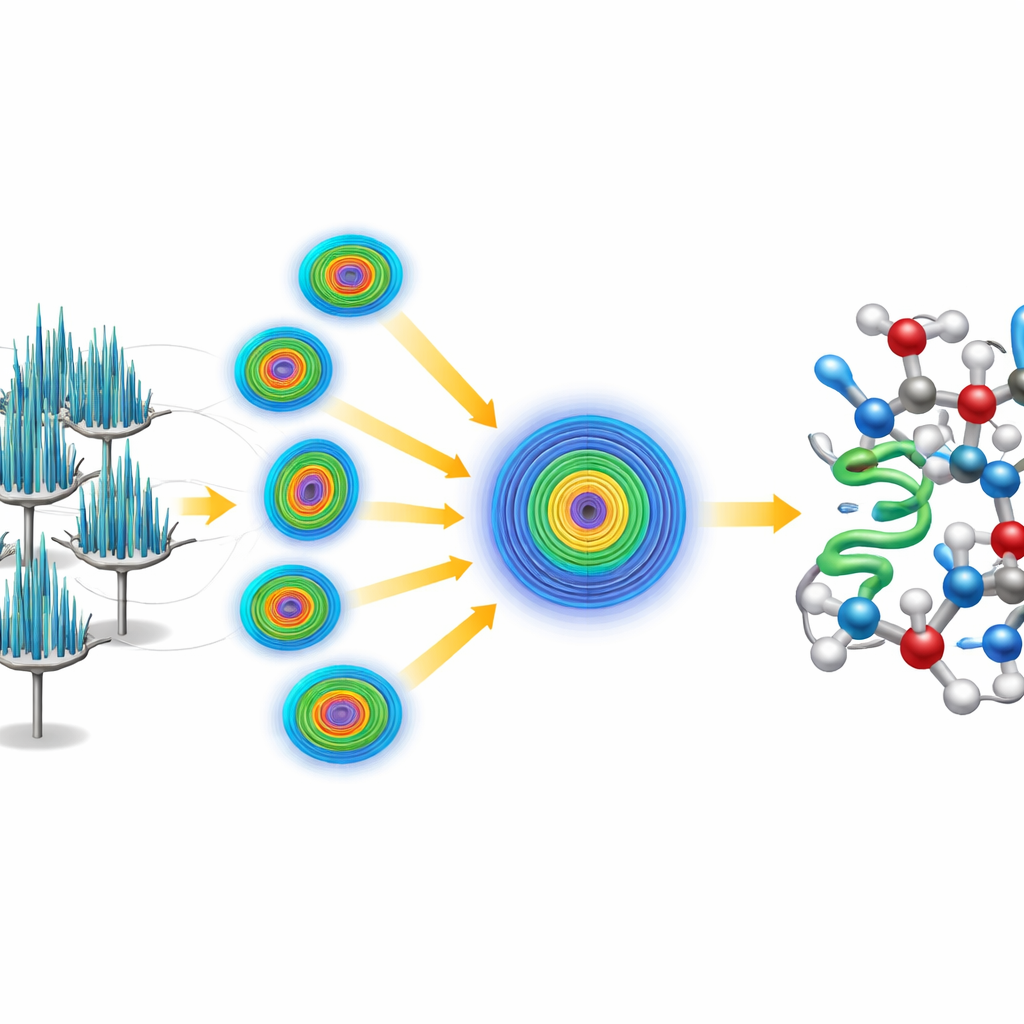
Yapıyı Baştan Çözmek
Crambin’in mevcut bir modeline yaslanmak yerine ekip kendine meydan okudu ve yapıyı “ab initio”, yani ilkelerden başlayarak çözmeyi denedi. Bunun için yalnızca çok küçük, beş amino asitlik genel bir heliksle başladılar—temelde crambin’in bilinen yapısıyla ilişkili olmayan kısa, idealize edilmiş bir protein fragmanı. Yerleşik yazılımlar kullanarak bu fragmanın kristalin tekrar eden düzeni içinde makul bir şekilde nerede bulunabileceğini tespit ettiler, ardından elektron kaynaklı haritayı kademeli olarak iyileştiren yinelemeli bir keskinleştirme prosedürü uyguladılar. İyileştirilmiş harita, otomatik yazılımların insan müdahalesine gerek kalmadan tüm crambin zincirini izlemesine yetecek kadar netleşti ve böylece eksiksiz, yüksek çözünürlüklü bir model elde edildi. Veriler o kadar ayrıntılıydı ki araştırmacılar zincirde yalnızca iki pozisyonda farklılık gösteren doğal olarak oluşan iki crambin varyantını ayırt edip nicel olarak belirleyebildiler.
Gelecek Çalışmalar İçin Anlamı
Bu çalışma gösteriyor ki dikkatli veri toplama ve anizotropi farkındalıklı işleme ile, yalnızca kendiliğinden oluşmuş nanokristaller ve standart elektron mikroskobu donanımı kullanılarak gerçek atom çözünürlüğüne ulaşmak ve bir protein yapısını sıfırdan çözmek mümkün. Crambin artık diğer bilim insanlarının yeni analiz yöntemlerini test edebileceği, elektron saçılması modellerini rafine edebileceği ve hidrojen bağları ile yük dağılımı gibi olguları keşfedebileceği halka açık bir kıyas veri seti olarak duruyor. Uzman olmayanlar için alınacak ana mesaj şudur: güçlü yeni elektron tabanlı araçlar yapısal biyolojinin erişimini genişletiyor ve bir zamanlar çok küçük, çok kırılgan veya çok alışılmadık olduğu için atom düzeyinde çalışılamaz sayılan proteinlerin en küçük ayrıntılarını görselleştirmeyi giderek daha mümkün kılıyor.
Atıf: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
Anahtar kelimeler: MicroED, protein yapısı, crambin, elektron kırınımı, nanokristaller