Clear Sky Science · de
Direkt aus dem Samen: eine Proteinstruktur mit atomarer Auflösung durch ab initio MicroED
Die kleinsten Bausteine des Lebens sehen
Proteine sind die winzigen Maschinen, die lebende Zellen am Laufen halten. Um jedoch wirklich zu verstehen, wie sie funktionieren, müssen Wissenschaftler ihre Atome mit außerordentlicher Klarheit sehen. Dieser Artikel beschreibt, wie Forschende eine leistungsstarke, auf Elektronen basierende Methode nutzten, um eine Proteinstruktur auf atomarer Ebene direkt aus zermahlenen Pflanzensamen zu bestimmen, ohne auf vorhandene Strukturmodelle zurückzugreifen. Ihr Erfolg setzt einen neuen Maßstab für die Untersuchung kleiner oder problematischer Proteine, die traditionellen Techniken widerstehen.
Warum winzige Kristalle ein großes Problem sind
Jahrzehntelang war die Röntgenkristallographie das wichtigste Werkzeug zur Kartierung von Proteinstrukturen mit atomarer Auflösung. Sie erfordert jedoch vergleichsweise große, hoch geordnete Kristalle – oft einige zehn bis mehrere hundert Mikrometer groß. Viele wichtige Proteine bilden natürlicherweise nur winzige Kristalle, die deutlich kleiner sind und daher den Standardmethoden entgehen. Ein weiterer verbreiteter Ansatz, die Einzelpartikel-Kryo-Elektronenmikroskopie, hat bei kleineren Proteinen, insbesondere solchen in der Größenordnung typischer menschlicher Proteine, Schwierigkeiten. Zusammen führen diese Einschränkungen dazu, dass ein großer Bereich der Biologie strukturell unerforscht bleibt.
Elektronen statt Röntgenstrahlen verwenden
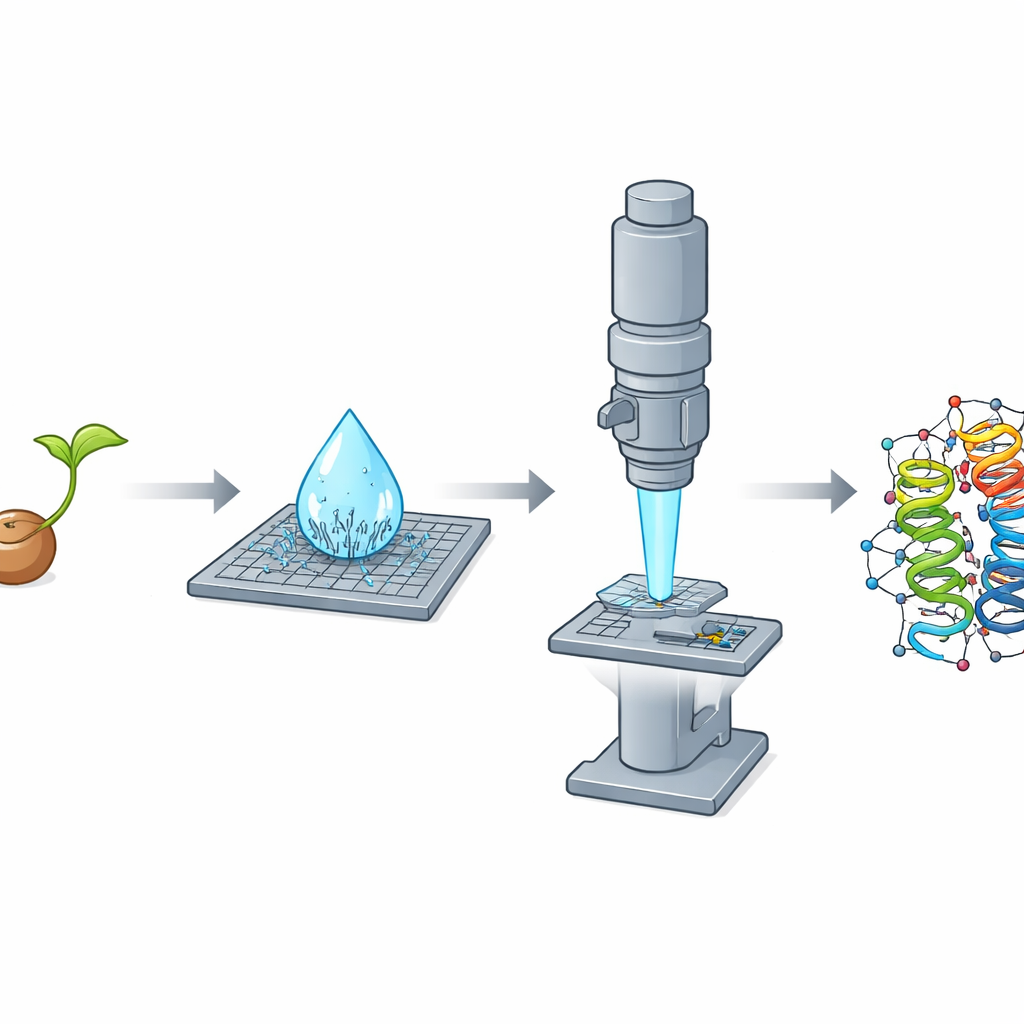
Die Mikro-Kristall-Elektronenbeugung, oder MicroED, begegnet diesem Problem, indem sie Elektronen statt Röntgenstrahlen verwendet. Elektronen wechselwirken viel stärker mit Materie, sodass Wissenschaftler detaillierte strukturelle Informationen aus Kristallen gewinnen können, die im Volumen tausendfach kleiner sind als für Röntgenmessungen erforderliche Kristalle. In dieser Studie konzentrierte sich das Team auf Crambin, ein kleines Protein, das in den Samen der Ölpflanze Crambe abyssinica vorkommt. Crambin dient seit langem als Prüfobjekt für fortgeschrittene kristallographische Methoden; frühere Arbeiten mit Röntgenstrahlen und Neutronen erreichten erstaunliche Auflösungen. Eine vollständige, von Grund auf mit MicroED durchgeführte Untersuchung von Crambin war jedoch bislang nicht vollständig realisiert worden.
Ein glücklicher Fund in einem trocknenden Tropfen
Bei der Reinigung von Crambin aus zermahlenen Samen mittels eines einfachen ethanolbasierten Verfahrens machten die Forschenden eine auffällige Beobachtung: Während ein mikroliterkleiner Tropfen der Lösung auf einem Objektträger trocknete, bildete er innerhalb von Sekunden spontan einen dichten Schauer nadelartiger Nanokristalle. Diese dünnen Kristalle zeigten sich für Röntgenmessungen ungeeignet, waren jedoch für die Elektronenbeugung nahezu ideal, weil sie in einer Dimension extrem dünn und damit für den Elektronenstrahl durchsichtig waren. Das Team züchtete zudem traditionelle, blockartige Kristalle, die sich für Röntgenexperimente hervorragend eigneten, aber selbst nach dem Zerkleinern zu dick für MicroED waren. Diese klare Umkehrung – Nadeln schlecht für Röntgen, hervorragend für Elektronen; Blöcke umgekehrt – machte deutlich, wie Form und Dicke der Kristalle darüber entscheiden, welche Methode zum Erfolg führt.
Viele Nadeln zu einem klaren Bild vereinen
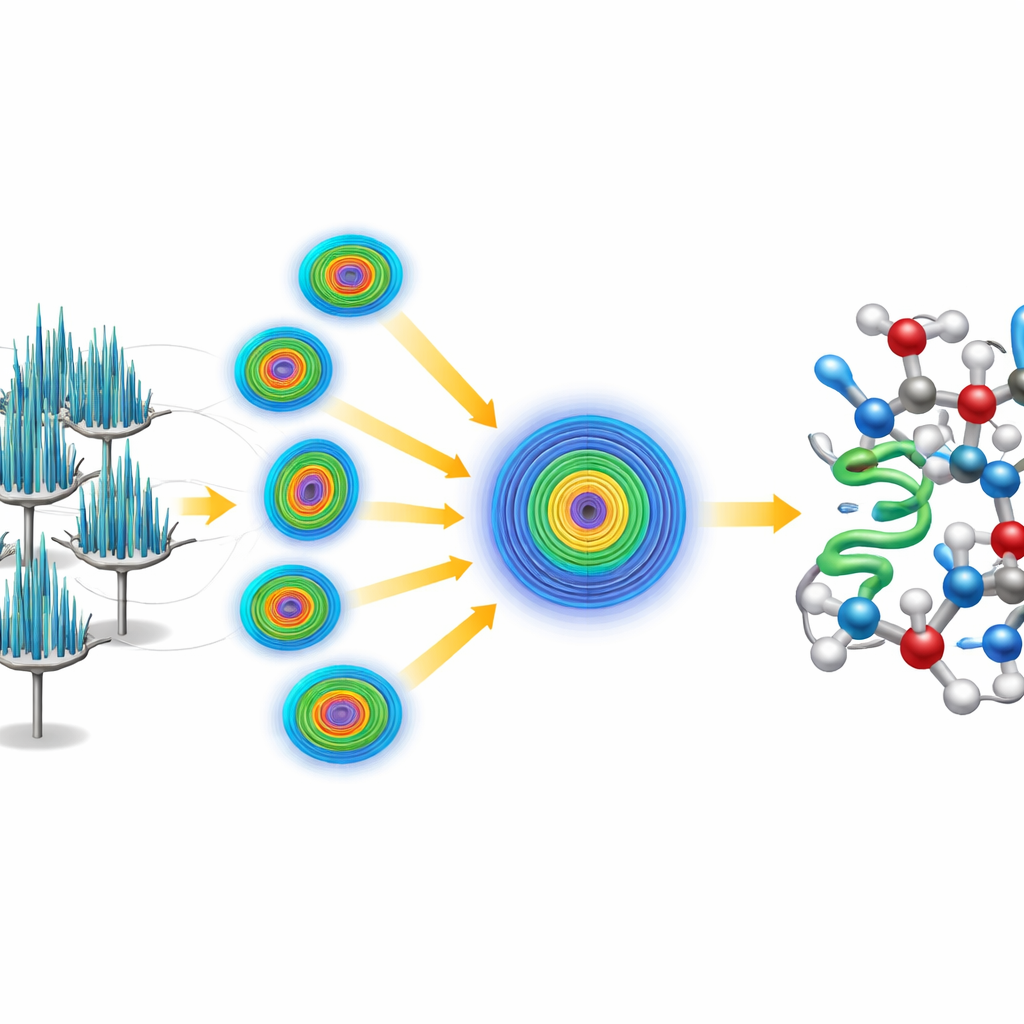
Es gab einen Haken: Die Nadelkristalle lagen auf dem Raster des Mikroskops oft in derselben Orientierung, sodass ein einzelner Kristall nur eine unvollständige und richtungsbedingt verzerrte Sicht auf das Protein lieferte. Um das zu umgehen, verfolgten die Forschenden eine serielle Strategie: Sie sammelten kleine Datenabschnitte von 58 verschiedenen Kristallen und fassten diese zu einem großen Datensatz zusammen. Da die Datenqualität stark von der Blickrichtung abhing, verwendeten sie einen spezialisierten Verarbeitungsschritt, der schwache, verrauschte Messwerte in schlecht abgedeckten Richtungen erkennt und entfernt, während starke Signale aus gut diffraktierenden Richtungen erhalten bleiben. Diese Behandlung ergab einen sehr hochwertigen Datensatz mit besser als einem Ångström Auflösung, reich genug, um einzelne Atome sichtbar zu machen, einschließlich vieler Wasserstoffe.
Die Struktur von Grund auf lösen
Anstatt sich auf ein bestehendes Modell von Crambin zu stützen, stellten sich die Forschenden der Herausforderung, die Struktur „ab initio“, also von ersten Prinzipien, zu lösen. Sie begannen lediglich mit einer winzigen, generischen Helix aus fünf Aminosäuren – im Wesentlichen einem kurzen, idealisierten Proteinfragment ohne Bezug zur bekannten Crambin-Struktur. Mit etablierter Software lokalisierten sie, wo dieses Fragment plausibel in das periodische Muster des Kristalls passen könnte, und wandten dann ein iteratives Schärfungsverfahren an, das die aus Elektronen gewonnenen Karten schrittweise verbesserte. Die verfeinerte Karte wurde so deutlich, dass automatisierte Programme die gesamte Crambin-Kette ohne menschliches Eingreifen nachverfolgen konnten und ein vollständiges, hochaufgelöstes Modell entstand. Die Daten waren so detailliert, dass die Forschenden zwei natürlich vorkommende Varianten von Crambin unterscheiden und quantifizieren konnten, die sich nur an zwei Positionen der Kette unterscheiden.
Was das für künftige Studien bedeutet
Die Arbeit zeigt, dass es mit sorgfältiger Datenerfassung und anisotropie-bewusster Verarbeitung möglich ist, echte atomare Auflösung zu erreichen und eine Proteinstruktur von Grund auf allein mit spontan gebildeten Nanokristallen und standardmäßiger Elektronenmikroskop-Hardware zu lösen. Crambin dient nun als öffentlich verfügbares Referenzdatenset, das andere Wissenschaftler nutzen können, um neue Analysemethoden zu testen, Modelle der Elektronenstreuung zu verfeinern und Phänomene wie Wasserstoffbrücken und Ladungsverteilung zu untersuchen. Für Nicht‑Spezialisten lautet die Kernbotschaft: Leistungsfähige, auf Elektronen basierende Werkzeuge erweitern das Spektrum der Strukturbiologie und machen es zunehmend möglich, die kleinsten Details von Proteinen sichtbar zu machen, die früher als zu klein, zu fragil oder zu unkonventionell galten, um sie atomar zu untersuchen.
Zitation: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
Schlüsselwörter: MicroED, Proteinstruktur, Crambin, Elektronenbeugung, Nanokristalle