Clear Sky Science · ja
種子そのままから:ab initio MicroED による原子分解能のタンパク質構造
生命の最小構成要素を観る
タンパク質は細胞を動かす小さな機械ですが、その働きを本当に理解するには、原子レベルで極めて明瞭に観察する必要があります。本稿は、研究者たちが強力な電子線ベースの手法を用い、粉砕した植物の種子から直接出発して先行構造モデルに頼らずに原子レベルのタンパク質構造を決定した経緯を説明します。彼らの成功は、従来の手法に抵抗する小さなタンパク質や解析が難しいタンパク質を研究するための新たな基準を示します。
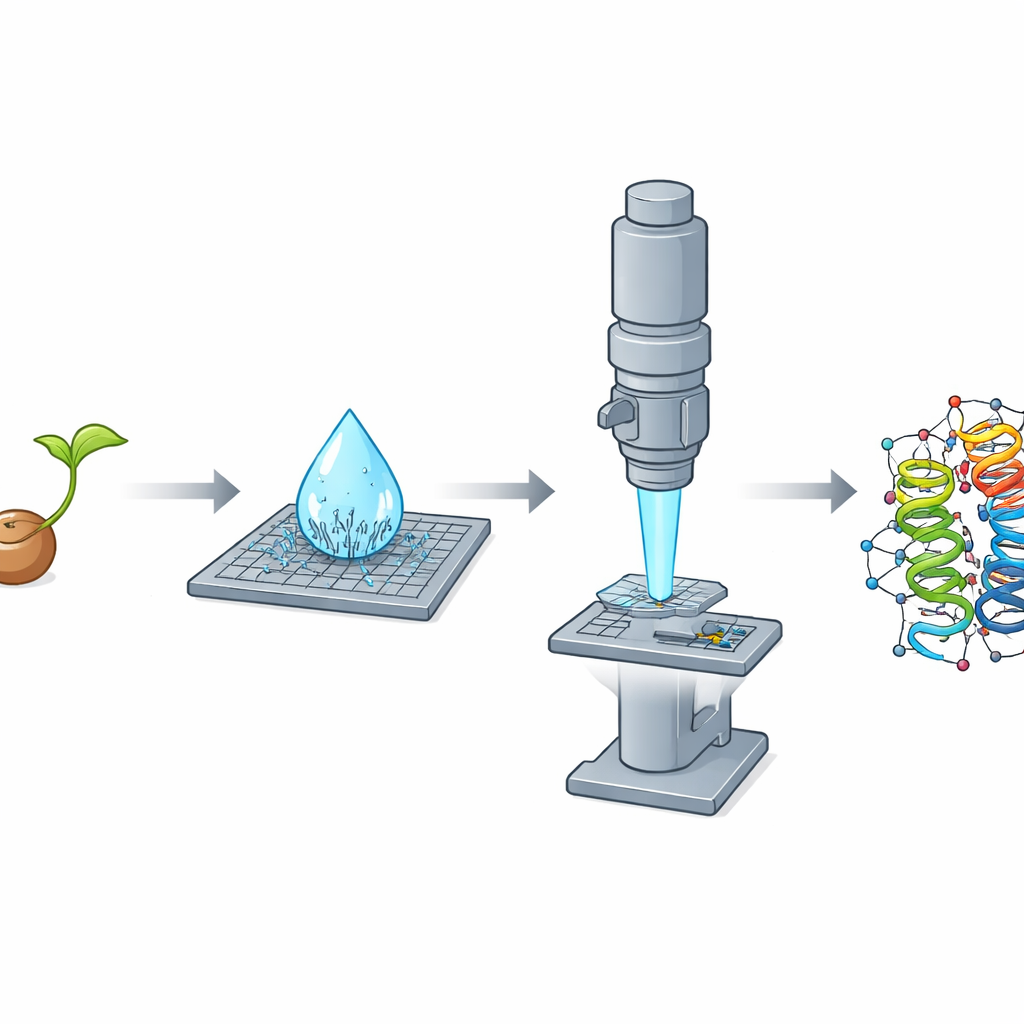
なぜ小さな結晶が大きな問題なのか
何十年ものあいだ、X線結晶構造解析は原子分解能でタンパク質構造を明らかにする主要手段でした。しかしそれは比較的大きく、非常に秩序だった結晶――しばしば数十〜数百マイクロメートルに達する――を必要とします。多くの重要なタンパク質は自然に非常に小さな結晶しか作らず、そのため標準的な手法では取りこぼされてきました。別の人気ある手法である単粒子クライオ電子顕微鏡も、特にヒトタンパク質に典型的なサイズに近い小さなタンパク質では苦戦します。これらの制約が重なり、構造的に未踏の生物学的領域が広く残される結果となっています。
X線ではなく電子を使う
マイクロ結晶電子回折(MicroED)は、この問題に電子を使うことで対処します。電子は物質と強く相互作用するため、X線で必要とされる体積より何千倍も小さい結晶から詳細な構造情報を取り出すことができます。本研究では、研究チームは油糧種子の一種であるCrambe abyssinicaの種子に含まれる小さなタンパク質、クランビンに注目しました。クランビンは高度な結晶学的手法の試験対象として長く使われており、以前のX線や中性子を用いた研究が驚異的な解像度を達成してきました。それでも、MicroEDを用いて完全にゼロから(from-scratch)クランビンを調べる試みは十分には実現していませんでした。
乾く一滴の中での幸運な発見
種子を粉砕してエタノールを基本とした簡便な精製を行っているとき、研究者たちは目を引く観察をしました。スライド上でマイクロリットル単位の液滴が乾くと、数秒のうちに針状のナノ結晶が密にシャワーのように自発的に生じたのです。これらの細片はX線実験には不向きでしたが、非常に薄い一方向性を持ち電子線に対してはほぼ理想的であることがわかりました。チームはまた、X線実験で優れる伝統的なブロック状結晶も育てましたが、それらはMicroEDには厚すぎ、粉砕しても適さなかったのです。この明確な逆転――針状はX線に不利だが電子には優れる、ブロックはその逆――は、結晶の形と厚さがどの方法が有利かを決定づけることを際立たせました。
多数の針を組み合わせて一つの鮮明な像に
ひとつ問題がありました。針状結晶は顕微鏡グリッド上で同じ向きに並ぶ傾向があり、個々の結晶からは不完全で方向的に偏った情報しか得られません。これを克服するために、研究者たちは逐次(シリアル)戦略を採用し、58個の異なる結晶から小さなデータ切片を収集してそれらを一つの大きなデータセットに統合しました。データ品質は観測方向に強く依存したため、彼らは特殊な処理ステップを用い、サンプリングが不十分な方向の弱くノイズの多い測定を識別して切り捨て、結晶が最もよく回折した方向の強い信号を保持しました。この処理により、1オングストロームより良い解像度に達する非常に高品質なデータセットが得られ、個々の原子、さらには多くの水素原子までも明らかにできるほどの情報が得られました。
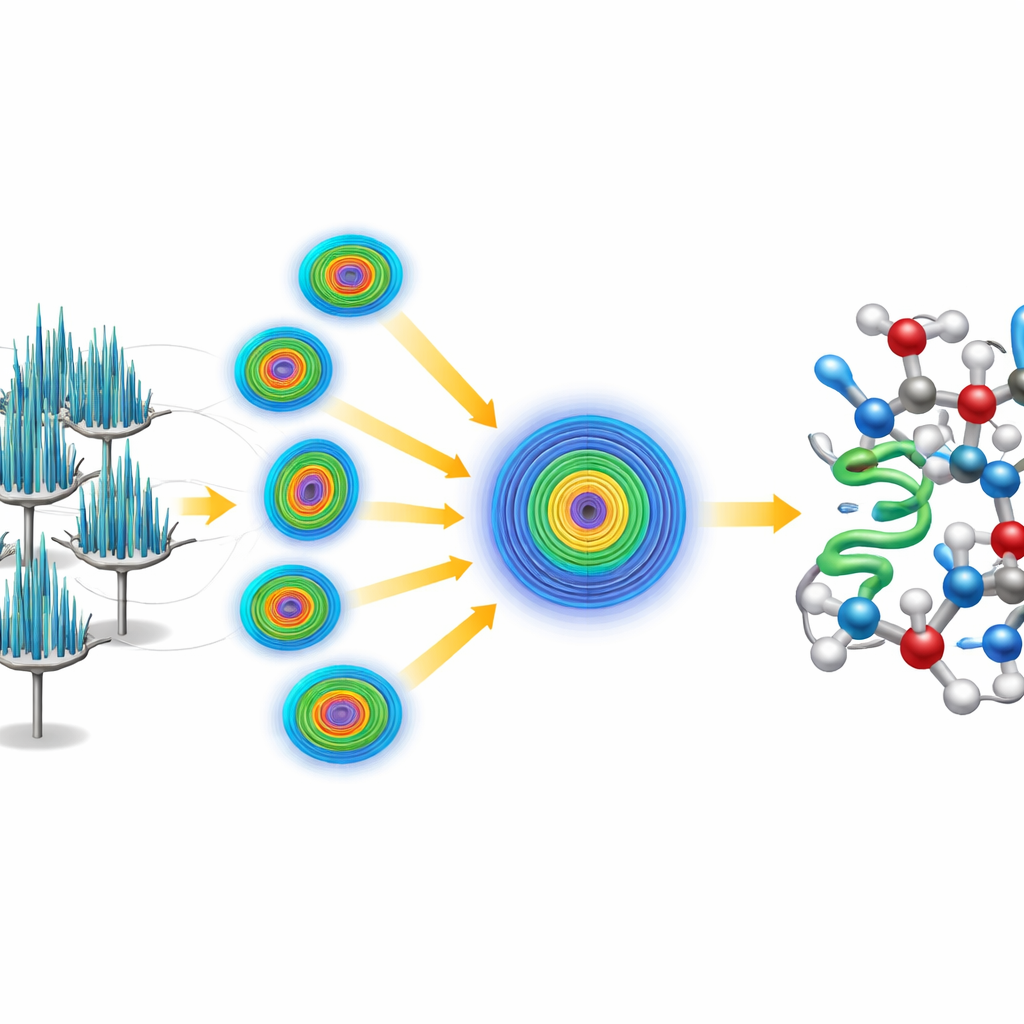
ゼロから構造を解く
既存のクランビンモデルに頼る代わりに、チームは構造を「ab initio」(第一原理から)で解くことに挑みました。彼らはごく小さく一般的な5残基のヘリックス、すなわちクランビンの既知構造とは無関係の短く理想化されたタンパク質断片だけを出発点としました。既存のソフトウェアを用いて、この断片が結晶の繰り返しパターンの中でどこにありうるかを探索し、続いて電子由来マップを徐々に改善する反復的なシャープニング処理を行いました。精密化されたマップは自動トレースソフトウェアが介入なしでクランビン全鎖を追跡できるほど明瞭になり、完全な高解像度モデルが得られました。データは詳細で、鎖のわずか二箇所の違いしか持たない自然変異体を二種識別し、それらを定量化することさえ可能でした。
今後の研究にとっての意義
この研究は、注意深いデータ収集と異方性を考慮した処理を行えば、自発的に形成したナノ結晶と標準的な電子顕微鏡ハードウェアだけで真の原子分解能に到達し、タンパク質構造をゼロから解けることを示しています。クランビンは今や他の研究者が新しい解析手法を試したり、電子散乱のモデルを洗練したり、水素結合や電荷分布といった現象を探るための公開ベンチマークデータセットとして位置づけられます。専門外の読者にとっての要点は、強力な電子線ベースの新しいツールが構造生物学の到達範囲を広げ、かつてはあまりに小さい、脆弱すぎる、あるいは型破りで原子レベルでの研究が難しいと考えられていたタンパク質の最小の詳細を可視化することがますます現実的になっている、ということです。
引用: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
キーワード: MicroED, タンパク質構造, クランビン, 電子回折, ナノ結晶