Clear Sky Science · ru
Прямо из семени: атомное разрешение структуры белка методом ab initio MicroED
Наблюдая мельчайшие строительные блоки жизни
Белки — это крошечные машины, обеспечивающие работу живых клеток, но чтобы действительно понять их функционирование, учёным нужно видеть атомы с исключительной чёткостью. В этой статье описывается, как исследователи использовали мощный метод на основе электронов для определения структуры белка с атомным разрешением, начав прямо с измельчённых семян растений и без опоры на предварительные структурные модели. Их успех задаёт новый ориентир для изучения маленьких или трудных белков, которые не поддаются традиционным методикам.
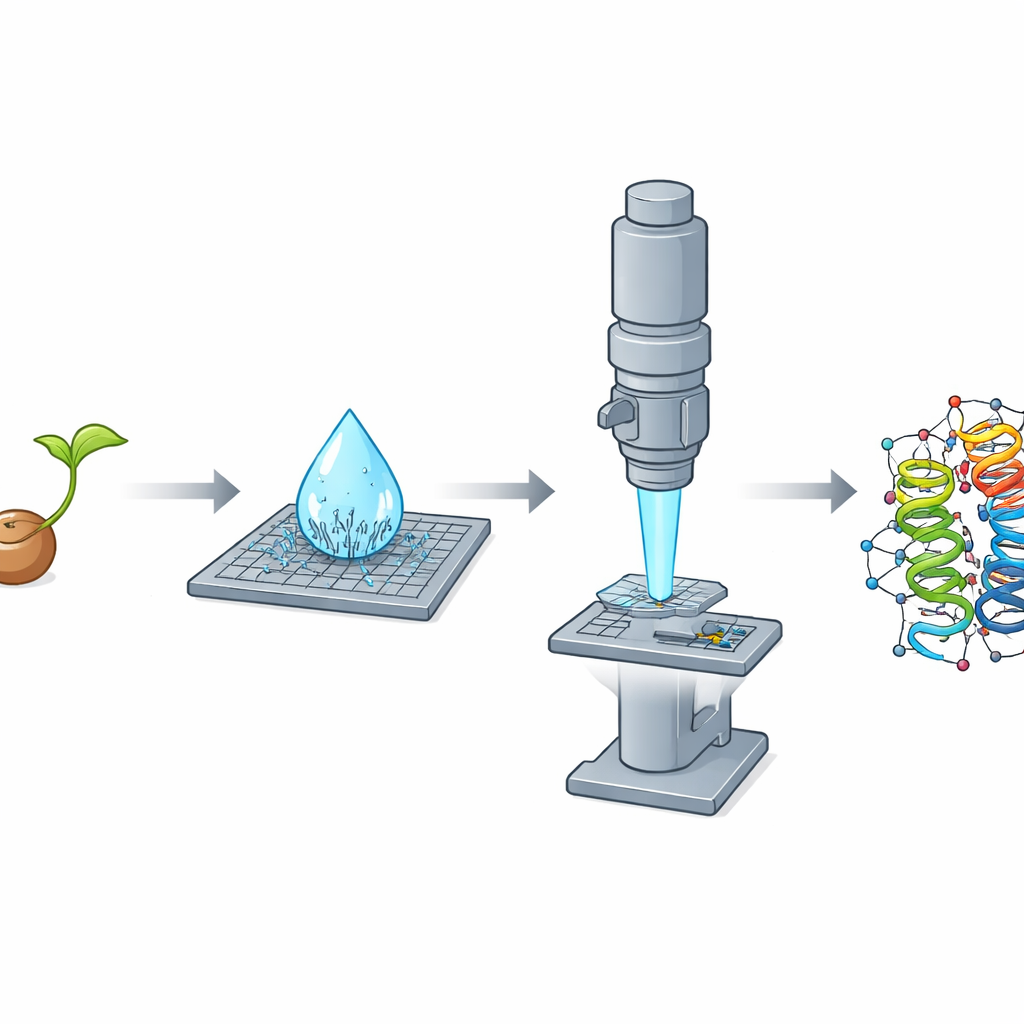
Почему крошечные кристаллы — большая проблема
Долги годы рентгеновская кристаллография была основным инструментом для картирования белковых структур с атомным разрешением. Однако она требует относительно крупных, хорошо упорядоченных кристаллов — часто десятки или сотни микрометров в поперечнике. Многие важные белки естественным образом образуют лишь крошечные кристаллы, намного меньшие по размеру, и потому ускользают от сетей стандартных методов. Другой распространённый подход — криоэлектронная микроскопия одиночных частиц — испытывает трудности с малыми белками, особенно теми, чей размер близок к типичным человеческим белкам. В совокупности эти ограничения оставляют большую часть биологии структурно неизученной.
Использование электронов вместо рентгеновских лучей
Метод микроэлектронной кристаллической дифракции, MicroED, решает эту проблему, применяя электроны вместо рентгеновских лучей. Электроны сильнее взаимодействуют с веществом, что позволяет извлекать детальную структурную информацию из кристаллов по объёму в тысячи раз меньших, чем требуются для рентгена. В данном исследовании команда сосредоточилась на крамбине — мелком белке, содержащемся в семенах масличного растения Crambe abyssinica. Крамбин давно служил испытательным полигоном для продвинутых кристаллографических методов: предыдущие работы с использованием рентгена и нейтронов доводили разрешение до впечатляющих значений. Тем не менее полноценного исследования крамбина «с нуля» методом MicroED ещё не было выполнено в полной мере.
Удачная находка в высыхающей капле
При очистке крамбина из измельчённых семян простым этаноловым способом исследователи сделали впечатляющее наблюдение: когда микролитровая капля раствора высыхала на предметном стекле, в течение нескольких секунд она спонтанно образовывала плотный дождь игольчатых нанокристаллов. Эти тонкие образования оказались плохи для рентгеновских экспериментов, но почти идеальными для электронной дифракции, поскольку были чрезвычайно тонкими по одному измерению и потому прозрачными для электронного пучка. Команда также выращивала традиционные, блочные кристаллы, превосходные для рентгеновских исследований, но слишком толстые для MicroED, даже после дробления. Это явное противопоставление — иглы плохи для рентгена, но отличны для электронов; блоки — наоборот — подчёркивает, как форма и толщина кристалла могут определять, какой метод окажется предпочтительным.
Объединение множества игл в одну ясную картину
Была одна загвоздка: игольчатые кристаллы обычно располагались на сетке микроскопа в одинаковой ориентации, так что отдельный кристалл давал неполный и направленно смещённый вид белка. Чтобы преодолеть это, исследователи применили серийную стратегию, собирая небольшие фрагменты данных из 58 разных кристаллов и объединяя их в один большой набор. Поскольку качество данных сильно зависело от направления обзора, они использовали специальную стадию обработки, которая распознаёт и отбрасывает слабые, зашумлённые измерения в плохо покрытых направлениях, сохраняя при этом сильные сигналы там, где кристаллы дифрагировали лучше всего. Такая обработка дала высококачественный набор данных с разрешением лучше одного ангстрема, достаточно подробный, чтобы выявить отдельные атомы, включая многие водороды.
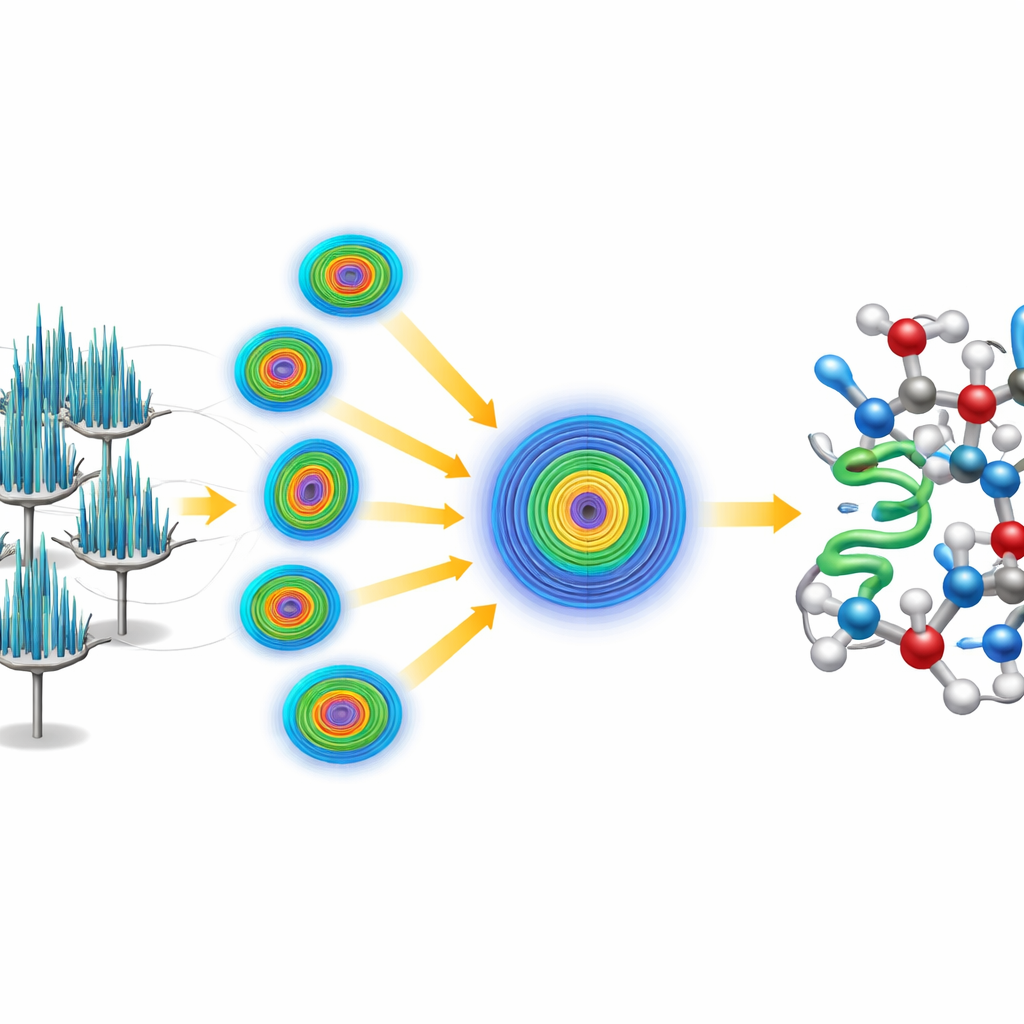
Решение структуры «с нуля»
Вместо того чтобы опираться на существующую модель крамбина, команда поставила перед собой задачу решить структуру «ab initio», то есть из первых принципов. Они начали лишь с крошечного, общего пятиаминокислотного спирального фрагмента — по существу короткого идеализированного участка белка, не связанного со знаменитой структурой крамбина. Используя проверенное программное обеспечение, они определили, где этот фрагмент мог бы правдоподобно располагаться внутри повторяющейся кристаллической решётки, затем применили итеративную процедуру «заострения», которая постепенно улучшала карту, полученную от электронных данных. Отшлифованная карта стала настолько ясной, что автоматическое ПО смогло проследить весь полимера цепочки крамбина без человеческого вмешательства, дав полную модель высокого разрешения. Данные были настолько детализированы, что исследователи смогли различить и количественно оценить две природно встречающиеся варианты крамбина, отличающиеся всего в двух положениях в цепи.
Что это значит для будущих исследований
Работа демонстрирует, что при тщательном сборе данных и обработке с учётом анизотропии возможно достичь истинного атомного разрешения и решить структуру белка с нуля, используя только спонтанно образовавшиеся нанокристаллы и стандартное оборудование электронного микроскопа. Крамбин теперь служит публичным эталонным набором данных, который другие учёные могут применять для тестирования новых методов анализа, уточнения моделей рассеяния электронов и изучения явлений, таких как водородные связи и распределение зарядов. Для неспециалистов ключевая мысль такова: мощные новые методы на основе электронов расширяют возможности структурной биологии, делая всё более достижимой визуализацию мельчайших деталей белков, которые раньше считались слишком маленькими, слишком хрупкими или слишком необычными для изучения с атомной точностью.
Цитирование: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
Ключевые слова: MicroED, структура белка, крамбин, электронная дифракция, нанокристаллы