Clear Sky Science · pt
Direto da semente: uma estrutura proteica em resolução atômica por MicroED ab initio
Vendo os Menores Blocos de Construção da Vida
Proteínas são as pequenas máquinas que mantêm as células vivas funcionando, mas para compreender verdadeiramente como elas atuam, os cientistas precisam visualizar seus átomos com clareza extraordinária. Este artigo descreve como pesquisadores usaram um método poderoso baseado em elétrons para determinar uma estrutura proteica em nível atômico começando diretamente de sementes trituradas de planta, sem depender de modelos estruturais prévios. O sucesso deles estabelece um novo referencial para estudar proteínas pequenas ou difíceis que resistem às técnicas tradicionais.
Por que Cristais Minúsculos São um Grande Problema
Durante décadas, a cristalografia de raios X tem sido a principal ferramenta para mapear estruturas proteicas em resolução atômica. No entanto, ela exige cristais relativamente grandes e altamente ordenados — frequentemente dezenas a centenas de micrômetros de dimensão. Muitas proteínas importantes formam naturalmente apenas cristais minúsculos, muito menores que isso, e portanto escapam às malhas dos métodos padrão. Outra abordagem popular, a criomicroscopia eletrônica de partículas isoladas, encontra dificuldades com proteínas menores, especialmente aquelas mais próximas do tamanho típico das proteínas humanas. Juntas, essas limitações deixam uma ampla faixa da biologia estruturalmente inexplorada.
Usando Elétrons em Vez de Raios X
A difração eletrônica de microcristais, ou MicroED, enfrenta esse problema ao usar elétrons em vez de raios X. Elétrons interagem muito mais fortemente com a matéria, permitindo que os cientistas extraiam informações estruturais detalhadas de cristais milhares de vezes menores em volume do que os exigidos para experimentos com raios X. Neste estudo, a equipe focou na crambina, uma proteína diminuta encontrada nas sementes da planta oleaginosa Crambe abyssinica. A crambina tem servido há muito tempo como um campo de prova para métodos cristalográficos avançados, com trabalhos anteriores usando raios X e nêutrons alcançando resoluções impressionantes. Ainda assim, uma investigação completa e do zero da crambina usando MicroED não havia sido totalmente realizada.
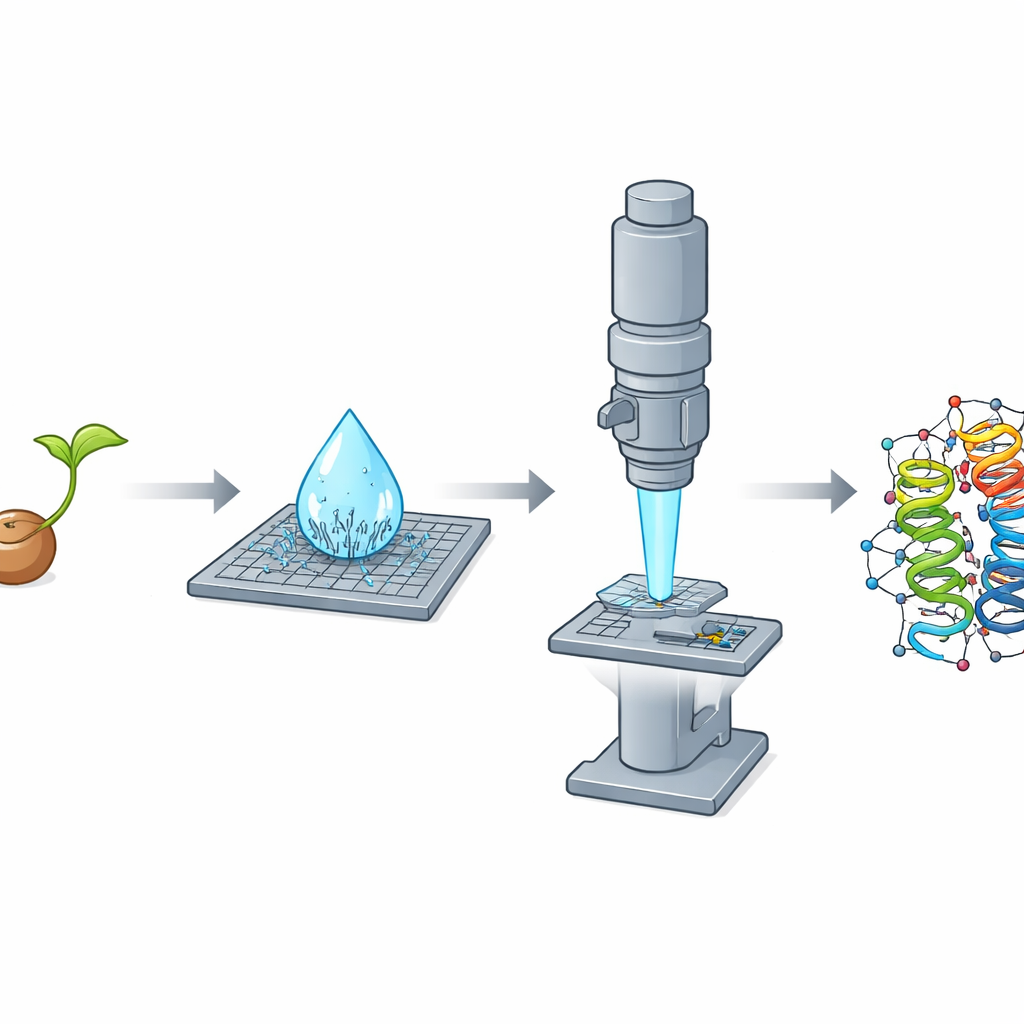
Uma Descoberta Fortuita em uma Gota que Seca
Ao purificar a crambina a partir de sementes trituradas com um procedimento simples à base de etanol, os pesquisadores fizeram uma observação marcante: conforme uma gota microlitro da solução secava sobre uma lamínula, ela produzia espontaneamente em segundos uma chuva densa de nanocristais em forma de agulha. Esses fragmentos mostraram-se maus candidatos para experimentos de raios X, mas quase ideais para difração eletrônica, porque eram extremamente finos em uma dimensão e, portanto, transparentes ao feixe de elétrons. A equipe também cresceu cristais tradicionais, em bloco, que se saíram muito bem em experimentos de raios X, mas eram espessos demais para MicroED, mesmo após trituração. Essa clara inversão — agulhas ruins para raios X mas excelentes para elétrons, blocos o oposto — destacou como a forma e a espessura do cristal podem ditar qual método prevalece.
Combinando Muitas Agulhas em Uma Imagem Clara
Havia um problema: os cristais em forma de agulha tendiam a se posicionar na mesma orientação sobre a grade do microscópio, o que significava que qualquer cristal isolado fornecia uma visão incompleta e enviesada da proteína. Para superar isso, os pesquisadores adotaram uma estratégia serial, coletando pequenas fatias de dados de 58 cristais diferentes e mesclando-as em um único conjunto de dados. Como a qualidade dos dados dependia fortemente da direção de visualização, eles usaram um passo de processamento especializado que reconhece e elimina medições fracas e ruidosas em direções mal amostradas, preservando sinais fortes onde os cristais difratavam melhor. Esse tratamento produziu um conjunto de dados de altíssima qualidade, alcançando resolução melhor que um ângström, suficientemente rico para revelar átomos individuais, incluindo muitos hidrogênios.
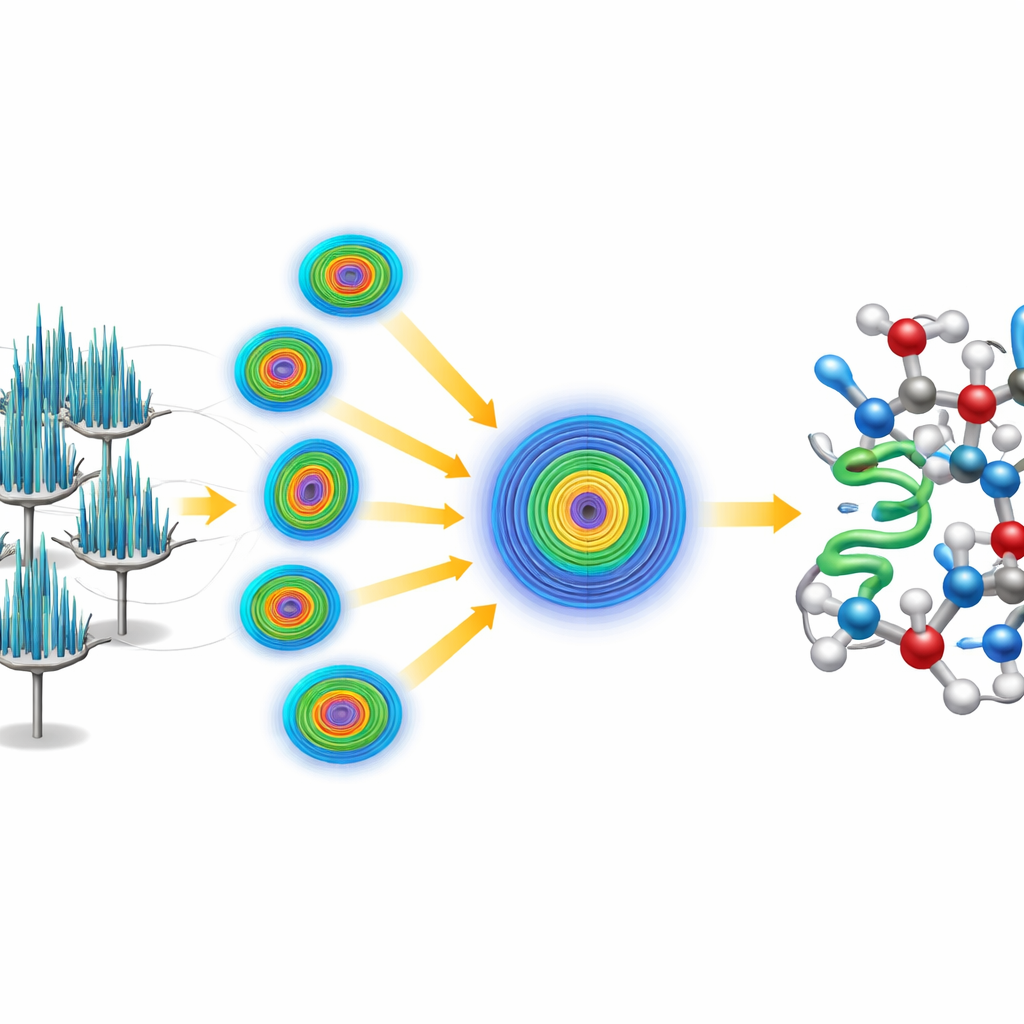
Resolvendo a Estrutura do Zero
Em vez de apoiar-se em um modelo existente da crambina, a equipe desafiou-se a resolver a estrutura “ab initio”, ou a partir dos primeiros princípios. Eles começaram com apenas um pequeno e genérico helicóide de cinco aminoácidos — essencialmente um curto fragmento proteico idealizado, sem relação com a estrutura conhecida da crambina. Usando softwares estabelecidos, localizaram onde esse fragmento poderia plausivelmente se encaixar no padrão repetitivo do cristal e então aplicaram um procedimento iterativo de afinação que gradualmente melhorou o mapa derivado dos elétrons. O mapa refinado tornou-se suficientemente claro para que um software automatizado traçasse toda a cadeia da crambina sem intervenção humana, produzindo um modelo completo e de alta resolução. Os dados foram tão detalhados que os pesquisadores puderam distinguir e quantificar duas variantes naturais da crambina que diferem em apenas duas posições da cadeia.
O Que Isso Significa para Estudos Futuros
O trabalho demonstra que, com coleta de dados cuidadosa e processamento sensível à anisotropia, é possível alcançar verdadeira resolução atômica e resolver a estrutura de uma proteína desde o início usando apenas nanocristais formados espontaneamente e equipamento padrão de microscopia eletrônica. A crambina agora se firma como um conjunto de dados de referência público que outros cientistas podem usar para testar novos métodos de análise, refinar modelos de espalhamento de elétrons e explorar fenômenos como ligação por hidrogênio e distribuição de carga. Para não especialistas, a principal conclusão é que poderosas novas ferramentas baseadas em elétrons estão ampliando o alcance da biologia estrutural, tornando cada vez mais viável visualizar os menores detalhes de proteínas que antes eram consideradas pequenas demais, frágeis demais ou pouco convencionais para serem estudadas em detalhe atômico.
Citação: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
Palavras-chave: MicroED, estrutura de proteína, crambina, difração de elétrons, nanocristais