Clear Sky Science · sv
Direkt från fröet: en proteinstruktur i atomupplösning med ab initio MicroED
Att se livets minsta byggstenar
Proteiner är de små maskiner som håller levande celler i gång, men för att verkligen förstå hur de fungerar behöver forskare se deras atomer med enastående klarhet. Denna artikel beskriver hur forskare använde en kraftfull elektronbaserad metod för att bestämma en proteinstruktur på atomnivå med start direkt från krossade växtfrön, utan att förlita sig på tidigare strukturella modeller. Deras framgång ger en ny referenspunkt för studier av små eller svårhanterliga proteiner som motstår traditionella tekniker.
Varför små kristaller är ett stort problem
I årtionden har röntgenkristallografi varit huvudmetoden för att kartlägga proteinstrukturer i atomupplösning. Den kräver emellertid relativt stora, välordnade kristaller—ofta tiotals till hundratals mikrometer i omkrets. Många viktiga proteiner bildar naturligt endast mikroskopiska kristaller, mycket mindre än så, och faller därför utanför standardmetodernas räckvidd. En annan populär metod, enkelpartikel kryo-elektronmikroskopi, har svårt med mindre proteiner, särskilt de i storleksklassen för typiska humana proteiner. Tillsammans lämnar dessa begränsningar ett stort område av biologin strukturellt outforskad.
Att använda elektroner istället för röntgen
Microcrystal electron diffraction, eller MicroED, tar itu med detta problem genom att använda elektroner i stället för röntgenstrålar. Elektroner interagerar mycket starkare med materia, vilket gör det möjligt för forskare att utvinna detaljerad strukturell information från kristaller som är tusentals gånger mindre i volym än de som krävs för röntgenstudier. I denna studie fokuserade teamet på crambin, ett litet protein som finns i fröna från oljeväxten Crambe abyssinica. Crambin har länge tjänat som testobjekt för avancerade kristallografiska metoder, där tidigare arbete med röntgen och neutroner pressat upplösningen till häpnadsväckande nivåer. Ändå hade en fullständig, från-grunden-analys av crambin med MicroED inte tidigare realiserats fullt ut.
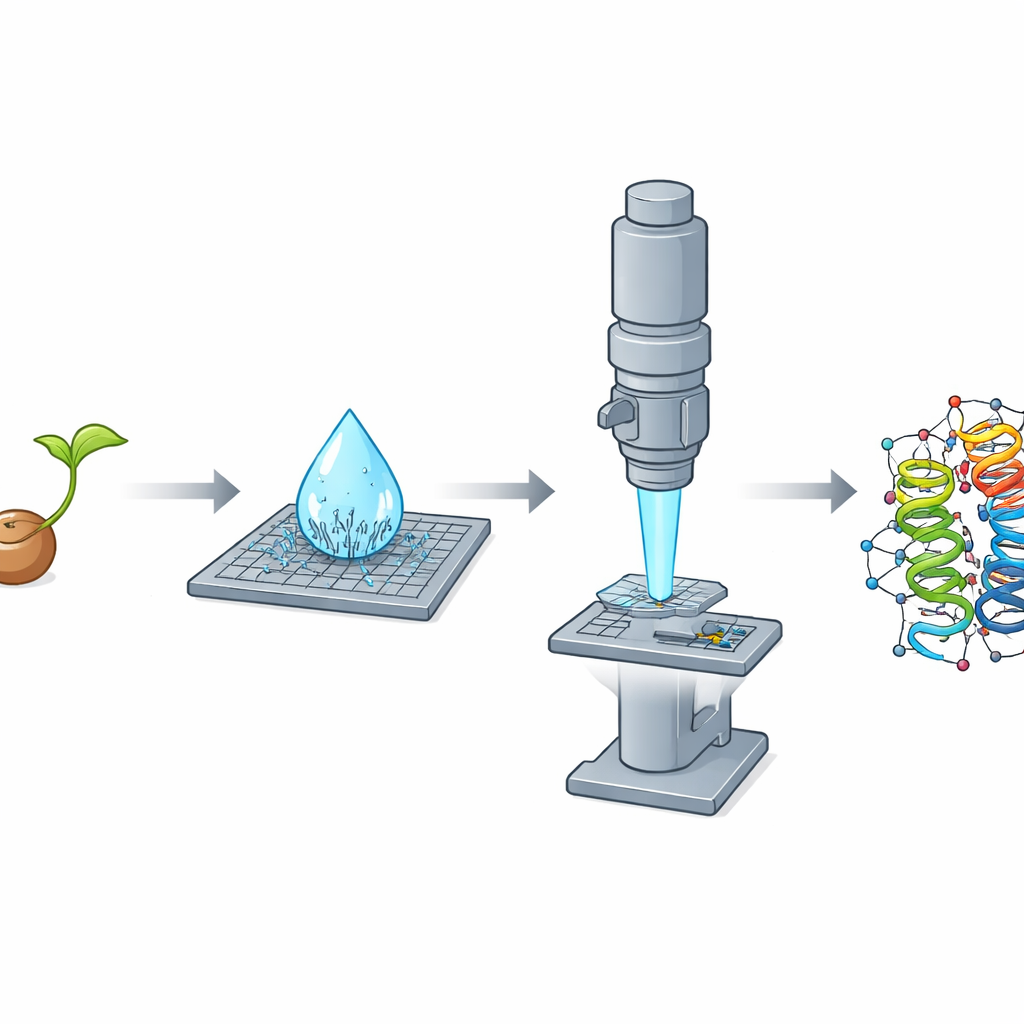
En lycklig upptäckt i en torkande droppe
Vid rening av crambin från krossade frön med en enkel etanolbaserad procedur gjorde forskarna en anmärkningsvärd observation: när en mikroliters droppe av lösningen torkade på ett objektglas bildades spontant en tät skur av nålformade nanokristaller inom sekunder. Dessa skivor visade sig vara dåliga för röntgenarbete men nästan idealiska för elektrondiffraktion, eftersom de var extremt tunna i en dimension och därmed genomskinliga för elektronstrålen. Teamet odlade också traditionella, blocklika kristaller som utmärkte sig i röntgenexperiment men var för tjocka för MicroED, även efter krossning. Denna tydliga omvändning—nålar dåliga för röntgen men utmärkta för elektroner, blocken tvärtom—belyste hur kristallens form och tjocklek kan avgöra vilken metod som blir framgångsrik.
Att kombinera många nålar till en tydlig bild
Det fanns en hake: nålkristallerna tenderade att lägga sig i samma orientering på mikroskopgallret, vilket innebar att varje enskild kristall gav en ofullständig och riktad skev bild av proteinet. För att övervinna detta antog forskarna en serieteknik, där de samlade små dataskivor från 58 olika kristaller och slog samman dem till en stor datamängd. Eftersom datakvaliteten var starkt beroende av siktlinjen använde de ett specialiserat bearbetningssteg som känner igen och trimmar bort svaga, brusiga mätningar i dåligt täckta riktningar samtidigt som starka signaler bevaras där kristallerna diffrakterade bäst. Denna behandling gav en mycket högkvalitativ datamängd med bättre än en ångströms upplösning, rik nog att avslöja individuella atomer, inklusive många väten.
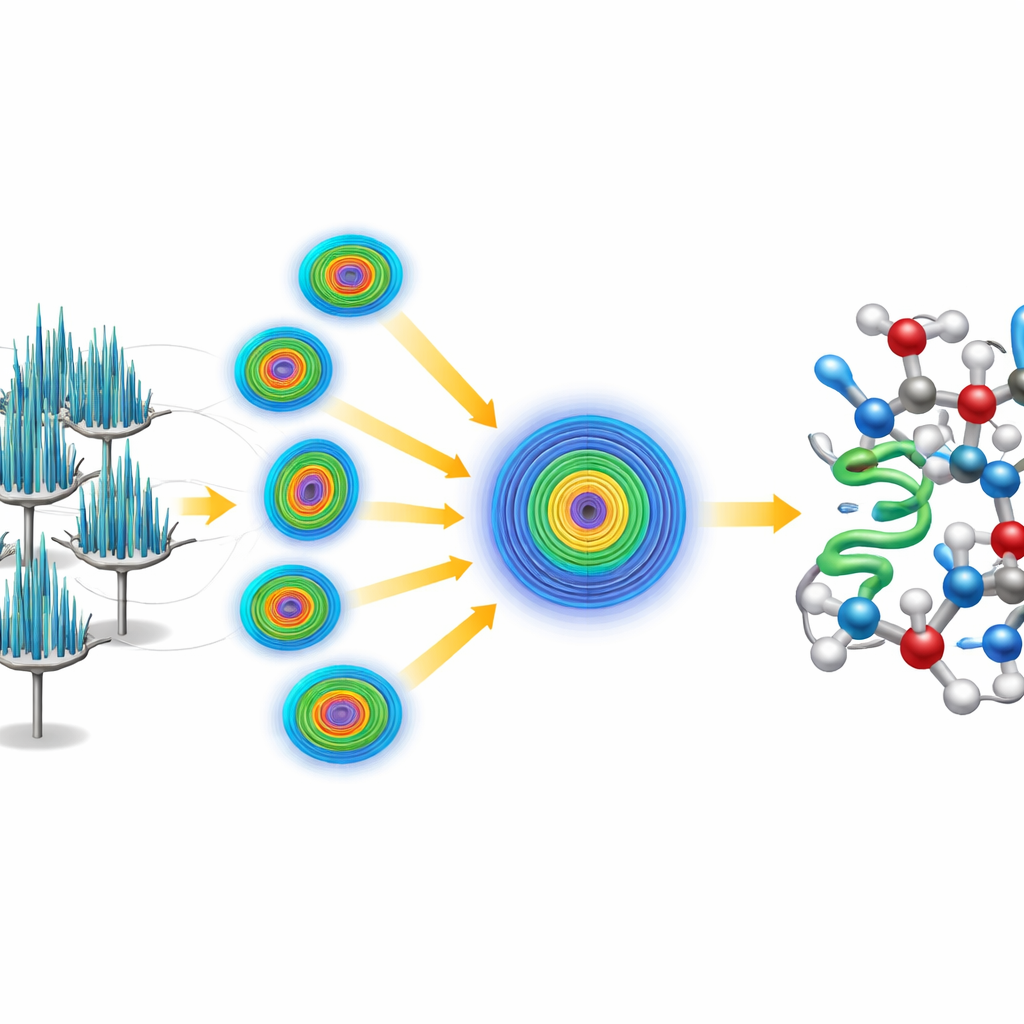
Att lösa strukturen från grunden
I stället för att luta sig mot en befintlig modell av crambin utmanade teamet sig själva att lösa strukturen “ab initio”, det vill säga från första principer. De började med endast en liten, generisk fem-aminosyrors helix—i praktiken en kort, idealiserad proteinfragment som inte var relaterat till crambins kända struktur. Med etablerad programvara lokaliserade de var detta fragment rimligen kunde passa in i kristallens upprepande mönster, och tillämpade sedan en iterativ skärpningsprocedur som successivt förbättrade den elektronbaserade kartan. Den förfinade kartan blev tillräckligt tydlig för att automatiserad programvara skulle kunna spåra hela crambinkedjan utan mänsklig inblandning, vilket gav en komplett modell i hög upplösning. Datat var så detaljerat att forskarna kunde särskilja och kvantifiera två naturligt förekommande varianter av crambin som skiljde sig på endast två positioner i kedjan.
Vad detta betyder för framtida studier
Arbetet visar att med noggrann datainsamling och anisotropi-medveten bearbetning är det möjligt att nå verklig atomupplösning och lösa en proteinstruktur från grunden med enbart spontant bildade nanokristaller och standardutrustning för elektronmikroskopi. Crambin fungerar nu som en offentlig referensdatamängd som andra forskare kan använda för att testa nya analysmetoder, förfina modeller av elektron-spridning och utforska fenomen som vätebindningar och laddningsfördelning. För icke-specialister är huvudpoängen att kraftfulla nya elektronbaserade verktyg utvidgar strukturell biologis räckvidd, vilket gör det alltmer möjligt att visualisera de minsta detaljerna hos proteiner som tidigare betraktades som för små, för sköra eller för ovanliga för att studera i atomär detalj.
Citering: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
Nyckelord: MicroED, proteinstruktur, crambin, elektrondiffraktion, nanokristaller