Clear Sky Science · es
Directo desde la semilla: una estructura proteica a resolución atómica mediante MicroED ab initio
Ver los bloques construidos más pequeños de la vida
Las proteínas son las diminutas máquinas que mantienen en funcionamiento las células vivas, pero para comprender realmente cómo actúan, los científicos necesitan ver sus átomos con una claridad extraordinaria. Este artículo describe cómo los investigadores emplearon un potente método basado en electrones para determinar una estructura proteica a nivel atómico partiendo directamente de semillas trituradas, sin apoyarse en modelos estructurales previos. Su éxito ofrece un nuevo referente para estudiar proteínas pequeñas o difíciles que resisten las técnicas tradicionales.
Por qué los cristales diminutos son un gran problema
Durante décadas, la cristalografía de rayos X ha sido la herramienta principal para mapear estructuras proteicas a resolución atómica. Sin embargo, exige cristales relativamente grandes y muy ordenados, a menudo de decenas a cientos de micrómetros. Muchas proteínas importantes forman de forma natural cristales minúsculos, mucho más pequeños que eso, y por tanto se escapan a los métodos estándar. Otro enfoque popular, la criomicroscopía electrónica de partículas individuales, tiene dificultades con proteínas pequeñas, especialmente las del tamaño típico de las proteínas humanas. En conjunto, estas limitaciones dejan un amplio terreno de la biología estructural sin explorar.
Usar electrones en lugar de rayos X
La difracción electrónica de microcristales, o MicroED, aborda este problema usando electrones en lugar de rayos X. Los electrones interactúan mucho más fuertemente con la materia, lo que permite extraer información estructural detallada de cristales miles de veces más pequeños en volumen que los necesarios para trabajos con rayos X. En este estudio, el equipo se centró en la crambina, una proteína diminuta presente en las semillas de la planta oleaginosa Crambe abyssinica. La crambina ha servido durante mucho tiempo como campo de prueba para métodos cristalográficos avanzados, con estudios previos usando rayos X y neutrones que alcanzaron resoluciones asombrosas. Sin embargo, no se había realizado por completo una investigación desde cero de la crambina usando MicroED.
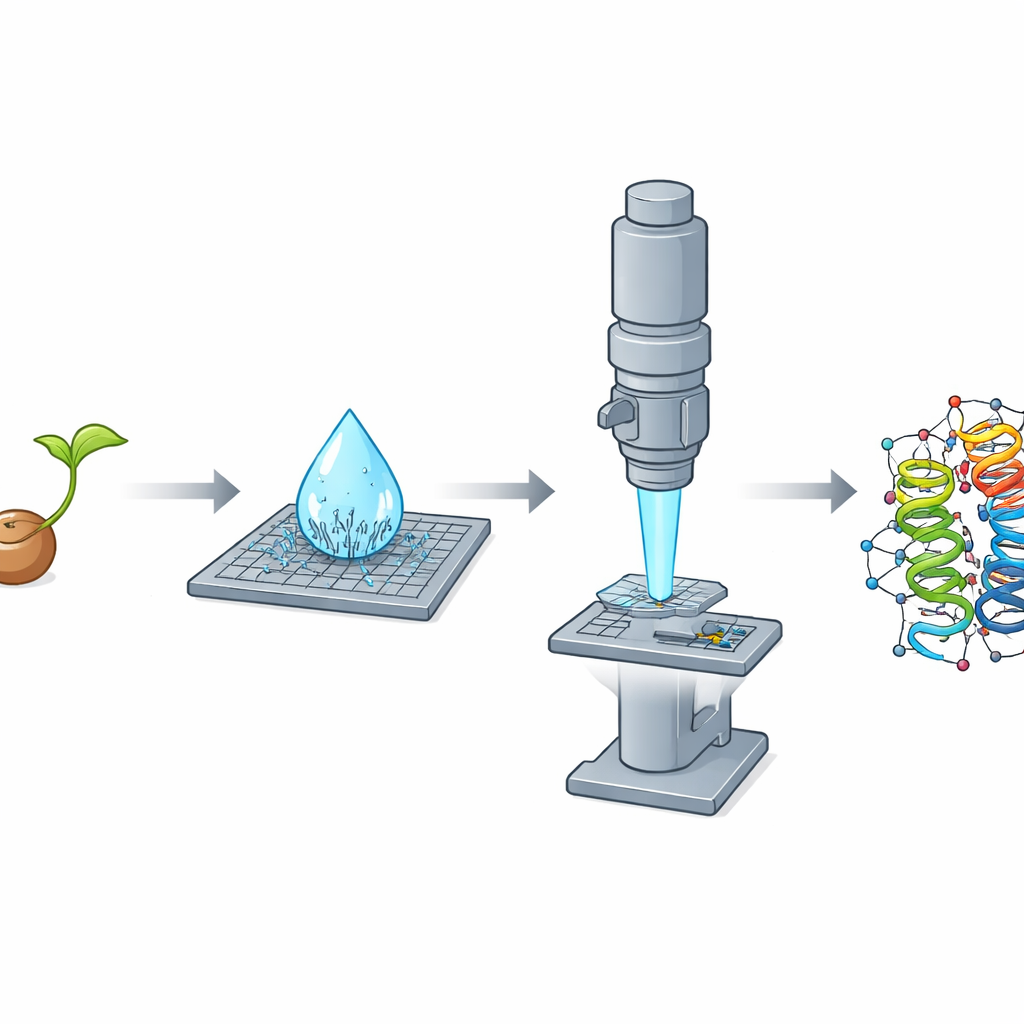
Un hallazgo afortunado en una gota que se seca
Mientras purificaban la crambina a partir de semillas trituradas con un procedimiento sencillo basado en etanol, los investigadores hicieron una observación llamativa: al secarse sobre un portaobjetos una gota microlitro de la solución, se formó espontáneamente en segundos una densa lluvia de nanocristales en forma de agujas. Estas láminas resultaron ser malos candidatos para rayos X pero casi ideales para difracción electrónica, porque eran extremadamente finas en una dimensión y por tanto transparentes al haz de electrones. El equipo también cultivó cristales tradicionales, en forma de bloques, que rendían muy bien en experimentos de rayos X pero eran demasiado gruesos para MicroED, incluso tras triturarlos. Esta clara inversión —agujas malas para rayos X pero excelentes para electrones, bloques al revés— destacó cómo la forma y el grosor del cristal pueden dictar qué método resulta ganador.
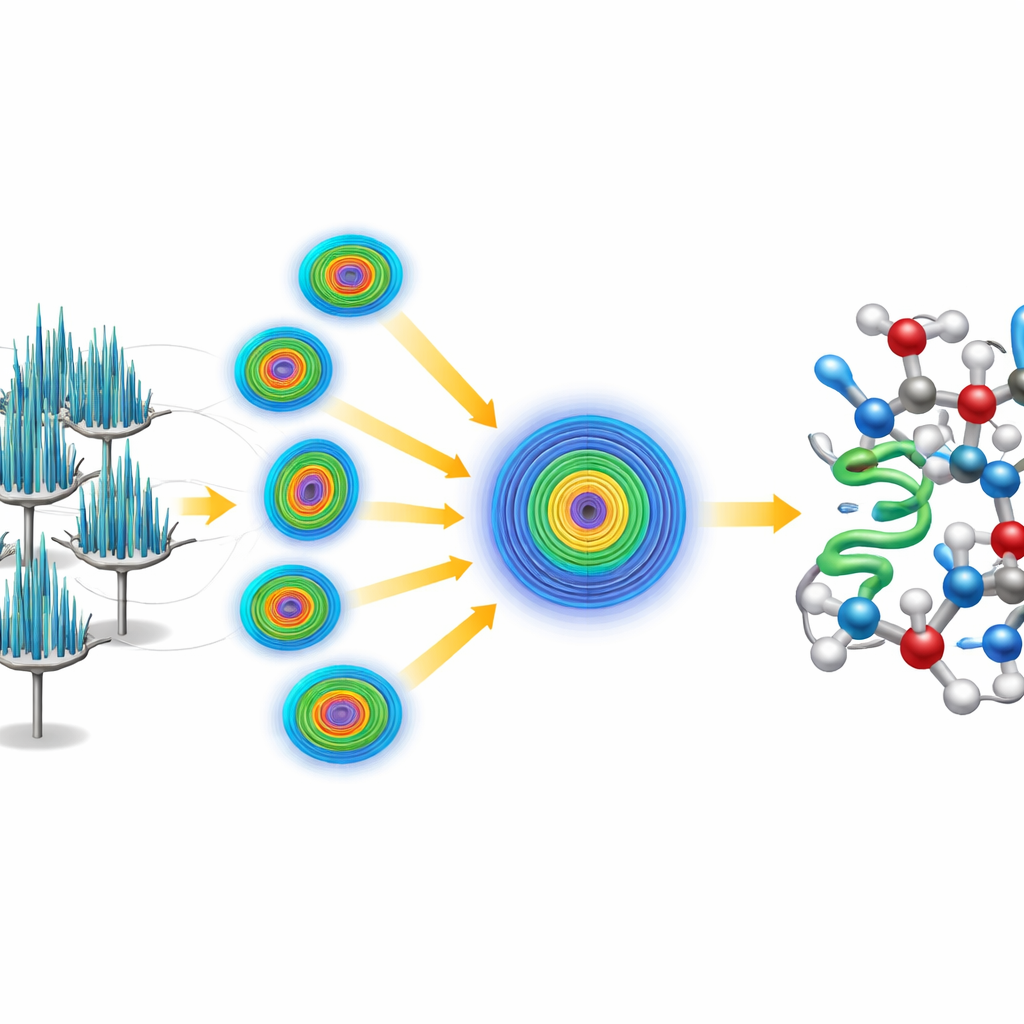
Combinar muchas agujas en una imagen clara
Había un inconveniente: los cristales en forma de aguja tendían a colocarse en la misma orientación sobre la rejilla del microscopio, lo que significaba que cualquier cristal individual ofrecía una visión incompleta y sesgada direccionalmente de la proteína. Para superar esto, los investigadores adoptaron una estrategia serial, recopilando pequeños fragmentos de datos de 58 cristales distintos y fusionándolos en un único conjunto de datos. Dado que la calidad de los datos dependía fuertemente de la dirección de observación, emplearon un paso de procesamiento especializado que reconoce y recorta mediciones débiles y ruidosas en direcciones pobremente muestreadas, manteniendo las señales fuertes donde los cristales difractaban mejor. Este tratamiento generó un conjunto de datos de muy alta calidad que alcanzó mejor que una angstrom de resolución, lo bastante rico como para revelar átomos individuales, incluidos muchos hidrógenos.
Resolver la estructura desde cero
En lugar de apoyarse en un modelo existente de la crambina, el equipo se propuso resolver la estructura “ab initio”, o desde primeros principios. Comenzaron con solo una pequeña hélice genérica de cinco aminoácidos —esencialmente un fragmento proteico corto e idealizado no relacionado con la estructura conocida de la crambina. Usando software establecido, localizaron dónde podría encajar plausiblemente este fragmento dentro del patrón repetitivo del cristal y luego aplicaron un procedimiento iterativo de afilado que mejoró gradualmente el mapa derivado de electrones. El mapa refinado se volvió lo bastante claro como para que un programa automático trazara toda la cadena de la crambina sin intervención humana, produciendo un modelo completo y de alta resolución. Los datos fueron tan detallados que los investigadores pudieron distinguir y cuantificar dos variantes naturales de la crambina que difieren en apenas dos posiciones de la cadena.
Qué significa esto para estudios futuros
El trabajo demuestra que, con una recolección de datos cuidadosa y un procesamiento que tiene en cuenta la anisotropía, es posible alcanzar una resolución verdaderamente atómica y resolver la estructura de una proteína desde cero usando únicamente nanocristales formados espontáneamente y hardware estándar de microscopio electrónico. La crambina se establece ahora como un conjunto de datos de referencia público que otros científicos pueden usar para probar nuevos métodos de análisis, refinar modelos de dispersión electrónica y explorar fenómenos como enlaces de hidrógeno y distribución de carga. Para los no especialistas, la conclusión principal es que poderosas herramientas electrónicas están ampliando el alcance de la biología estructural, haciendo cada vez más factible visualizar los detalles más pequeños de proteínas que antes se consideraban demasiado pequeñas, frágiles o poco convencionales para estudiarse con detalle atómico.
Cita: Vasireddy, P.C.R., Low-Beer, T., Spoth, K.A. et al. Direct from the seed: an atomic resolution protein structure by ab initio MicroED. Nat Commun 17, 2759 (2026). https://doi.org/10.1038/s41467-026-69601-y
Palabras clave: MicroED, estructura de proteínas, crambina, difracción de electrones, nanocristales