Clear Sky Science · zh
GLP-1通过激活冠状动脉周细胞中的KATP通道,作为介导脑-肠-心信号传导的效应子以实现心脏保护
为什么保护微小心脏血管很重要
在心脏病发作后重新开放被阻塞的冠状动脉时,许多人以为血流会完全恢复。然而多达一半的患者中,心脏中最小的血管仍然保持关闭,导致部分心肌持续缺血。这种被忽视的问题称为“无再灌注”(no‑reflow),会大幅增加心力衰竭和死亡的风险。本研究总结揭示了一条能够从内部打开这些微小血管的脑–肠–心信号通路,并指出可利用已用于糖尿病治疗的药物来保护心脏的新方法。
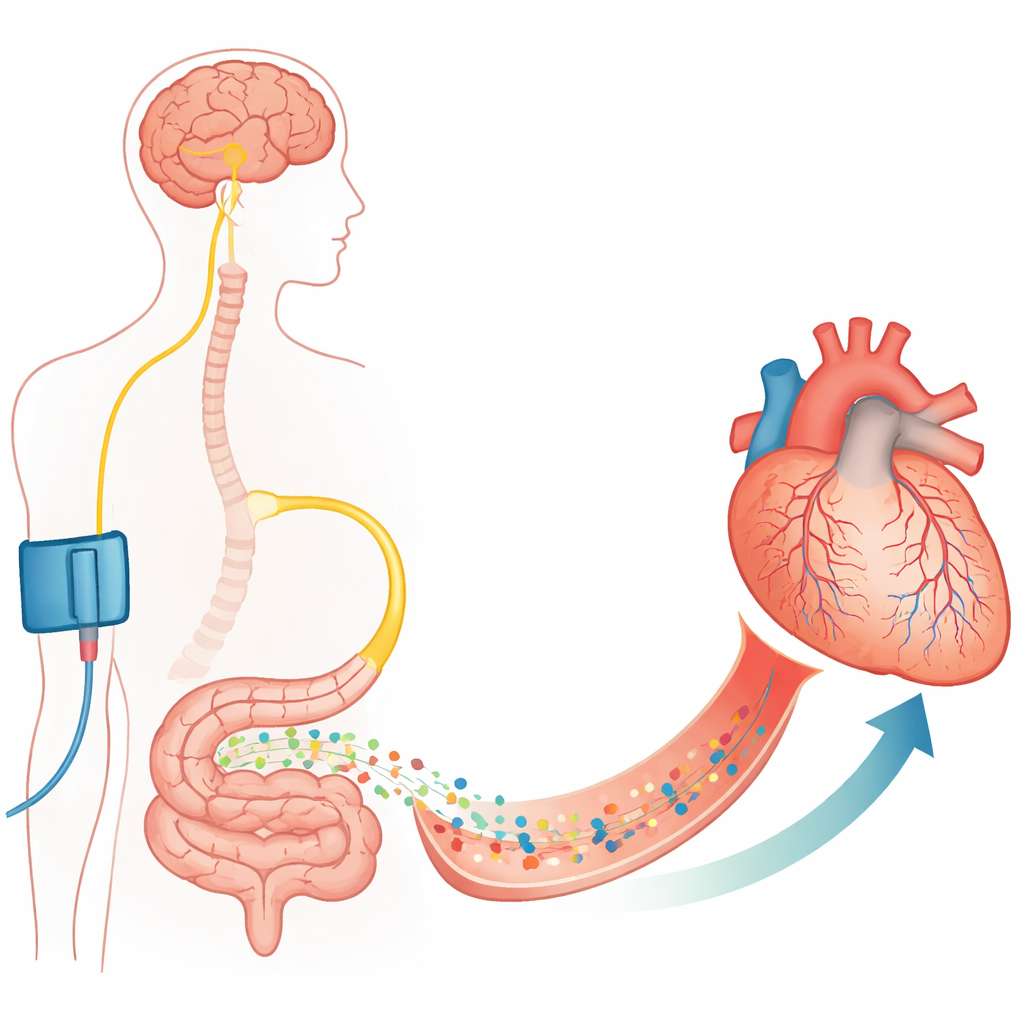
从大动脉到微小守门细胞
用支架打开堵塞的冠状动脉虽能挽救生命,但并不总是足够。作者将注意力放在毛细血管上——这些头发丝般细小的血管才是真正把氧气送到心肌的结构。包绕在这些毛细血管周围的支撑细胞称为周细胞(pericytes),它们能收缩或放松血管壁。早期研究表明,在缺血和再灌注过程中,周细胞会收紧并有时在收缩状态下死亡,导致毛细血管永久变窄并引起无再灌注。本研究在大鼠和小鼠心脏中证实,在对冠状动脉进行可控阻塞并重新开放后,许多毛细血管在周细胞处仍然收缩,且大部分不再有血流,尽管主干动脉已经通畅。
来自肠道的激素与心脏毛细血管交流
研究人员接着探讨机体是否存在内在机制来使这些周细胞松弛。他们考察了远端缺血预处理(remote ischaemic preconditioning)这一现象——例如用袖带短暂阻断肢体血流,竟能在后续心脏堵塞时提供保护。既往工作指出迷走神经和肠道激素GLP‑1是关键传讯分子。利用荧光探针和抗体,研究团队证明小鼠的冠状动脉周细胞以及培养的人类心脏周细胞上存在GLP‑1受体。在活体大鼠中,在冠状动脉阻塞前短暂使后肢缺血,能显著减少毛细血管阻塞并恢复濒危心区的灌注血容量——但该效果依赖于GLP‑1受体的活性。阻断这些受体会消除这种益处,使无再灌注现象重新出现。
GLP‑1如何使毛细血管重新扩张
为解析机制,作者使用了隔离并加压的鼠心组织片段,在显微镜下观察单个毛细血管和周细胞。当他们从灌注液中去除氧气和葡萄糖时,周细胞收缩,毛细血管直径变小。在持续低氧条件下加入一种类GLP‑1药物(Exendin‑4)会使周细胞松弛,毛细血管几乎恢复到原来的宽度。如果阻断一种称为ATP敏感钾通道(KATP)的特定离子通道或在周细胞中基因性去除该通道的关键成分,这一效应就消失。同样,直接的KATP通道开启剂能逆转药物诱导的收缩,但对周细胞KATP敲除的小鼠无效。在整只动物的实验中,缺失周细胞KATP通道的小鼠也丧失了远端预处理带来的心脏保护,坚定地把这些通道与保护性通路联系在一起。
通过细胞能量和信号传导进行精细调控
故事还深入到这些通道如何被调控。团队表明,感知细胞能量状态的酶——AMP激活蛋白激酶(AMPK)是关键。阻断AMPK会阻止GLP‑1重新打开收缩的毛细血管,并使KATP通道从细胞表面移位,提示AMPK有助于将这些通道运送到周细胞膜上以发挥作用。他们还发现,阻断一氧化氮产生或阻断毒蕈碱(乙酰胆碱)受体本身并不会加重收缩,但会特异性地阻断GLP‑1触发的扩张。这支持了这样一个模型:一氧化氮和乙酰胆碱在上游激活AMPK,进而促进KATP通道的运输,使GLP‑1能够使周细胞超极化并松弛。
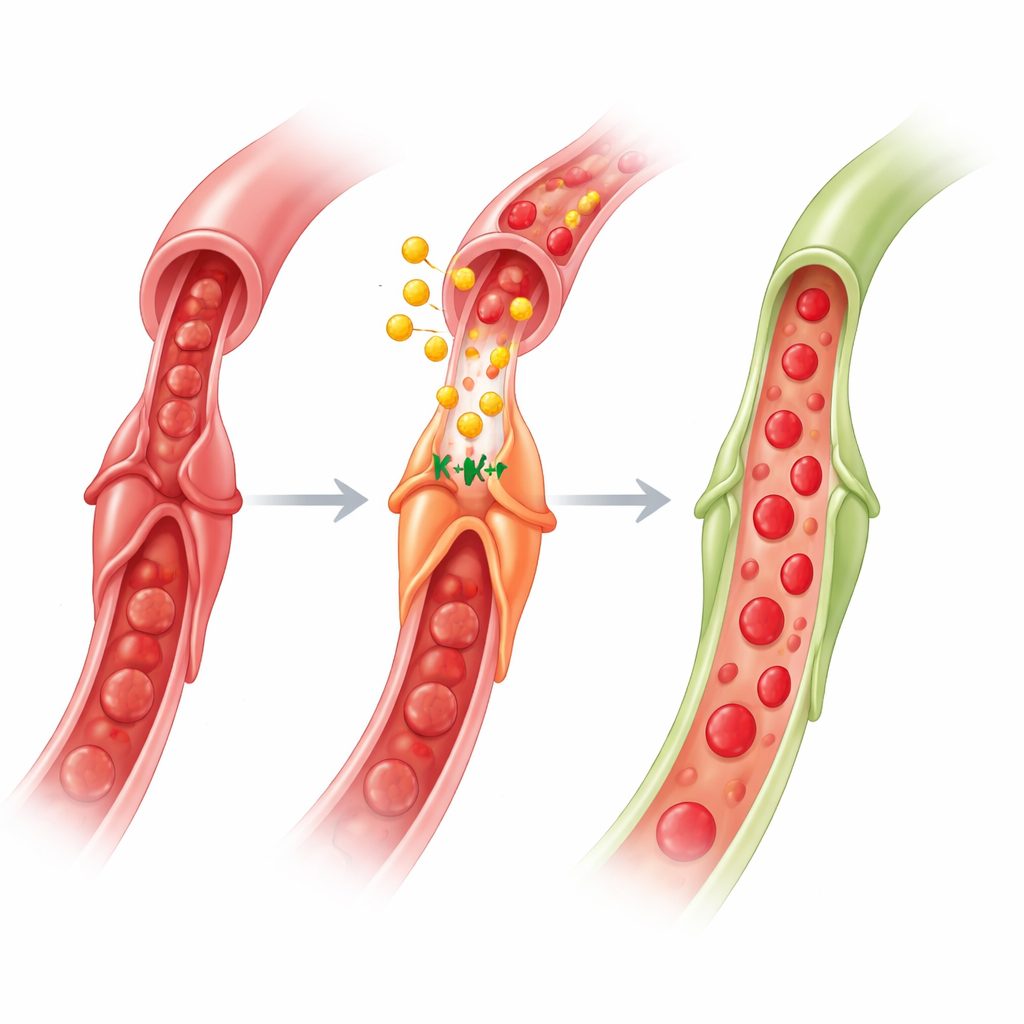
这对未来心脏治疗意味着什么
综合来看,这项工作揭示了一条脑–肠–心回路:肢体的短暂缺血信号激活通往肠道的神经,肠道细胞将GLP‑1释放到血液中,GLP‑1到达心脏并作用于周细胞。通过在AMPK、一氧化氮和乙酰胆碱的协助下调动KATP通道,GLP‑1使周细胞松开毛细血管,在动脉重新开放后恢复微循环中的血流。对非专业读者而言,关键点在于保护心脏不仅仅是疏通大动脉;同样重要的是让这些微小的守门细胞打开。由于基于GLP‑1的药物已广泛用于糖尿病和肥胖治疗并显示出心血管益处,针对在心脏病发作期间及之后调节周细胞功能来优化这些药物,可能为减少无再灌注并改善康复提供一种新途径。
引用: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
关键词: 心脏病发作, 微循环, GLP-1, 周细胞, 心脏保护