Clear Sky Science · pl
GLP-1 aktywuje kanały KATP w osierdziowych perycytach jako efektor sygnalizacji mózg‑jelita‑serce pośredniczącej w kardioprotekcji
Dlaczego ochrona maleńkich naczyń serca ma znaczenie
Gdy po zawale serca udrożniona zostaje zablokowana tętnica wieńcowa, wielu ludzi zakłada, że przepływ krwi zostaje w pełni przywrócony. Jednak u nawet połowy pacjentów najmniejsze naczynia w sercu pozostają zamknięte, więc części mięśnia sercowego nadal są pozbawione krwi. Ten utajony problem, zwany „no‑reflow” (brakiem ponownego przepływu), znacząco zwiększa ryzyko niewydolności serca i zgonu. Badanie streszczone tutaj odsłania szlak sygnalizacji mózg–jelita–serce, który może otwierać te maleńkie naczynia od wewnątrz, i sugeruje nowe sposoby ochrony serca przy użyciu leków już znanych z terapii cukrzycy.
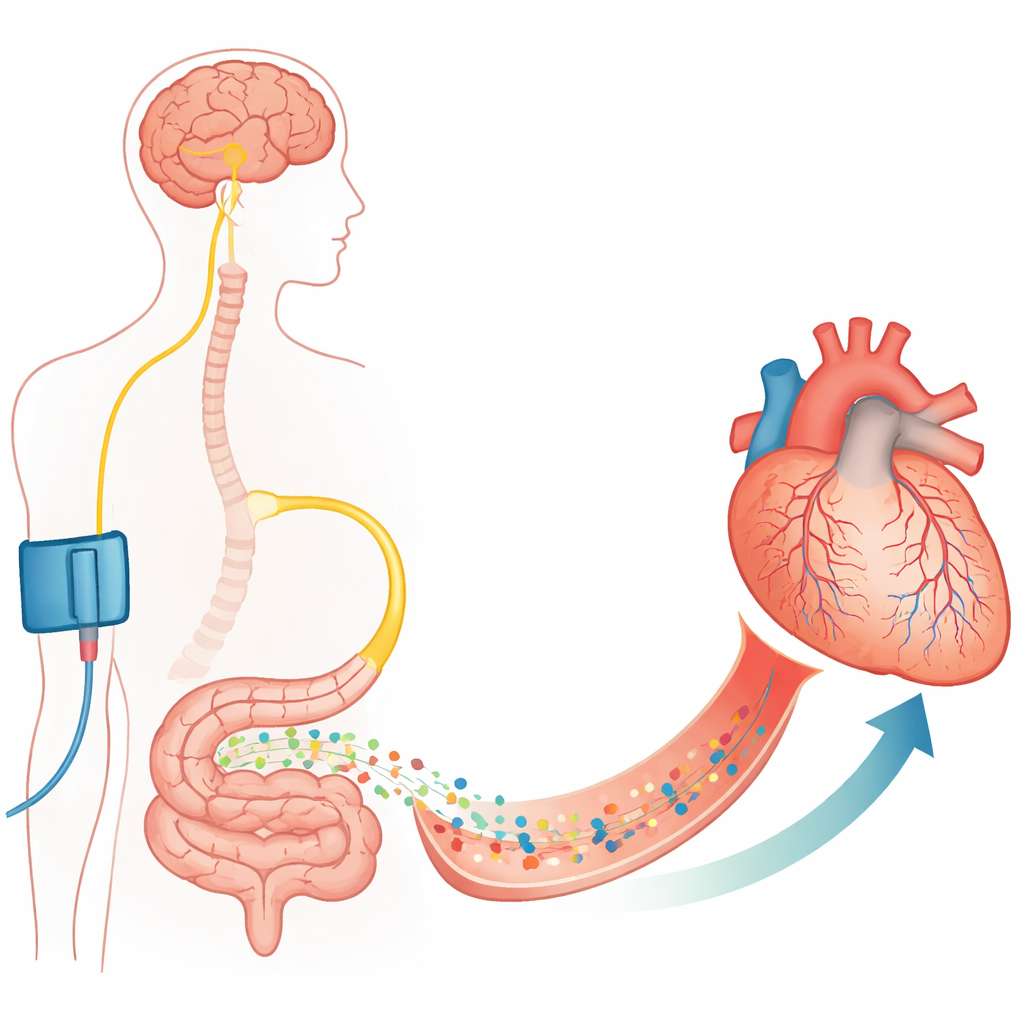
Od dużych tętnic do maleńkich komórek‑strażników
Udrożnienie zatkanej tętnicy wieńcowej przy użyciu stentu ratuje życie, ale nie zawsze wystarcza. Autorzy koncentrują się na naczyniach włosowatych — cienkich jak włos naczyniach, które faktycznie dostarczają tlen do mięśnia sercowego. Otaczające te naczynia komórki wsparcia, zwane perycytami, mogą ściskać lub rozluźniać ścianę naczynia. Wcześniejsze prace wykazały, że podczas i po okresie niedokrwienia perycyty się kurczą, a czasem umierają w stanie skurczu, trwale zwężając naczynia włosowate i powodując no‑reflow. To badanie potwierdza w sercach szczurów i myszy, że po kontrolowanym zamknięciu i ponownym otwarciu tętnicy wieńcowej wiele naczyń włosowatych pozostaje zwężonych w miejscu perycytów, a duża ich część przestaje przepuszczać krew, mimo że główna tętnica jest drożna.
Hormon z jelita, który „mówi” do naczyń włosowatych serca
Naukowcy zapytali następnie, czy organizm ma wbudowany sposób na rozluźnienie tych perycytów. Zbadali zjawisko zwane zdalnym przedconditioning niedokrwiennym, gdzie krótkotrwałe przerwanie przepływu krwi w kończynie (na przykład za pomocą mankietu) w jakiś sposób chroni serce przed późniejszym zablokowaniem. Wcześniejsze prace wskazywały nerw błędny i jelitowy hormon GLP‑1 jako kluczowe przekaźniki. Przy użyciu fluorescencyjnych sond i przeciwciał zespół wykazał obecność receptorów GLP‑1 na perycytach wieńcowych u myszy oraz w hodowlach ludzkich perycytów sercowych. U żywych szczurów krótkie niedokrwienie kończyn przed zamknięciem tętnicy wieńcowej wyraźnie zmniejszało zatory w naczyniach włosowatych i przywracało objętość perfundowanej krwi w zagrożonym obszarze serca — ale tylko jeśli receptory GLP‑1 były aktywne. Zablokowanie tych receptorów likwidowało korzyść i przywracało no‑reflow.
Jak GLP‑1 sprawia, że naczynia włosowate z powrotem się rozszerzają
Aby rozpracować mechanizm, autorzy użyli izolowanego, ciśnieniowego fragmentu serca myszy, gdzie mogli obserwować pojedyncze naczynia włosowate i perycyty pod mikroskopem. Gdy z płynu otaczającego tkankę usunęli tlen i glukozę, perycyty się skurczyły, a średnice naczyń włosowatych zmalały. Dodanie leku podobnego do GLP‑1 (Exendin‑4) podczas trwania warunków niskiego tlenu spowodowało rozluźnienie perycytów i niemal całkowite przywrócenie szerokości kapilar do pierwotnego stanu. Efekt ten znikał, jeśli zablokowano określony typ kanału jonowego znanego jako kanał potasowy wrażliwy na ATP (KATP) lub jeśli genetycznie usunięto kluczowy składnik KATP wyłącznie w perycytach. Podobnie, bezpośredni otwieracz kanałów KATP mógł odwrócić skurcz wywołany brakiem tlenu u normalnych myszy, lecz nie u myszy z wyłączonymi kanałami KATP w perycytach. Myszy pozbawione kanałów KATP w perycytach także utraciły korzyść ochronną z zdalnego przedconditioningu w eksperymentach na całym organizmie, co silnie wiąże te kanały z opisanym mechanizmem ochronnym.
Strojenie szlaku przez energetykę komórkową i sygnalizację
Opowieść sięga głębiej, jak te kanały są regulowane. Zespół wykazał, że kluczowa jest enzymatyczna czujka stanu energetycznego komórki, kinaza aktywowana przez AMP (AMPK). Zablokowanie AMPK uniemożliwiało GLP‑1 ponowne otwarcie zwężonych kapilar i przesuwało kanały KATP z dala od powierzchni komórkowej, co sugeruje, że AMPK pomaga przemieścić te kanały na błonę perycytów, gdzie mogą działać. Stwierdzono także, że zablokowanie produkcji tlenku azotu lub receptorów muskarynowych (acetylocholinowych) samo w sobie nie pogarszało skurczu, ale specyficznie blokowało rozszerzenie wywołane przez GLP‑1. Pasuje to do modelu, w którym tlenek azotu i acetylocholina działają upstream, pobudzając AMPK, który z kolei sprzyja trafickowaniu kanałów KATP i umożliwia GLP‑1 hiperpolaryzację i rozluźnienie perycytów.
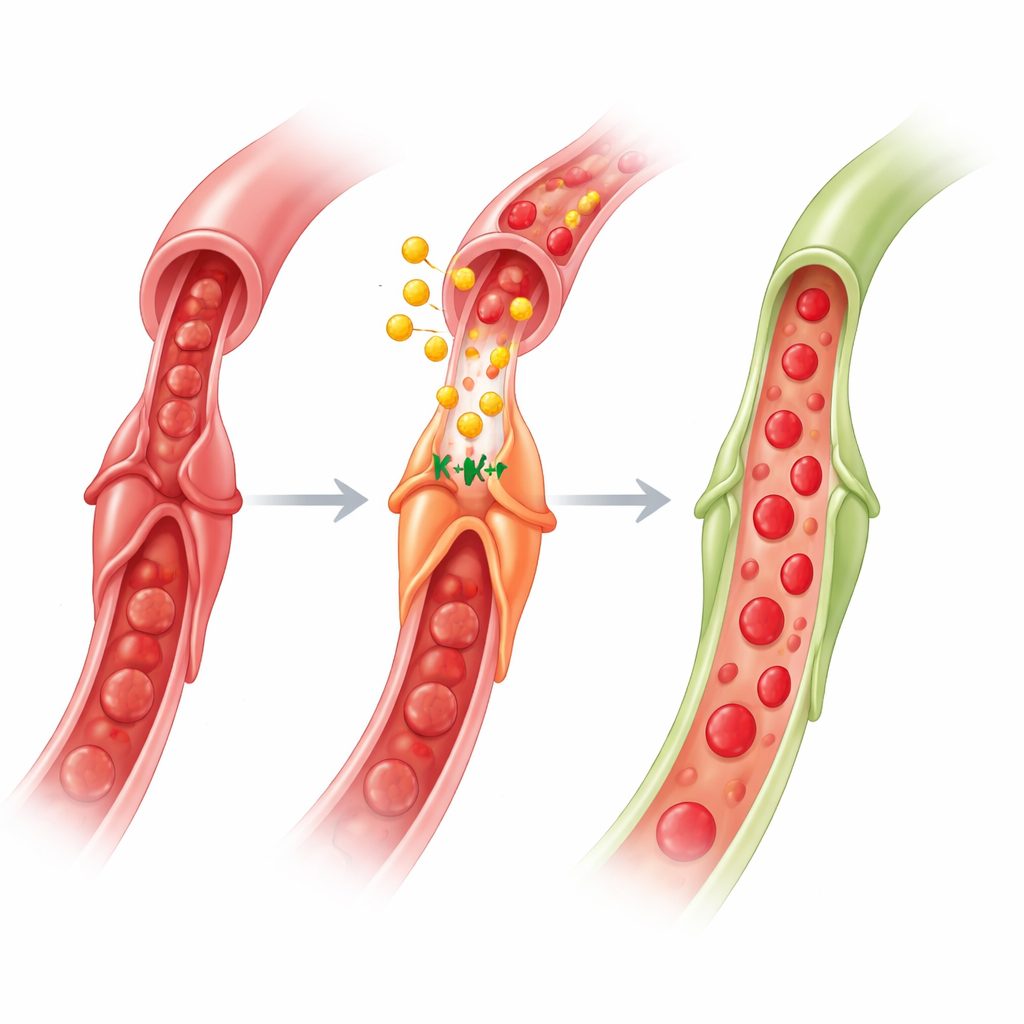
Co to oznacza dla przyszłych terapii serca
Sumarycznie praca ujawnia obwód mózg–jelito–serce: krótki sygnał niedokrwienny w kończynie aktywuje nerwy do jelit, komórki jelitowe uwalniają GLP‑1 do krwiobiegu, a GLP‑1 dociera do serca i działa na perycyty. Poprzez uruchomienie kanałów KATP — przy wsparciu AMPK, tlenku azotu i acetylocholiny — GLP‑1 powoduje, że perycyty odpuszczają naczyńkom włosowatym, przywracając przepływ w mikrokrążeniu po ponownym udrożnieniu tętnicy. Dla czytelników niebędących specjalistami kluczowy przekaz jest taki, że ochrona serca to nie tylko odblokowanie dużych tętnic; chodzi także o przekonanie maleńkich komórek‑strażników, by się otworzyły. Ponieważ leki oparte na GLP‑1 są już szeroko stosowane w leczeniu cukrzycy i otyłości oraz wykazały korzyści sercowo‑naczyniowe, ich dostrojenie pod kątem funkcji perycytów podczas i po zawale mogłoby dać nowy sposób ograniczania no‑reflow i poprawy zdrowienia.
Cytowanie: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Słowa kluczowe: zawał serca, mikrokrążenie, GLP-1, perycyty, kardioprotekcja