Clear Sky Science · tr
GLP-1, beyin-bağırsak-kalp sinyalleşmesinin etkileyicisi olarak koroner perisitlerde KATP kanallarını aktive eder ve kardiyoproteksiyon sağlar
Neden küçük kalp damarlarını korumak önemli?
Bir kalp krizi sonrasında tıkalı bir koroner arter tekrar açıldığında, birçok kişi kan akışının tamamen geri geldiğini varsayar. Oysa hastaların yarısına kadar olan bölümünde kalbin en küçük damarları kapalı kalır; bu nedenle kalp kasının bazı bölümleri kanla beslenmeye devam edemez. “No‑reflow” (yeniden akışın olmaması) olarak adlandırılan bu gizli sorun, kalp yetmezliği ve ölüm riskini önemli ölçüde artırır. Burada özetlenen çalışma, bu küçük damarları içeriden açabilen bir beyin–bağırsak–kalp sinyal yolunu ortaya koyuyor ve diyabet tedavisinde bilinen ilaçları kullanarak kalbi korumaya yönelik yeni yaklaşımlar öneriyor.
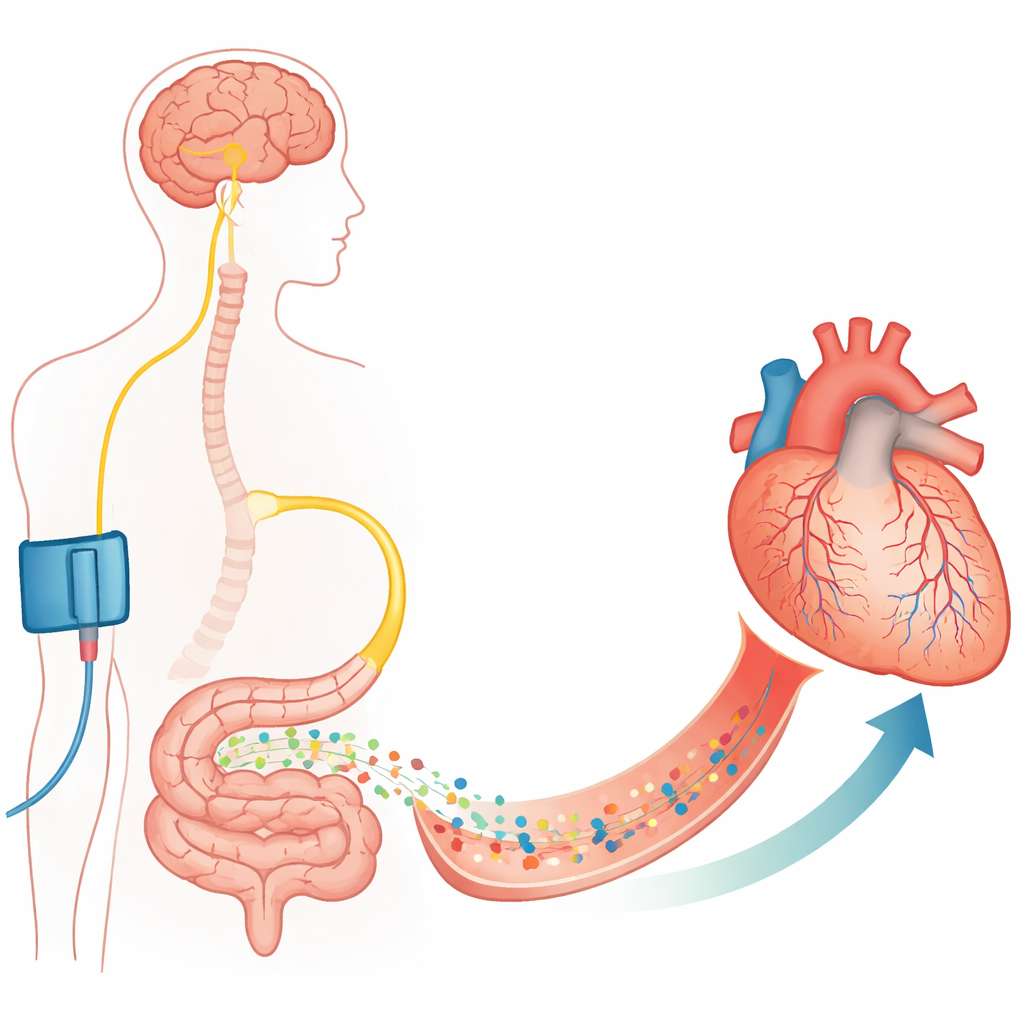
Büyük arterlerden küçük bekçi hücrelere
Tıkalı bir koroner arterin stentle açılması hayat kurtarıcıdır ama her zaman yeterli olmayabilir. Yazarlar, oksijeni gerçekten kalp kasına taşıyan kılcal damarlara odaklanıyor. Bu kılcal damarların etrafını saran ve damar duvarını sıkıp gevşetebilen destek hücrelerine perisit denir. Önceki çalışmalar, kan akışının kesildiği ve ardından geri geldiği dönemde perisitlerin sıkıştığını ve bazı durumlarda kasılmış halde ölüme gittiğini; bunun da kılcal damarları kalıcı olarak daraltıp no‑reflow’a yol açtığını göstermişti. Bu çalışma, kontrollü bir tıkanma ve yeniden açılma sonrası sıçan ve fare kalplerinde birçok kılcal damarın perisit bölgelerinde daraldığını ve ana arter açık olmasına rağmen büyük bir kısmının artık kan taşımadığını doğruluyor.
Kalp kılcal damarlarıyla konuşan bağırsaktan bir hormon
Araştırmacılar, vücudun bu perisitleri gevşetecek yerleşik bir yolu olup olmadığını sordular. Kısa süreli bir kol veya bacağın kan akışını kesmenin (örneğin manşonla) daha sonra ortaya çıkacak bir tıkanmaya karşı kalbi nasıl koruduğu anlamına gelen uzak iskemi ön koşullandırması olgusunu incelediler. Önceki çalışmalar vagus siniri ve bağırsak hormonu GLP‑1’i ana mesajcılar olarak işaret etmişti. Ekip, floresan problar ve antikorlar kullanarak fare koroner perisitlerinde ve kültüre edilmiş insan kalp perisitlerinde GLP‑1 reseptörlerinin bulunduğunu gösterdi. Yaşayan sıçanlarda, koroner tıkanmadan önce arka bacakları kısa süreli iskemiye uğratmak, perisit bölgelerindeki kılcal damar tıkanıklıklarını keskin biçimde azalttı ve tehlikedeki kalp bölgesinde perfüze kan hacmini geri getirdi—ancak yalnızca GLP‑1 reseptörleri aktifse. Bu reseptörleri bloke etmek faydayı ortadan kaldırdı ve no‑reflow geri geldi.
GLP‑1 kılcal damarları nasıl tekrar genişletiyor
Mechanizmayı ayırmak için yazarlar, tek tek kılcal damarları ve perisitleri mikroskop altında izleyebilecekleri izole, basınçlandırılmış bir fare kalp parçası kullandılar. Dokuyu saran sıvudan oksijen ve glukoz kaldırıldığında perisitler kasıldı ve kılcal damar çapları küçüldü. Düşük oksijen koşulları sürerken GLP‑1 benzeri bir ilaç (Exendin‑4) eklemek, perisitlerin gevşemesine ve kılcal damarların neredeyse orijinal genişliklerine yeniden ulaşmasına neden oldu. Bu etki, ATP‑duyarlı potasyum (KATP) kanalının belirli bir türünü bloke ettiklerinde veya yalnızca perisitlerde önemli bir KATP bileşenini genetik olarak ortadan kaldırdıklarında ortadan kayboldu. Benzer şekilde, doğrudan KATP kanal açıcı bir madde normal farelerde ilaçla indüklenen daralmayı tersine çevirebildi ama perisit KATP knockout farelerinde bunu yapamadı. Perisit KATP kanallarından yoksun fareler, tüm organizmada yapılan uzak ön koşullandırmanın kalp koruyucu faydasını da kaybetti; bu da bu kanalları koruyucu yolakla sağlam biçimde ilişkilendiriyor.
Hücresel enerji ve sinyalizasyonla yolun hassas ayarı
Hikâye bu kanalların nasıl kontrol edildiğine dair daha derine iniyor. Ekip, hücresel enerji durumunu algılayan bir enzim olan AMP‑aktive protein kinazın (AMPK) kritik olduğunu gösterdi. AMPK’nın bloke edilmesi, GLP‑1’in daralmış kılcal damarları tekrar açmasını engelledi ve KATP kanallarını hücre yüzeyinden uzaklaştırdı; bu da AMPK’nın bu kanalları perisit zarında işlev görebilecek konuma taşımasına yardımcı olduğunu düşündürüyor. Ayrıca nitrik oksit üretimini veya muskarinik (asetilkolin) reseptörlerini bloke etmenin tek başına daralmayı kötüleştirmediğini, ancak özellikle GLP‑1 tarafından tetiklenen genişlemeyi engellediğini buldular. Bu, nitrik oksit ve asetilkolinin upstream (üst akış) olarak AMPK’yı uyardığı, AMPK’nın ise KATP kanal taşınmasını teşvik edip GLP‑1’in perisitleri hiperpolarize ederek gevşetmesini mümkün kıldığı bir modele uyuyor.
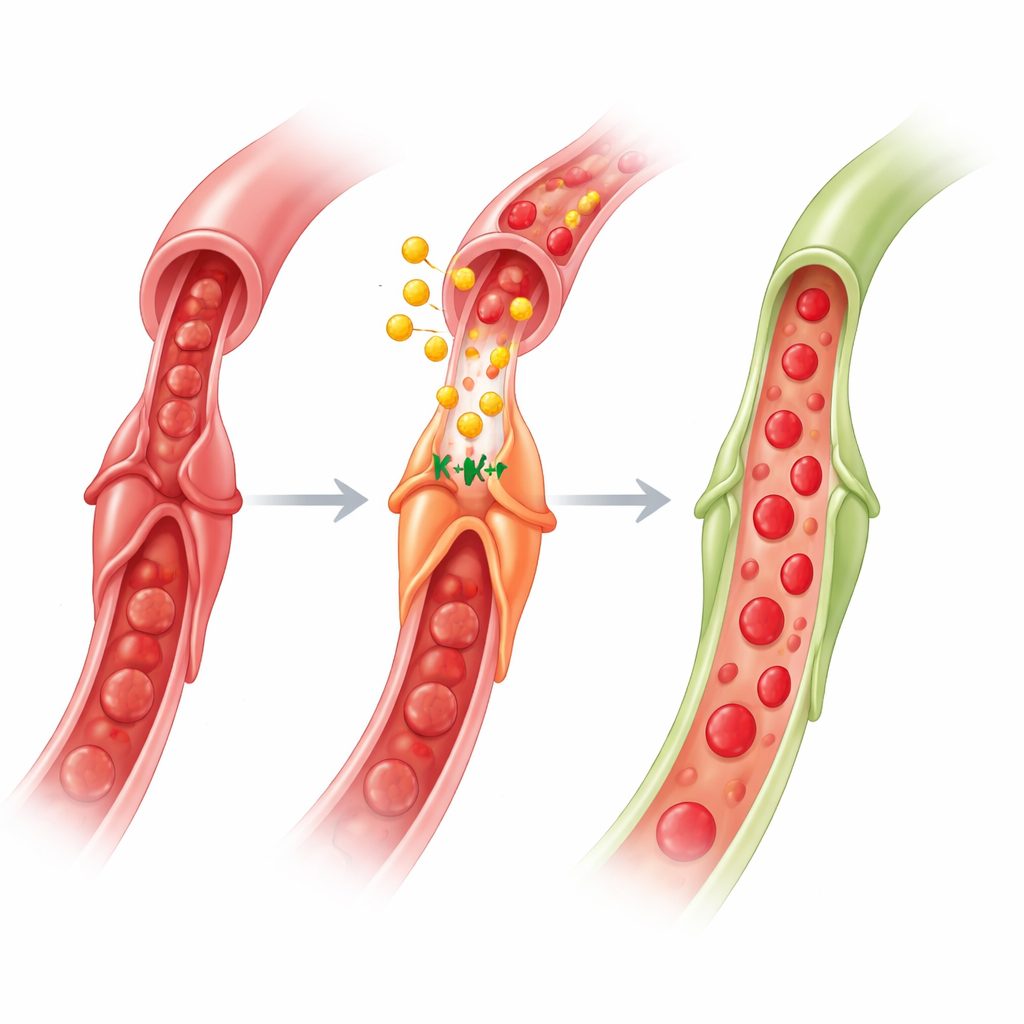
Gelecekteki kalp tedavileri için bunun anlamı
Toparlanınca, çalışma bir beyin–bağırsak–kalp devresini ortaya koyuyor: bir ekstremitede kısa süreli iskemi sinyali sinirleri bağırsaklara etkinleştiriyor, bağırsak hücreleri GLP‑1’i kana salıyor ve GLP‑1 kalbe giderek perisitler üzerinde etkili oluyor. AMPK, nitrik oksit ve asetilkolinin yardımıyla KATP kanallarını devreye sokan GLP‑1, perisitlerin kılcal damarları bırakmasını sağlayarak bir arter yeniden açıldıktan sonra mikro dolaşımda akışı geri getiriyor. Uzman olmayanlar için ana mesaj, kalbi korumanın yalnızca büyük arterlerin tıkanıklığını gidermekle ilgili olmadığı; küçük bekçi hücreleri açmaya ikna etmekle de ilgili olduğudur. GLP‑1 bazlı ilaçlar zaten diyabet ve obezite için yaygın olarak kullanılıyor ve kardiyovasküler fayda gösterdiklerinden, bu ilaçları kalp krizi sırasında ve sonrasında perisit fonksiyonunu hedefleyecek şekilde geliştirmek no‑reflow’u azaltmak ve iyileşmeyi artırmak için yeni bir yol sunabilir.
Atıf: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Anahtar kelimeler: kalp krizi, mikrosirkülasyon, GLP-1, perisitler, kardiyoproteksiyon