Clear Sky Science · it
GLP-1 attiva i canali KATP nei periciti coronarici come effettore del segnale cervello-intestino-cuore che media la cardioprotezione
Perché proteggere i vasi minuscoli del cuore è importante
Quando un’arteria coronaria ostruita viene riaperta dopo un infarto, molti pensano che il flusso sanguigno sia completamente ristabilito. Eppure, in fino a metà dei pazienti, i vasi sanguigni più piccoli del cuore rimangono chiusi, lasciando parti del muscolo cardiaco in condizioni di ischemia. Questo problema nascosto, chiamato “no‑reflow”, aumenta notevolmente il rischio di insufficienza cardiaca e morte. Lo studio qui riassunto scopre una via di segnalazione cervello–intestino–cuore che può riaprire questi vasi minuscoli dall’interno e suggerisce nuovi modi per proteggere il cuore usando farmaci già noti nel trattamento del diabete.
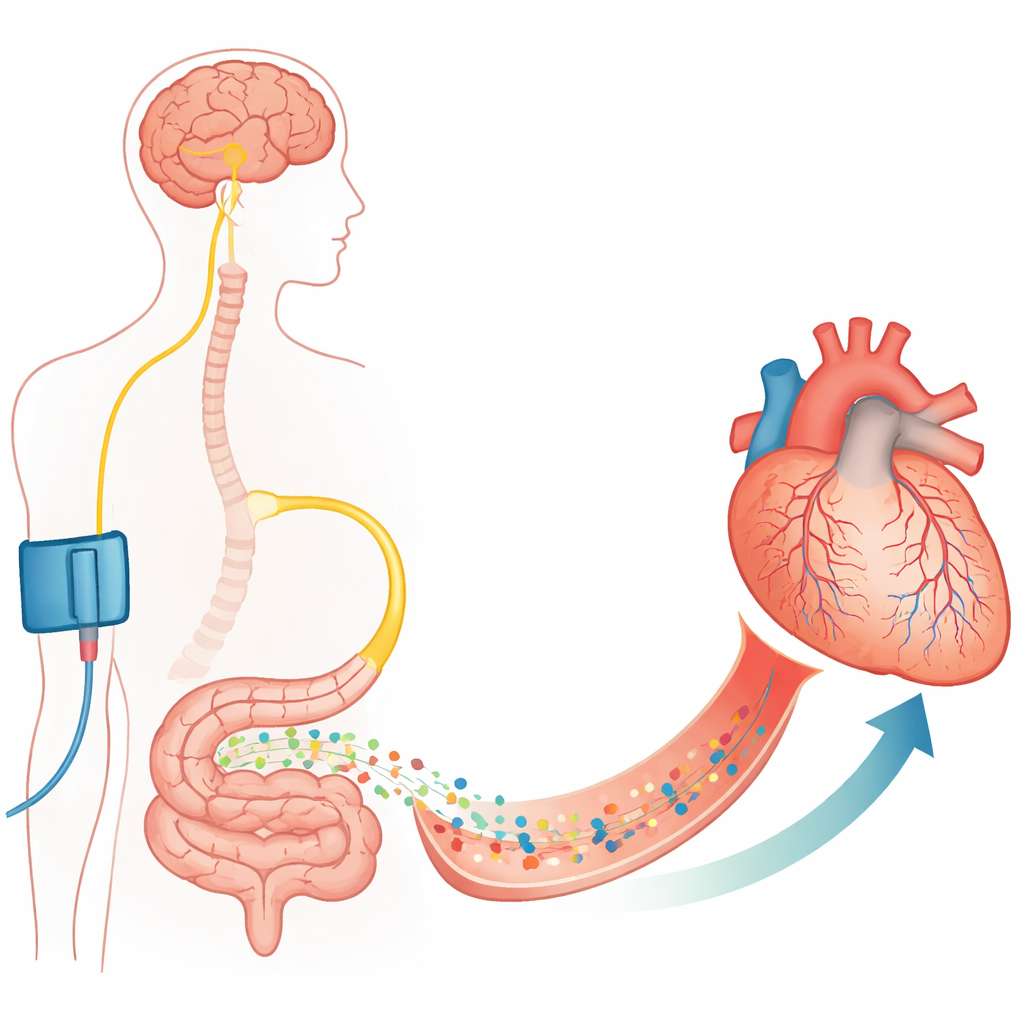
Dalle grosse arterie alle piccole cellule guardiane
Riaprire un’arteria coronaria ostruita con uno stent salva la vita ma non è sempre sufficiente. Gli autori si concentrano sui capillari, i vasi sottilissimi che forniscono ossigeno al muscolo cardiaco. Avvolti intorno a questi capillari ci sono cellule di supporto chiamate periciti, che possono contrarre o rilassare la parete del vaso. Lavori precedenti hanno mostrato che durante e dopo un periodo di assenza di flusso queste cellule si contraggono e talvolta muoiono in stato contratto, riducendo permanentemente il diametro dei capillari e causando il no‑reflow. Questo studio conferma, in cuori di ratto e di topo, che dopo un’occlusione controllata e la riapertura di un’arteria coronaria molti capillari restano ristretti nei siti dei periciti e una larga frazione non è più perfusa, anche se l’arteria principale è pervia.
Un ormone intestinale che parla ai capillari cardiaci
I ricercatori si sono poi chiesti se l’organismo abbia un modo intrinseco per rilassare questi periciti. Hanno esaminato un fenomeno chiamato precondizionamento ischemico remoto, in cui una breve interruzione del flusso sanguigno a un arto (per esempio con un laccio) protegge in qualche modo il cuore da una successiva occlusione. Lavori precedenti indicavano il nervo vago e l’ormone intestinale GLP‑1 come messaggeri chiave. Utilizzando sonde fluorescenti e anticorpi, il gruppo ha dimostrato che i recettori del GLP‑1 sono presenti sui periciti coronarici nei topi e in periciti cardiaci umani coltivati. In ratti vivi, rendere ischemici brevemente gli arti posteriori prima di un’occlusione coronarica ha ridotto drasticamente le ostruzioni capillari e ripristinato il volume di sangue perfuso nella regione cardiaca a rischio—ma solo se i recettori del GLP‑1 erano attivi. Bloccare questi recettori annullava il beneficio e riportava il no‑reflow.
Come il GLP‑1 fa riaprirsi i capillari
Per analizzare il meccanismo, gli autori hanno usato un frammento isolato e pressurizzato di cuore di topo dove potevano osservare singoli capillari e periciti al microscopio. Quando hanno rimosso ossigeno e glucosio dal liquido che nutriva il tessuto, i periciti si sono contratti e i diametri capillari si sono ridotti. L’aggiunta di un farmaco simile al GLP‑1 (Exendin‑4) mentre le condizioni di ipossia continuavano ha indotto il rilassamento dei periciti e la riespansione dei capillari quasi fino al diametro originale. Questo effetto scompariva se veniva bloccato un tipo specifico di canale ionico noto come canale del potassio sensibile all’ATP (KATP) o se un componente chiave del KATP veniva rimosso geneticamente solo nei periciti. Analogamente, un apritore diretto dei canali KATP poteva invertire la costrizione indotta dalla malattia nei topi normali ma non nei topi con knockout del KATP nei periciti. I topi privi dei canali KATP nei periciti perdevano anche il beneficio cardioprotettivo del precondizionamento remoto negli esperimenti sull’animale intero, collegando in modo definitivo questi canali alla via protettiva.
Affinare la via con energia cellulare e segnalazione
La storia si addentra nel controllo di questi canali. Il gruppo ha mostrato che un enzima sensore dello stato energetico cellulare, la proteina chinasi attivata da AMP (AMPK), è cruciale. Bloccare l’AMPK impediva al GLP‑1 di riaprire i capillari costretti e spostava i canali KATP lontano dalla superficie cellulare, suggerendo che l’AMPK aiuta a traslocare questi canali sulla membrana dei periciti dove possono funzionare. Hanno anche osservato che bloccare la produzione di ossido nitrico o i recettori muscarinici (acetilcolina) non peggiorava la costrizione di per sé, ma bloccava specificamente la dilatazione indotta dal GLP‑1. Questo si adatta a un modello in cui ossido nitrico e acetilcolina agiscono a monte stimolando AMPK, che a sua volta promuove il traffico dei canali KATP e permette al GLP‑1 di iperpolarizzare e rilassare i periciti.
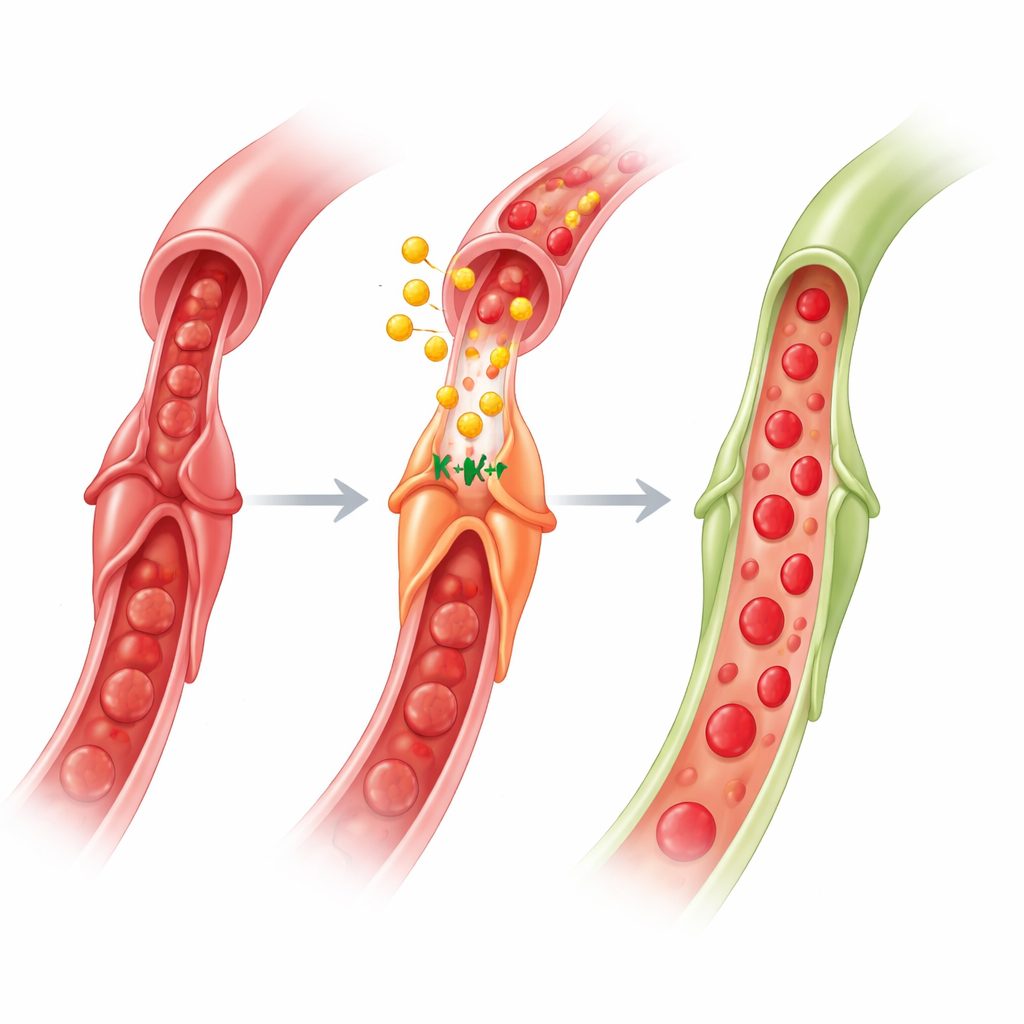
Cosa significa per i trattamenti cardiaci futuri
Nel complesso, il lavoro rivela un circuito cervello–intestino–cuore: un breve segnale ischemico in un arto attiva i nervi diretti all’intestino, le cellule intestinali rilasciano GLP‑1 nel flusso sanguigno e il GLP‑1 raggiunge il cuore per agire sui periciti. Attivando i canali KATP—con il contributo di AMPK, ossido nitrico e acetilcolina—il GLP‑1 fa sì che i periciti lascino andare i capillari, ripristinando il flusso nella microcircolazione dopo la riapertura di un’arteria. Per i non specialisti, il messaggio principale è che proteggere il cuore non riguarda solo lo sbloccare le grandi arterie; riguarda anche convincere le minuscole cellule guardiane ad aprirsi. Poiché i farmaci a base di GLP‑1 sono già largamente usati per diabete e obesità e hanno mostrato benefici cardiovascolari, perfezionarli per mirare alla funzione dei periciti durante e dopo gli infarti potrebbe offrire un nuovo modo per ridurre il no‑reflow e migliorare il recupero.
Citazione: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Parole chiave: infarto, microcircolazione, GLP-1, periciti, cardioprotezione