Clear Sky Science · nl
GLP-1 activeert KATP-kanalen in coronare pericyten als effectormechanisme van hersen-darm-hart-signaaloverdracht die cardioprotectie medieert
Waarom het beschermen van kleine hartvaten ertoe doet
Wanneer een afgesloten kransslagader wordt heropend na een hartinfarct, gaan veel mensen ervan uit dat de bloedstroom volledig is hersteld. Toch blijven bij tot de helft van de patiënten de allerkleinste bloedvaten in het hart dicht, zodat delen van de hartspier toch van bloed worden beroofd. Dit verborgen probleem, “no‑reflow” genoemd, verhoogt het risico op hartfalen en overlijden sterk. De hier samengevatte studie onthult een hersen–darm–hart signaalweg die deze kleine vaten van binnenuit kan openen en suggereert nieuwe manieren om het hart te beschermen met geneesmiddelen die al bekend zijn uit de diabetesbehandeling.
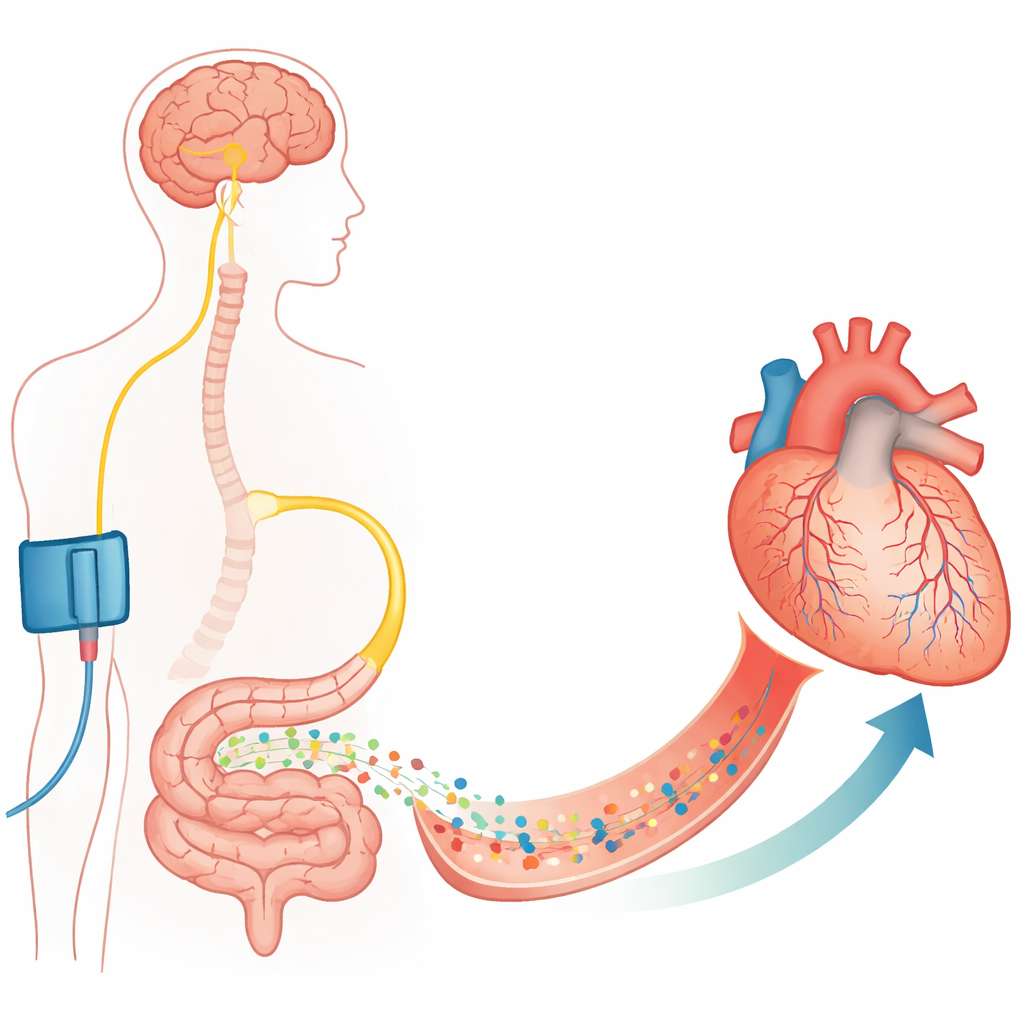
Van grote slagaders naar kleine poortwachters
Het openen van een verstopte kransslagader met een stent redt levens maar is niet altijd voldoende. De auteurs richten zich op haarvaten, de ultradunne vaten die daadwerkelijk zuurstof aan de hartspier leveren. Rond deze haarvaten liggen steuncellen, pericyten genaamd, die de vaatwand kunnen samentrekken of ontspannen. Eerder werk toonde dat deze pericyten tijdens en na een periode zonder bloed samentrekken en soms doodgaan in een gecontracteerde toestand, waardoor haarvaten blijvend vernauwen en no‑reflow ontstaat. Deze studie bevestigt in rat‑ en muizenharten dat na een gecontroleerde afsluiting en heropening van een kransslagader veel haarvaten ter hoogte van pericyten vernauwd blijven en een groot deel geen bloed meer voert, zelfs als de hoofdslagader doorgankelijk is.
Een hormoon uit de darm dat met harthaarvaten praat
De onderzoekers vroegen zich vervolgens af of het lichaam een ingebouwde manier heeft om deze pericyten te ontspannen. Ze onderzochten een fenomeen genaamd remote ischemische preconditionering, waarbij het kort afklemmen van de bloedtoevoer naar een ledemaat (bijvoorbeeld met een manchet) op de een of andere manier het hart beschermt tegen een latere afsluiting. Eerder werk wees op de nervus vagus en het darmhormoon GLP‑1 als belangrijke boodschappers. Met fluorescerende sondes en antilichamen liet het team zien dat GLP‑1‑receptoren aanwezig zijn op coronare pericyten in muizen en op gekweekte menselijke hartpericyten. In levende ratten verminderde het kort ischemisch maken van de achterpoten vóór een kransslagaderafsluiting scherp het aantal afgesloten haarvaten en herstelde het met bloed gevulde volumedeel van het bedreigde hartgebied—maar alleen als GLP‑1‑receptoren actief waren. Het blokkeren van deze receptoren tilde het voordeel op en deed no‑reflow terugkeren.
Hoe GLP‑1 haarvaten weer doet wijder worden
Om het mechanisme te ontleden gebruikten de auteurs een geïsoleerd, geperst deel van een muizenhart waarin ze onder een microscoop individuele haarvaten en pericyten konden volgen. Wanneer ze zuurstof en glucose uit de vloeistof rond het weefsel verwijderden, trokken pericyten samen en krompen de haarvatdiameters. Het toevoegen van een GLP‑1‑achtig middel (Exendin‑4) terwijl de laag‑zuurstofcondities aanhielden, liet de pericyten ontspannen en de haarvaten bijna tot hun oorspronkelijke breedte terugveren. Dit effect verdween als ze een specifiek type ionkanaal blokkeerden dat bekendstaat als een ATP‑gevoelig kaliumkanaal (KATP) of wanneer ze genetisch een essentieel KATP‑component uitsluitend in pericyten verwijderden. Evenzo kon een directe KATP‑kanalenopener de door zuurstofgebrek veroorzaakte vernauwing bij normale muizen omkeren, maar niet bij pericyt‑specifieke KATP‑knockouts. Muizen zonder pericyt KATP‑kanalen verloren ook het hartbeschermende voordeel van remote preconditioning in intacte dierexperimenten, waarmee deze kanalen stevig aan de beschermende route worden gekoppeld.
Fijnregeling van de route met cellulaire energie en signaaloverdracht
Het verhaal gaat dieper in op hoe deze kanalen worden geregeld. Het team toonde aan dat een enzym dat de cellulaire energiestatus waarneemt, AMP‑geactiveerde proteïnekinase (AMPK), cruciaal is. Het blokkeren van AMPK verhinderde dat GLP‑1 vernauwde haarvaten weer opende en verplaatste KATP‑kanalen weg van het celoppervlak, wat suggereert dat AMPK helpt deze kanalen naar de pericyt‑membraan te brengen waar ze kunnen functioneren. Ze vonden ook dat het blokkeren van stikstofoxideproductie of muscarine (acetylcholine) receptoren de vernauwing op zichzelf niet verergerde, maar specifiek de door GLP‑1 geïnduceerde verwijding blokkeerde. Dit past bij een model waarin stikstofoxide en acetylcholine upstream werken door AMPK te stimuleren, wat op zijn beurt KATP‑kanaaltrafficking bevordert en GLP‑1 in staat stelt pericyten te hyperpolariseren en te ontspannen.
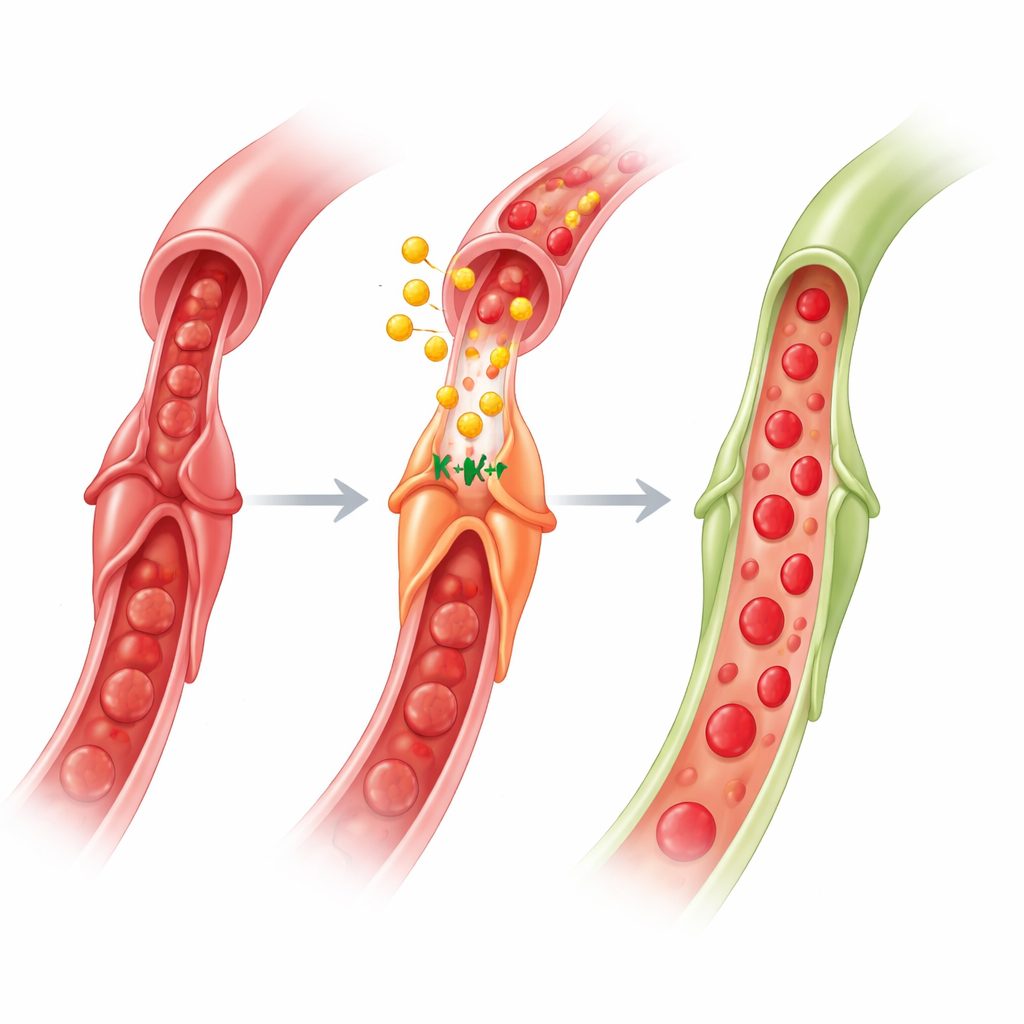
Wat dit betekent voor toekomstige hartbehandelingen
Alles bij elkaar onthult het werk een hersen–darm–hart circuit: een korte ischemische prikkel in een ledemaat activeert zenuwen naar de darm, darmcellen geven GLP‑1 af in de bloedbaan, en GLP‑1 reist naar het hart om op pericyten in te werken. Door KATP‑kanalen te betrekken—met hulp van AMPK, stikstofoxide en acetylcholine—laat GLP‑1 pericyten de haarvaten los, waardoor de doorstroming in de microcirculatie wordt hersteld nadat een slagader is heropend. Voor niet‑specialisten is de kernboodschap dat het beschermen van het hart niet alleen gaat om het openmaken van grote slagaders; het gaat ook om het overtuigen van kleine poortwachtercellen om te openen. Omdat GLP‑1‑gebaseerde geneesmiddelen al veel worden gebruikt voor diabetes en obesitas en cardiovasculaire voordelen hebben laten zien, kan het verfijnen van deze middelen om pericytfunctie tijdens en na hartinfarcten te beïnvloeden een nieuwe manier bieden om no‑reflow te verminderen en het herstel te verbeteren.
Bronvermelding: Mastitskaya, S., de Freitas, F.S.S., Evans, L.E. et al. GLP-1 activates KATP channels in coronary pericytes as the effector of brain-gut-heart signalling mediating cardioprotection. Nat Commun 17, 2773 (2026). https://doi.org/10.1038/s41467-026-69555-1
Trefwoorden: hartinfarct, microcirculatie, GLP-1, pericyten, cardioprotectie